DNA修复研究领域重要成果解读!
来源:本站原创 2019-05-21 23:03
近年来,科学家们在DNA修复研究领域进行了深入探索,也取得了很多可喜的成绩,本文中,小编就整理了近期的重要研究成果,与大家一起学习!【1】Cell:科学家鉴别出维持细胞基因组完整性的新型DNA修复机制doi:10.1016/j.cell.2018.10.055日前,一项刊登在国际杂志Cell上的研究报告中,来自范德堡大学的科学家们通过研究鉴别出了保持基因组完整性的新型DNA修复机制。研究者表示,这
近年来,科学家们在DNA修复研究领域进行了深入探索,也取得了很多可喜的成绩,本文中,小编就整理了近期的重要研究成果,与大家一起学习!

【1】Cell:科学家鉴别出维持细胞基因组完整性的新型DNA修复机制
doi:10.1016/j.cell.2018.10.055
日前,一项刊登在国际杂志Cell上的研究报告中,来自范德堡大学的科学家们通过研究鉴别出了保持基因组完整性的新型DNA修复机制。研究者表示,这种机制是由一种名为HMCES的蛋白质所开启的,HMCES是此前研究者所鉴别出的200多种蛋白质家族的一种,这些蛋白质属于特殊分子机器的一员,其能在细胞分裂时帮助DNA进行复制。其中有些蛋白质是用于与DNA复制相关的功能,而包括HMCES在内的一些蛋白质则并未发现该功能。
研究者Cortez说道,每一种有机体中都有HMCES样的蛋白质,比如人类、细菌等;这项研究中我们剔除了细胞中的HMCES基因来寻找细胞复制中的问题,但研究者并未发现任何问题,即缺失HMCES的细胞依然能够正常进行分裂和DNA复制;当研究者利用损伤的DNA来挑战这些细胞时他们发现,HMCES对于维持细胞健康至关重要。
【2】Nature:重磅!CDK12控制着DNA修复基因的RNA转录本长短
doi:10.1038/s41586-018-0758-y
基因BRCA1和BRCA2发生突变对乳腺癌和卵巢癌构成严重风险,这是因为它们通过干扰同源重组修复(HR)来危害细胞的基因组稳定性,其中同源重组修复是一种准确地修复有害的DNA双链断裂的关键机制。如果没有利用这种机制修复DNA双链断裂的能力,那么细胞就不得不采用更容易出错因而更容易发生癌变的DNA修复方式。
基因BRCA1和BRCA2不是唯一的当发生突变时会导致无法利用同源重组修复DNA双链断裂而促进肿瘤发生的基因。已知22个基因发生的突变会破坏同源重组修复,从而产生具有“BRCAness”表型的肿瘤。已知在这22个BRCAness基因中,除了其中的一个基因之外的所有其他的BRCAness基因都直接参与同源重组修复通路。
【3】Nature:重磅!揭示Shieldin蛋白复合物在DNA修复中起关键性作用
doi:10.1038/s41586-018-0340-7
在一项新的里程碑研究中,来自加拿大多伦多大学、英国伦敦癌症研究所、荷兰癌症研究院和瑞士伯尔尼大学的研究人员分析了乳腺癌细胞和携带着BRCA1基因突变的小鼠。他们利用前沿的CRISPR/Cas9基因操纵技术寻找导致癌细胞对PARP抑制剂药物奥拉帕尼(olaparib)和talaoparib以及铂类化疗药物顺铂(cisplatin)产生耐药性的基因突变。
通过一番艰苦的实验,这些研究人员能够找出导致耐药性产生的关键性基因突变,这些突变对哪些蛋白产生影响,并揭示出这些蛋白在细胞中发挥的作用。他们发现细胞中的一种全新的蛋白复合物能够保护断裂DNA的末端并且控制着这种断裂DNA的修复方式,而且这种被命名为Shieldin的蛋白复合物由新鉴定出的蛋白SHLD1、SHLD2和SHLD3组成。
【4】Nat Struct Mol Biol:科学家发现DNA修复蛋白的特殊开关
doi:10.1038/s41594-018-0083-z
DNA损伤是一种日常发生的现象,而人类细胞早已经学会如何应对这种状况了,日前,一项刊登在国际杂志Nature Structural & Molecular Biology上的研究报告中,来自梅奥诊所的研究人员通过研究阐明了一种DNA修复蛋白如何到达DNA的损伤位点,相关研究或能帮助研究人员开发出治疗卵巢癌的新型疗法。
当人类基因组受到持续性损伤时,细胞中就会产生检测并且修复损伤的蛋白质,其中一种蛋白质名为53BP1,当DNA链破碎时其主要参与修复DNA的功能,这项研究中,研究人员阐明了蛋白质53BP1如何重新定位到染色体上来发挥其作用。研究者Mer解释道,当不存在DNA损伤时,53BP1就会被TIRR阻断从而处于失活状态,利用X射线晶体学技术,研究人员发现,TIRR能够阻断53BP1的区域,从而使得53BP1用来结合染色体;但TIRR如何脱离53BP1的呢?这种修复蛋白又是如何发挥作用的呢?
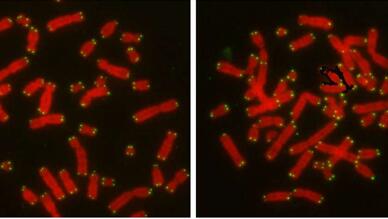
【5】Science:我国科学家解析出DNA修复关键组分Mec1-Ddc2的三维结构
doi:10.1126/science.aan8414
细胞不断地复制以便修复和替换受损组织,而且每次细胞分裂都需要复制DNA。 当DNA复制时,错误不可避免地发生,这会造成DNA损害,如果不加以修复的话,那么这可能导致细胞死亡。
作为DNA损伤的第一个线索,一种被称作ATR激酶的蛋白激活细胞的内在修复系统。如今,在一项新的研究中,来自中国科技大学、中科院分子细胞科学卓越创新中心和南京农业大学的研究人员以前所未有的分辨率解析出这种蛋白的结构图,并开始理解它对DNA损伤作出的反应;研究者表示,ATR蛋白是应对DNA损伤和复制应激(replication stress)的顶端激酶。长期以来,一个关键的问题是确定ATR激酶的激活机制---它如何对DNA损伤作出反应,以及它如何被激活。
【6】Nature子刊:重大突破!利用CRISPR-Gold在体内诱导同源介导的DNA修复
doi:10.1038/s41551-017-0137-2
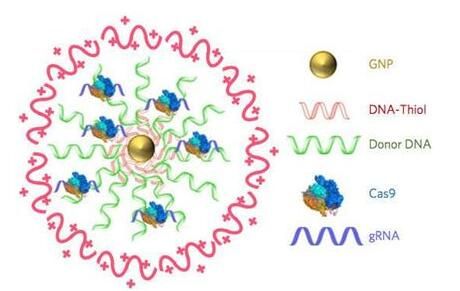
虽然很有前景,但是CRISPR-Cas9基因编辑的应用迄今为止因遭受运送挑战---也就是如何把所有的CRISPR组分提供给每个需要它们的细胞中---而受到限制。在一项新的研究中,来自美国加州大学伯克利分校等机构的研究人员通过注射一种他们称为CRISPR-Gold的载体,成功地修复杜兴氏肌肉营养不良(Duchenne muscular dystrophy)模式小鼠体内发生的抗肌营养不良蛋白(dystrophin)基因突变。CRISPR-Gold含有Cas9蛋白、向导RNA(gRNA)和供者DNA,它们都被包被在微小的金纳米颗粒周围。
杜兴氏肌肉营养不良是是一种由抗肌营养不良蛋白缺乏引起的肌肉退化性疾病。在大约三分之一的患者中,编码抗肌营养不良蛋白的基因发生小片段缺失或者单碱基突变,从而使得它丧失功能,这就让这种基因成为基因编辑的一种极佳的候选对象。科学家们之前已利用病毒运送CRISPR-Cas9组分来剔除这个基因中发生突变的外显子,并且让这种疾病的模式小鼠获得临床上的症状改善。
【7】Nature:重大突破!揭示蛋白CYREN调节细胞选择DNA修复途径之谜
doi:10.1038/nature24023
是快速地做事情但会犯错误更好,还是做得慢些但做得完美更好呢?当决定选择如何修复DNA中的断裂时,细胞在两种主要的修复途径之间面临着同样的选择。这种决定比较重要,这是因为错误的决定可能导致更多的DNA损伤和癌症。
如今,在一项新的研究中,来自美国沙克生物研究所、加州大学圣地亚哥分校和英国弗朗西斯-克里克研究所的研究人员发现一种被称作CYREN的小分子蛋白协助细胞在合适的时间选择合适的修复途径,这就阐明了一个长期存在的关于DNA修复的谜团,并且为科学家们提供一种强大的工具,从而可能指导人们开发出更好的癌症疗法。
【8】Mol Cell:揭示出蛋白Rad52在RNA依赖性DNA修复中发挥关键性作用
doi:10.1016/j.molcel.2017.05.019
在一项新的研究中,来自美国德雷塞尔大学和佐治亚理工学院的研究人员发现同源重组蛋白Rad52如何在RNA依赖性的DNA修复中发挥着至关重要的作用。这一研究结果揭示出这种蛋白的一种令人吃惊的作用,并且可能有助鉴定出新的癌症治疗靶标。相关研究结果于2017年6月8日在线发表在Molecular Cell期刊上。
放疗和化疗能够导致DNA双链断裂(最为有害的DNA损伤类型之一)。同源重组过程涉及在两个DNA分子之间交换遗传信息,在DNA修复中发挥着重要的作用,但是某些基因突变能够导致基因组失去稳定。比如,参与通过同源重组修复DNA损伤的肿瘤抑制基因BRCA2当发生突变时,能够导致致命性的乳腺癌和卵巢癌。
【9】PNAS:揭示DNA修复酶APE2结构域Zf-GRF的功能
doi:10.1073/pnas.1610011114
一项新的研究揭示出一种保守性的酶组分Zf-GRF结构域的功能。它是DNA修复过程期间操纵DNA所必需的一种关键性的分子组分。活的有机体的DNA需要经常性的维护。每个细胞处于一种受到激烈围攻的状态,这是因为大量的活性氧化合物和离子经常攻击和破坏这个细胞的有机分子,特别是它的DNA。据估计,每个细胞每天发生的DNA氧化损伤超过1万次。
为了让生命在这个分子战场中存活下来,分子对策已进化出,在它们当中,一系列复合物分子检测DNA分子中遭受到氧化损伤的区域,随后多种修复分子靶向这些区域,并且进行一系列复杂的分子工程操作以便修复这些区域。然而,负责识别和修复DNA损伤的复杂分子组装体的详细工作机制尚未完全查明。
doi:10.1016/j.cell.2016.10.001
日前,一项刊登在国际杂志Cell上的研究报告中,来自澳大利亚国立大学和德国海德堡大学的研究人员通过研究发现了一种DNA修复过程中的必要组分,该研究或为后期开发新型抗癌药物提供一定的思路。
研究者Tamas Fischer教授指出,当DNA被损伤后,由DNA和RNA组成的混合结构在修复遗传信息上扮演着重要角色,RNAs是一种储存在DNA中短暂的遗传信息副本;文章中,研究者发现,靶向作用混合结构的酶类RNase H对于有效且精确地修复损伤DNA非常关键,研究者表示,该研究或为后期开发新型药物来靶向作用这些酶类提供思路,同时新型药物也能够调节酶类的活性并且阻断或者增强DNA修复途径的效率。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。