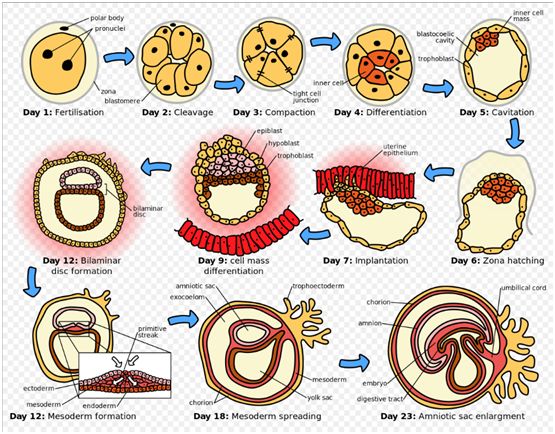
世界上首个人类-猴子胚胎嵌合体诞生于中国
2019年8月31日讯/生物谷BIOON/---2019年7月31日,西班牙《国家报(El País)》报道,一个国际研究小组构建出含有人类和猴子细胞的胚胎。据该报报道,这个有争议的项目是在中国进行的,而不是在项目负责人所在的美国进行的,这样做的目的在于“避免法律问题”,最终旨在培养可移植的人体器官。美国沙克研究所的Juan Carlos Izpisúa Belmonte与来自他自己的实验室的科学
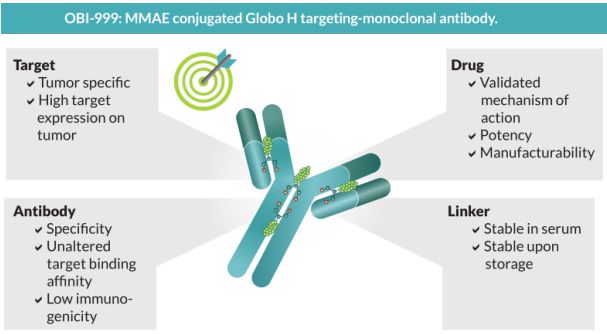
台湾浩鼎抗体药物偶联物OBI-999获美国FDA批准开展首个人体临床研究
2019年09月04日讯 /生物谷BIOON/ --台湾浩鼎生技股份有限公司(OBI Pharma,Inc.,以下简称浩鼎)近日宣布,美国食品和药物管理局(FDA)已批准一份临床试验申请(IND),对其抗体药物偶联物(ADC)OBI-999开展一项I/II期临床研究。该研究是评估OBI-999的首个人体临床研究,计划招募胰腺癌、胃癌、结直肠癌和食管癌等晚期实体瘤患者,评估OBI-999的安全性和初
基因疗法获FDA再生医学先进疗法认定 治疗“泡泡男孩病”
Mustang Bio公司与圣犹达儿童研究医院(St. Jude Children's Research Hospital)共同宣布,其合作研发的治疗X连锁严重联合免疫缺陷病(X-linked severe combined immunodeficiency,X-SCID)的MB-107慢病毒载体基因疗法被美国FDA授予再生医学先进疗法认定(RMAT)。X-SCID又被称为“泡泡男孩病
生基医药与锦斯生物合作 开拓用于先进治疗技术的病毒载体研发生产服务
中国上海,2019年8月13日 - 药明康德全资子公司无锡生基医药科技有限公司(“生基医药”)和上海锦斯生物技术有限公司(“锦斯生物”)近日签署战略合作协议,宣布将共同开拓用于先进治疗技术的病毒载体工业化领域,为客户提供包括溶瘤病毒在内的多种可复制生产型基因治疗病毒载体研发生产服务。此次合作将进一步提升药明康德基因治疗研发生产平台能力,更好地为客户提供覆盖全产业链的基因治疗产品的研发生产服务,推动
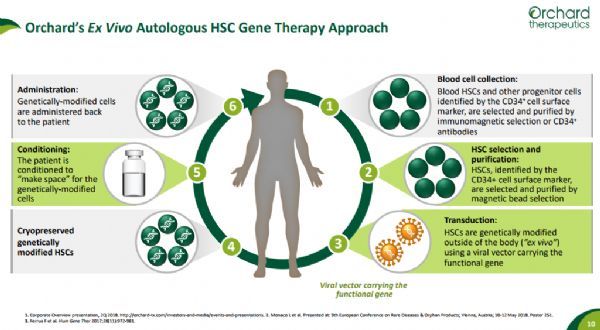
美国FDA授予Orchard公司OTL-103再生医学先进疗法资格(RMAT)
2019年07月30日讯 /生物谷BIOON/ --Orchard Therapeutics是英国的一家基因疗法新锐公司,致力于通过创新的基因疗法改变严重和危及生命的罕见病患者的生活。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其基于自体造血干细胞(HSC)的基因疗法OTL-103治疗Wiskott-Aldrich综合征(Wiskott-Aldrich syndrome,WAS)的再生医
大脑损伤会让我们变一个人么?
2019年7月10日讯 /生物谷BIOON /——我们是谁,是什么让我们成为"我们",一直是历史上许多争论的话题。在个人层面,构成一个人独特本质的要素主要是人格概念,比如善良、温暖、敌意和自私。然而,比这更深层次的是我们如何对周围的世界做出反应,如何在社会上做出反应,我们的道德推理,以及管理情绪和行为的能力。包括柏拉图和笛卡尔在内的哲学家将这些经历归因于非物质实体,而非大脑。他们描述道,"灵魂"是
血友病基因疗法获再生医学先进疗法认定 有望启动注册性试验
日前,Sangamo Therapeutics公司和辉瑞公司公布了双方联合开发的A型血友病基因疗法SB-525在1/2期临床试验中获得的最新结果。试验结果表明,SB-525能够剂量依赖性提高凝血因子VIII的水平,并且具有良好的安全性和耐受性。FDA同时授予SB-525再生医学先进疗法(RMAT)认定。基于这些积极结果,两家公司计划将SB-525推入注册性临床试验,辉瑞公司将接手这一疗
基因疗法获FDA再生医学先进疗法认定 3期试验今年启动
日前,Krystal Biotech公司宣布,其基因疗法KB103在2期临床试验中取得积极结果,治疗营养不良性大疱性表皮松解症(DEB)。该疗法同时获得了FDA授予的再生医学先进疗法(RMAT)认定,RMAT认定旨在加快再生医疗产品(包括基因治疗产品)的开发和批准。DEB是一种罕见的慢性遗传性疾病,患者编码VII型胶原蛋白(COL7)的基因出现突变,皮肤中缺少胶原蛋白,从而
罕见皮肤病基因疗法-KB103治疗大疱性表皮松解症(DEB)获美国FDA再生医学先进疗法资格(RMAT)
2019年06月27日讯 /生物谷BIOON/ --Krystal Biotech是一家专注于开发基因疗法治疗罕见皮肤病的生物技术公司。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其先导候选基因疗法KB103(bercolagene telserpavec)治疗营养不良型大疱性表皮松解症(DEB)的再生医学先进疗法资格(RMAT)。此次RMAT资格的授予,是基于来自GEM-1和GEM-2
华海重磅仿制药抢先进击超 50亿美国市场 首仿将出炉竞争激烈
5月23日,浙江华海药业股份有限公司收到美国食品药品监督管理局(以下简称“美国 FDA”)的通知,利伐沙班片的新药简略申请(ANDA)已获得暂时批准(暂时批准: 指 FDA 已经完成仿制药的所有审评要求,但由于专利权或专卖权未到期而给予的一种批准形式)。标志该产品通过了仿制药的所有审评要求。最终该产品需要在专利权到期并得到 FDA 最终批准后才能获得在美国市场销售的资格。据公告称,华海在利伐沙班片