BCMA CAR-T细胞疗法!强生/南京传奇cilta-cel治疗复发/难治性多发性骨髓瘤:客观缓解率高达98%!
来源:本站原创 2021-06-03 02:38
目前,cilta-cel正在接受美国FDA优先审查、欧盟EMA加速评估。

2021年06月03日讯 /生物谷BIOON/ --强生(JNJ)旗下杨森制药近日公布了BCMA导向CAR-T细胞疗法ciltacabtagene autoleucel(cilta-cel,前称JNJ-4528/LCAR-B38M,LCAR-B38M CAR-T细胞自体回输制剂)的新数据。结果表明,在先前接受过多种疗法(heavily-pretreated,过度预治疗)的复发/难治性多发性骨髓瘤(RRMM)患者中,cilta-cel显示出持续的疗效和持久缓解。
来自1b/2期CARTITUDE-1研究(n=97;NCT03548207)的最新结果显示,中位18个月的长期随访,客观缓解率(ORR)达到了98%,80%的患者达到严格的完全缓解(sCR),强调随着时间的推移缓解加深(sCR从2020年ASH年会上报告的67%增加到80%)。在18个月时,有66%(95%CI:54.9-75.0)的患者存活且疾病无进展。在2021年ASCO年会上将要公布的最新研究结果显示,中位随访18个月,总生存(OS)率为81%(95%CI:71.4-87.6),缓解率在全部预先指定的亚组和不同治疗线数患者中具有可比性。
来自CARTITUDE-1研究的数据,支持了向美国FDA提交的cilta-cel生物制品许可申请(BLA),该BLA最近已被FDA受理进行优先审查。此外,cilta-cel也正在接受欧盟EMA的加速评估。
该研究的首席调查员、莱文癌症研究所浆细胞疾病科主任Saad Z. Usmani表示:“在接受cilta-cel治疗的多发性骨髓瘤患者中观察到的疗效非常显著。在长期随访中,观察到实现无进展生存的可能性提高、缓解持续加深。这些结果表明,cilta-cel将为多发性骨髓瘤患者群体带来一个重要的新治疗选择。”
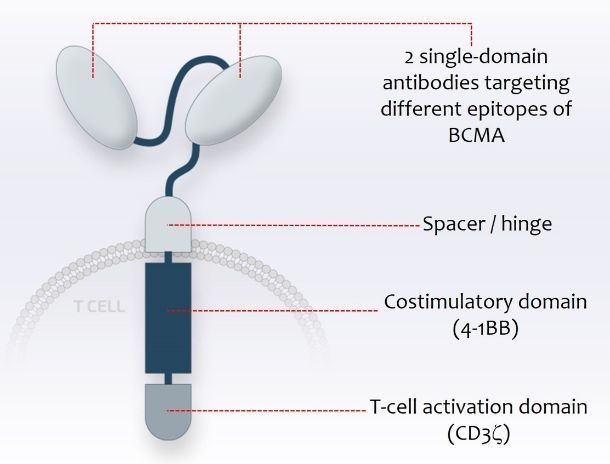
cilta-cel结构特征
cilta-cel是一款在研的B细胞成熟抗原(BCMA)导向的嵌合抗原受体T细胞(CAR-T)疗法,用于治疗复发或难治性多发性骨髓瘤(RRMM)。cilta-cel是一款自体CAR-T疗法,患者自身的T细胞被重新编程以靶向并根除癌症。
cilta-cel是一款独特的、结构上具有差异化的CAR-T细胞疗法,包含一个4-1BB共刺激结构域和两个BCMA靶向单域抗体,具有一种CD8+T细胞优先扩增的特征。CAR-T细胞是一种通过利用患者自身免疫系统的力量来消灭癌细胞的创新方法。BCMA是一种在骨髓瘤细胞上高度表达的蛋白质。
cilta-cel由金斯瑞(Genscript)子公司南京传奇生物科技(Legend Biotech)设计和开发。2017年12月,强生旗下杨森生物科技与南京传奇签订了独家全球许可和合作协议,开发和商业化cilta-cel。在美国,FDA于2019年12月授予cilta-cel突破性药物资格、2019年2月授予孤儿药资格。在欧盟,欧盟委员会(EC)于2020年2月授予cilta-cel孤儿药资格、2019年4月授予优先药物资格(PRIME)。在中国,国家药监局于2020年8月授予cilta-cel突破性药物资格(BTD)。

BCMA为靶点的在研MM免疫疗法(来源文献—PMID:31277554)
——CARTITUDE-1研究的更新结果:
CARTITUDE-1是一项正在进行的开放标签、多中心1b/2期研究,正在评估cilta-cel治疗复发或难治性多发性骨髓瘤(RRMM)成人患者的疗效和安全性。该研究入组了97例患者,这些患者先前接受的疗法中位数为6种(范围:3-18),88%(n=85)为三重难治、42%(n=41)为五重难治、99%(n=96)对最后一种疗法无效。该研究中,成功为所有患者制备cilta-cel。研究的Ib期部分主要目的是确定cilta-cel的安全性和剂量。II期部分将评估cilta-cel的疗效,主要终点是总缓解率(ORR)。
最新数据显示:缓解随时间推移加深,中位随访18个月,根据独立审查委员会(IRC)评估确定,98%的患者实现缓解(ORR=98%),包括:80%的患者实现严格的完全缓解(sCR=80%)、14%的患者实现非常好的部分缓解(VGPR=14%)、3%的患者实现部分缓解(PR=3%)。从治疗至达到首次缓解的中位时间为1个月(范围:0.9-10.7个月),缓解随时间推移加深。在61例微小残留病(MRD)可评估患者中,92%的患者在cilta-cel输注后中位时间1个月时达到了MRD阴性状态(10E-5)。中位随访18个月时,总生存率为81%(95%CI:71.4-87.6)。该研究中,cilta-cel具有一致的安全性,并且在较长时间的随访中没有观察到新的安全性信号,≥3级细胞因子综合征(CRS)发生率为5%,≥3级神经毒性发生率为10%。
——CARTITUDE-2研究的首批结果:
CARTITUDE-2(NCT04133636)是一项正在进行的多队列2期研究,正在评估cilta-cel治疗多发性骨髓瘤的安全性和有效性。队列A入组了先前接受过1-3线治疗(包括PI和IMiD)后出现进展的多发性骨髓瘤的患者,这些患者均为来那度胺治疗无效、并且之前没有接受过BCMA靶向药物。主要终点是微小残留病(MRD)10E-5阴性率。
队列A的结果将首次在ASCO年会和EHA年会上公布。该队列的结果显示,中位随访5.8个月,观察到早期和深刻缓解,ORR为95%,其中45%的患者达到sCR、30%的患者达到CR、10%的患者达到VGPR、10%的患者达到PR。该研究中,cilta-cel的总体安全状况,包括CRS的发生率和最常见的血液学不良事件,与CARTITUDE临床开发项目的观察结果一致。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


