中国2型糖尿病新药!诺和诺德诺和泰®(司美格鲁肽注射液)获批:兼顾降糖、降体重、降心血管风险三大功效!
来源:本站原创 2021-04-29 17:48
诺和泰®是一款新型长效胰高糖素样肽-1(GLP-1)类似物,半衰期长达7天,适合每周注射一次且血药浓度平稳。

2021年04月29日讯 /生物谷BIOON/ --诺和诺德(Novo Nordisk)近日宣布,中国国家药品监督管理局(NMPA)已批准诺和泰®(semaglutide,司美格鲁肽注射液,曾经暂用名:索马鲁肽,英文商品名:Ozempic),用于治疗2型糖尿病(T2D)患者,改善血糖控制。诺和泰®是一款新型长效胰高糖素样肽-1(GLP-1)类似物,半衰期长达7天,适合每周注射一次且血药浓度平稳。
在中国,糖尿病患病人数超过1.298亿,其中仅有15.8%血糖控制达标。糖尿病易引发大血管病变、微血管病变及其他并发症,严重影响患者生活质量,增加患者疾病负担。其中,心血管疾病是2型糖尿病患者的主要致死原因。在中国,每3位糖尿病患者中,就有1位患有心血管疾病。血糖控制不达标,血压、血脂、体重等心血管代谢指标管理不佳,是导致中国糖尿病患者并发症高发的主要原因。因此,糖尿病治疗需聚焦患者全面获益,兼顾血糖控制与心血管结局,对多重危险因素进行综合管理。
作为一周一次给药的重磅GLP-1产品,诺和泰®以突破性技术将半衰期延长至7天,实现一周一次给药,强效控糖、精准达标,并以全面心血管代谢获益,为中国2型糖尿病患者提供更加有效、简便、安全的治疗选择。诺和泰®的获批将进一步推动中国糖尿病治疗方式和治疗理念的变革,助力综合疾病管理,改善长期治疗结局,帮助患者回归泰然生活。
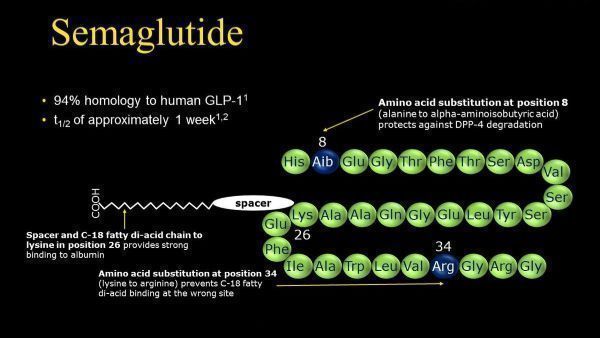
semaglutide分子结构特征
全球多中心大型临床研究SUSTAIN系列研究共纳入11000余名患者,其中包括605例中国患者,证实了司美格鲁肽优异的降糖疗效、安全性和心血管代谢获益。SUSTAIN China研究结果显示,在中国人群中,司美格鲁肽可显著降低糖化血红蛋白(HbA1c),最高降幅达1.8%,HbA1c达标率(<7.0%)高达86.1%,且低血糖发生率极低。进一步分析显示,司美格鲁肽能够显著改善2型糖尿病患者β细胞应答至健康人水平,实现“按需”降低HbA1c水平,无论患者是高基线HbA1c或者接近于7%,司美格鲁肽均可使平均HbA1c水平降至7%以内。
此外,司美格鲁肽还能够改善多项心血管代谢指标,更好地综合管理包括体重、血压和血脂等在内的多种心血管危险因素。SUSTAIN 6研究结果显示,在标准治疗基础上,相比安慰剂,司美格鲁肽显著降低主要心血管不良事件(MACE)发生风险达26%,显著降低非致死性卒中风险达39%。
兼具强效、长效和多效的诺和泰®,不仅将有效助力患者血糖平稳达标,并以全面心血管代谢获益帮助患者实现长久保护,大幅提高患者用药依从性,改善患者的生存质量,助力患者回归泰然生活。

2款已上市semaglutide产品
semaglutide(司美格鲁肽)是一款人胰高血糖素样肽-1(GLP-1)类似物,以葡萄糖浓度依赖性机制促胰岛素分泌并抑制胰高血糖素分泌,可使2型糖尿病患者血糖水平大幅改善,并且低血糖风险较低。此外,semaglutide还能够通过降低食欲和减少食物摄入量,诱导减肥。除此之外,semaglutide还能够显著降低2型糖尿病患者重大心血管事件(MACE)风险。
诺和诺德已针对semaglutide开发了注射制剂(Ozempic,诺和泰®)和口服制剂(Rybelsus):
——Ozempic(semaglutide,诺和泰®,注射制剂):是每周一次的皮下注射制剂(0.5mg或1mg),适用于:(1)作为饮食调整和运动的辅助手段,以改善2型糖尿病成人患者的血糖控制;(2)用于存在心血管疾病(CVD)的2型糖尿病成人患者,降低发生主要不良心血管事件(MACE,包括心血管死亡、非致死性心脏病发作、非致死性卒中)的风险。
Ozempic于2017年12月首次获得美国FDA批准,目前已在全球多个国家和地区上市销售。该药第二个适应症于2020年1月获得美国FDA批准,来自心血管结局试验(CVOT)SUSTAIN 6的数据显示:在心血管(CV)高风险的2型糖尿病患者中,当联合标准护理时,与安慰剂相比,Ozempic将MACE复合终点风险在统计学上显著降低了26%。
——Rybelsus(semaglutide,口服片剂):是一种每日一次的口服制剂,其中含有促进吸收的赋形剂SNAC,该药适用于:作为饮食调整和运动和辅助药物,改善2型糖尿病成人患者的血糖控制。Rybelsus是全球第一款也是唯一一款口服版GLP-1受体激动剂,每日服药一次,治疗剂量有2种:7mg和14mg。
在美国,Rybelsus的标签于2020年1月更新,纳入了证明CV安全性的PIONEER 6 CVOT的额外信息,该试验在CV高风险的2型糖尿病患者中开展,数据显示,当联合标准护理时,与安慰剂相比,Rybelsus达到了复合MACE终点非劣效性的主要终点,证明了CV安全性。研究中,经历了至少一次MACE的患者比例,Rybelsus组为3.8%,安慰剂组为4.8%。
除了上述2款产品,诺和诺德也正在开发Ozempic高剂量(2.0mg)用于2型糖尿病的强化治疗。该公司已于2020年12月、2021年1月在欧盟和美国提交了一份标签扩展申请,在Ozempic现有上市许可中引入2.0mg新剂量。来自SUSTAIN FORTE试验的结果显示,在需要强化治疗的2型糖尿病患者中,2.0mg剂量在降低血糖方面在统计学上显著优于1.0mg剂量,并且具有相似的安全性和耐受性。

肥胖症
此外,诺和诺德也正在开发每周一次semaglutide 2.4mg皮下注射制剂,作为成人肥胖症的治疗方法。semaglutide可通过减少饥饿感、增加饱腹感,帮助人们吃得更少、减少卡路里的摄入,从而诱导减肥。
2020年12月,诺和诺德向美国FDA提交了semaglutide 2.4mg皮下注射制剂的新药申请(NDA),该药是一种每周一次的胰高血糖素样肽-1(GLP-1)类似物,用于长期体重管理。值得一提的是,诺和诺德还递交了一张优先审查凭证(PRV)来加速NDA审查,该PRV可将NDA审查周期从标准的10个月缩短至6个月。
semaglutide 2.4mg皮下注射制剂申请的适应症为:作为低热量饮食和加强运动的辅助手段,用于治疗肥胖(BMI≥30kg/m2)或超重(BMI≥27kg/m2)并伴有至少一种体重相关合并症的成人患者。
今年4月,诺和诺德宣布将semaglutide(50mg,口服)推进至3a期临床开发,用于治疗肥胖症。

阿尔茨海默氏症-AD(图片来源于:tecake.in)
值得一提的是,2020年12月,诺和诺德还宣布,决定将semaglutide(14mg,口服)推进至3a期临床开发,治疗阿尔茨海默氏症(AD)。该决定是对临床前模型的GLP-1数据进行评估、真实世界的证据研究、大型心血管结果试验的事后分析以及与监管机构的讨论之后做出的。
临床前动物模型研究强调了与AD相关的GLP-1的关键作用,包括改善记忆功能和减少磷酸τ积累。semaglutide已被明确证明可以减少神经炎症,而神经炎症可能会影响认知和功能。
此外,来自丹麦2个全国性注册中心美国Truven索赔数据库和美国FDA FAERS数据库的真实证据支持GLP-1治疗后痴呆症风险降低之间的潜在联系。
最后,在对诺和诺德开展的3项大型心血管结局试验(LEADER,SUSTAIN 6和PIONEER 6)数据的事后分析中,共有47人被确定患有痴呆症,其中32人服用安慰剂,15人服用GLP-1(liraglutide[利拉鲁肽]或semaglutide)。数据有利于GLP-1,显示痴呆的发生率在统计学上显著降低了53%。(生物谷Bioon.com)
原文出处:诺和诺德、生物谷
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


