B7-H3靶点新药!omburtamab治疗神经母细胞瘤在欧盟申请上市:1年生存率87%,赛生药业引进中国!
来源:本站原创 2021-04-29 01:31
omburtamab有潜力成为第一个针对中枢神经系统(CNS)/软脑膜转移的神经母细胞瘤儿童患者的靶向疗法。
2021年04月28日讯 /生物谷BIOON/ --Y-mAbs Therapeutics是一家商业化阶段的生物制药公司,专注于开发和商业化基于抗体的创新疗法,用于癌症的治疗。近日,该公司宣布,已向欧洲药品管理局(EMA)提交了omburtamab的营销授权申请(MAA),哟用于治疗中枢神经系统(CNS)/软脑膜(LM)转移的神经母细胞瘤儿童患者。
omburtamab有潜力成为第一个针对中枢神经系统(CNS)/软脑膜转移的神经母细胞瘤儿童患者的靶向疗法。omburtamab是一种靶向B7-H3的单克隆抗体,在脑室内中枢神经系统(CNS)给药前已被放射性标记。B7-H3是一种免疫检查点分子,广泛表达于多种类型癌症的肿瘤细胞中。
目前,Y-mAbs已有一款商业化产品Danyelza(naxitamab-gqgk)40mg/10ml,该药于2020年11月获得美国FDA加速批准,联合粒细胞-巨噬细胞集落刺激因子(GM-CSF),用于治疗复发/难治性高危神经母细胞瘤患者,具体为:年龄≥1岁、对既往治疗表现出部分缓解、轻微缓解或疾病稳定、骨骼或骨髓中存在复发或难治性高危神经母细胞瘤的儿科和成人患者。
Danyelza和omburtamab由美国纪念斯隆·凯特林癌症中心(MSK)的研究人员开发出来,并由MSK独家授权给Y-mAbs。由于这一许可协议,MSK在Danyelza和omburtamab产品和Y-mAbs中拥有机构财务利益。
值得一提的是,2020年12月,赛生药业(SciClone)与Y-mAbs签订了一项许可协议,获得了在大中华区独家合作开发和商业化Danyelza和omburtamab的权利,将2款产品用于治疗中国的复发/难治性高危神经母细胞瘤患者和有中枢神经系统(CNS)/软脑膜转移的神经母细胞瘤儿童患者。
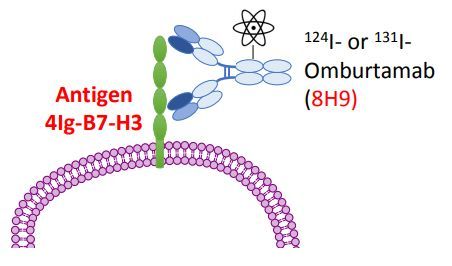
omburtamab分子结构及靶向结合B7-H3
Y-mAbs创始人、董事长兼总裁Thomas Gad表示:“我们相信,omburtamab有望成为EMA批准的首个针对CNS/软脑膜转移的神经母细胞瘤儿童患者的靶向疗法。Y-mAbs正在继续推进omburtamab项目,以便尽可能地为全球的儿童患者提供这种创新疗法。目前,针对这类患者还没有标准的治疗方法,omburtamab将解决该领域存在的重要的未满足的医疗需求。”
此外,Y-mAbs最近与美国食品和药物管理局(FDA)就omburtamab结束了一次B型会议,并收到了FDA关于额外数据的请求,该请求涉及Y-mAbs公司确定的历史对照组中的粒度数据(granularity data)。为了就统计分析计划(SAP)达成一致,该公司正在收集这些额外的粒度数据,并预计在4月底之前将其提交给FDA。下一次B型会议定于2021年6月1日举行,根据对额外数据的审查来讨论SAP。该公司将继续与FDA保持密切对话,并保持公司目标,即在2021年第二季度末或第三季度重新提交omburtamab的生物制品许可申请(BLA)。
Y-mAbs首席执行官Claus Moller博士表示:“我们很高兴在欧盟提交omburtamab的MAA,并对我们正在取得的进展感到非常高兴。我们相信,omburtamab有潜力解决CNS/软脑膜转移的神经母细胞瘤儿童患者群体中的显著未满足医疗需求。我们还将继续与FDA密切合作,重新提交omburtamab BLA。”
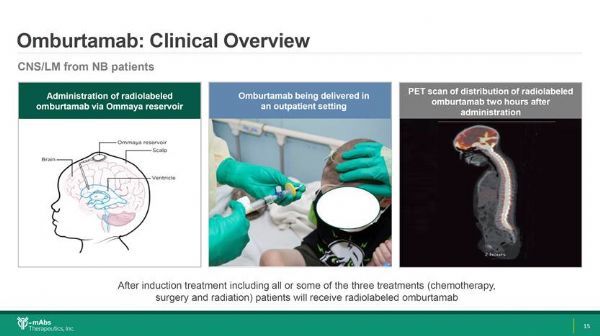
omburtamab给药方式(点击图片,查看大图)
B7-H3(B7同系物3)是一种免疫检查点分子,这是一种跨膜蛋白,归属于B7家族,在肿瘤生长和免疫应答中发挥作用。B7-H3常常在各种类型的癌症(包括肺癌、头颈癌、食管癌、前列腺癌、子宫内膜癌和乳腺癌等)中过度表达,并且在许多肿瘤类型中与疾病进展和不良预后相关。目前,还没有B7-H3靶向疗法被批准用于治疗任何癌症。
omburtamab是一种放射性碘标记的鼠源抗B7-H3单克隆抗体(131I-8H9),靶向人类实体肿瘤(包括胚胎肿瘤、癌、肉瘤和脑肿瘤)中表达肿瘤抗原B7-H3的细胞,并结合到B7-H3分子上的生物功能的关键区域--FG环依赖型构象。目前,omburtamab正处于临床开发,该药是治疗中枢神经系统(CNS)/软脑膜转移的神经母细胞瘤的一种很有前途的疗法。当神经母细胞瘤转移到软脑膜或CNS时,可使用Ommaya导管将放射性标记的omburtamab直接注射到CNS中。与系统(全身)给药相比,将治疗性液体辐射直接递送至CNS可使药物直达肿瘤。
之前,FDA已授予omburtamab突破性药物资格(BTD)。2020年10月公布的关键101多中心研究结果显示:在入组并接受治疗的17例患者中,中位随访26周,12个月总体生存(OS)率为78%。而历史对照组中,一年OS率大约为30%。
神经母细胞瘤是一种极具侵袭性的肿瘤,是婴幼儿最常见的肿瘤之一,尽管近年来强化多模式治疗已提高了生存率,但幸存者有很高的复发风险。
Y-mAbs公司已上市神经母细胞瘤药物Danyelza(naxitamab-gqgk)是一种靶向神经节苷脂GD2的人源化单克隆抗体,之前已获美国FDA授予突破性药物资格(BTD)。GD2抗原在各种神经外胚层来源的肿瘤和肉瘤中呈现高表达,包括神经母细胞瘤、黑色素瘤和骨肉瘤等肿瘤。Danyelza通过与肿瘤表面的GD2抗原结合,能够触发抗体介导的细胞毒性反应并激活免疫系统中的补体系统,从而达到杀伤肿瘤的效果。
Danyelza通过靶向GD2(一种神经母细胞瘤细胞表面的肿瘤抗原)起效。Danyelza因其良好的毒理学特征、较短的输注时间及门诊可操作而区别于其他GD2靶向疗法。除了神经母细胞瘤之外,Danyelza也正被开发用于治疗骨肉瘤以及其他GD2阳性肿瘤。
来自2项关键II期研究(201和12-230)的数据显示:在原发性难治性高危神经母细胞瘤儿童亚组中,Danyelza与GM-CSF联合治疗的客观缓解率(ORR)为78%、有50%的患者无进展生存期(PFS)达到24个月。在另一个对挽救性疗法有抵抗力的复发性神经母细胞瘤儿童亚组中,Danyelza与GM-CSF联合治疗的ORR为37%,编码该治疗方案在这类难治性患者中具有显著临床益处。(生物谷Bioon.com)
原文出处:Y-mAbs Submits Omburtamab Marketing Authorization application to the European Medicines Agency
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->