多发性硬化症新药!强生S1P1调节剂Ponvory(ponesimod)获美国FDA批准:疗效击败赛诺菲Aubagio!
来源:本站原创 2021-03-20 00:28
在中国,Aubagio(奥巴捷)已于2018年7月上市,是国内首个疾病修正口服疗法。

2021年03月19日/生物谷BIOON/--强生(JNJ)旗下杨森制药近日宣布,美国食品和药物管理局(FDA)已批准Ponvory(ponesimod),该药是一种每日一次、口服、选择性鞘氨醇-1-磷酸受体1(S1P1)调节剂,用于治疗复发型多发性硬化症(MS)成人患者,包括临床孤立综合征(CIS)、复发-缓解型多发性硬化症(RRMS)、活动性继发进展型多发性硬化症(SPMS)。用药方面,对于大多数患者,Ponvory不需要进行基因检测或首个剂量心脏监护。但由于启动Ponvory治疗会导致心率下降,建议对有特定心脏病史的患者进行首个剂量监测。
值得一提的是,Ponvory是FDA批准的第一个也是唯一一个针对已上市口服疗法进行对照研究的口服疾病修正疗法。与目前市面上的口服MS药物Aubagio(中文商品名:奥巴捷,通用名:teriflunomide,特立氟胺)相比,Ponvory在降低年复发率方面显示出优越疗效(年复发率减少近三分之一),而且已有超过10年的累积临床研究数据证明了其有效性和安全性。
Aubagio是赛诺菲的一款口服药物,早在2012年9月获得美国FDA批准用于治疗复发型多发性硬化症(RMS),该药是一款行业领先的口服MS药物,已在全球超过70个国家和地区上市。在中国,Aubagio(奥巴捷)于2018年7月获批上市,是国内批准治疗多发性硬化症的首个口服疾病修正治疗药物。
在美国,有近100万多发性硬化症(MS)成人患者,约85%在最初诊断时确诊为复发型MS。尽管近年来已取得了进展,但该领域仍然存在着未满足的医疗需求。与市面上的疗法相比,Ponvory显示出卓越疗效,特别是在减少新的炎症病变和残疾积累方面。Ponvory的批准上市,将为患者提供一个重要的新口服药物。
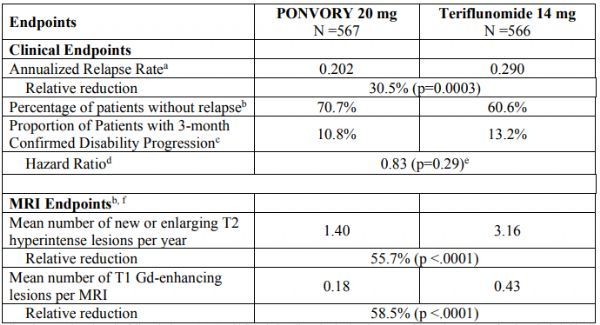
此次批准,基于头对头III期OPTIMUM研究(NCT02425644)的结果。该研究在RMS成人患者中开展,比较了ponesimod与Aubagio的疗效、安全性和耐受性。
值得一提的是,OPTIMUM研究是比较2种口服药物治疗RMS的首个大型对照头对头研究。数据显示,在研究的主要终点和多个次要终点方面,ponesimod(20mg,每日一次)与Aubagio(14mg,每日一次)相比均显示出优越性。
具体数据为:(1)主要终点方面,从基线至治疗第108周,与Aubagio治疗组相比,ponesimod治疗组年复发率(ARR)在统计学上显著降低30.5%(ARR:0.202 vs 0.290,p=0.0003);在研究期间,ponesimod治疗组有71%的患者没有确认的复发、Aubagio治疗组为61%。(2)ponesimod在减少新的钆增强(GdE)T1病变数目和新的或扩大的T2病变数目方面也优于Aubagio,分别减少59%和56%。GdE T1病变和T2病变分别通过磁共振成像(MRI)技术识别,并被认为是MS病理学的经典测量复发,可分别提供对疾病活动和疾病负担的见解。(3)该研究中观察到的ponesimod的安全性与先前研究以及已知的其他S1P受体调节剂的安全性一致,ponesimod治疗组最常见的治疗期间出现的不良事件(TEAE)为丙氨酸氨基转移酶(ALT)升高、鼻咽炎、头痛、上呼吸道感染。
多发性硬化症(MS)是一种慢性中枢神经系统自身免疫性炎症性疾病,影响全球230万人,受影响女性多于男性。该病特征是脱髓鞘和轴突丢失,导致神经功能受损和严重致残。MS的主要亚型是复发型多发性硬化症(RMS),占MS患者的85%,包括临床孤立综合征(CIS)、复发-缓解型多发性硬化症(RRMS)和活动性继发性进行性多发性硬化症(SPMS)。复发被定义为新的、恶化的或复发的神经症状,持续24小时以上,无发热或感染。复发可能在数天或数周内得到完全缓解,或导致持续的残缺和残疾的累积。
Ponvory的活性药物成分为ponesimod,这是一种新型、口服、选择性鞘氨醇-1-磷酸受体1(S1P1)调节剂,可功能性抑制S1P蛋白的活性,并将淋巴细胞束缚在淋巴结内,从而减少可穿过血脑屏障的循环淋巴细胞的数量。在多发性硬化症(MS)患者中,淋巴细胞进入大脑损害髓鞘(myelin)。髓鞘是一种保护性鞘,能隔离神经细胞。髓鞘损伤可减缓或终止神经传导、产生多发性硬化症的神经症状和体征。
目前,鞘氨醇-1-磷酸(S1P)受体已成为MS领域新药研发的一个重要靶点。2019年3月,诺华口服S1P受体调节剂Mayzent(siponimod)获美国FDA批准,用于RMS成人患者的治疗。2020年3月,来自新基(已被百时美施贵宝收购)的口服S1P受体调节剂Zeposia(ozanimod)获得美国FDA批准,治疗RMS成人患者。
Ponvory上市后,将与Mayzent和Zeposia展开直接竞争。此外,Ponvory还面临着其他多款口服药物的竞争,例如诺华的Gilenya、赛诺菲的Aubagio、渤健的Tecfidera和Vumerity、默克的Mavenclad,以及罗氏的每年仅需输注2次的抗体药物Ocrevus。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->