胶质母细胞瘤新药!吉利德210亿美元收购的下一代抗体偶联药物Trodelvy获美国FDA孤儿药资格!
来源:本站原创 2020-10-14 16:35
Trodelvy是第一个被批准的靶向Trop-2的抗体偶联药物(ADC),已被批准治疗三阴性乳腺癌。

2020年10月14日讯 /生物谷BIOON/ --Immunomedics是下一代抗体偶联药物(ADC)技术的先驱,致力于帮助癌症患者改变生活。其专有ADC平台的核心是使用一种新型的链接子,这种链接子不需要酶来释放有效荷载,可在肿瘤细胞内和肿瘤微环境中递送活性药物,从而产生近旁效应(bystander effect)。今年9月中旬,吉利德科学(Gilead Sciences)与Immunomedics达成一项最终协议,将以210亿美元收购Immunomedics,该笔交易已获得双方董事会一致批准,预计2020年第四季度完成。
此次交易将为吉利德带来一款首创的Trop-2靶向ADC产品Trodelvy(sacituzumab govitecan-hziy),该药是一款新型、同类首个ADC产品,由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。Trop-2是一种在许多实体瘤中表达的细胞表面蛋白。Trodelvy与Trop-2靶向结合并递送抗癌制剂SN-38来杀死癌细胞。
Trodelvy是Immunomedics公司的首个商业化ADC产品,于今年4月获得美国FDA加速批准,用于先前已接受过至少2种疗法治疗转移性疾病的转移性三阴性乳腺癌(mTNBC)成人患者。值得一提的是,Trodelvy是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个以Trop-2为靶点的ADC药物。
胶质瘤(图片来源:hmcisrael.com).jpg
近日,Immunomedics公司宣布,美国FDA已授予Trodelvy孤儿药资格(ODD),用于治疗胶质母细胞瘤(glioblastoma,GBM)成人和儿童患者。孤儿药(Orphan Drug)是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物上市后针对所批准适应症为期7年的市场独占期。
胶质母细胞瘤(GBM)是一种侵袭性的癌症,存在显著的未满足医疗需求。据美国国家癌症研究所(NCI)估计,在美国,2020年将有23890名人被诊断出患有脑和其他神经系统癌症,将有大约18020人死于这种疾病。在众多的脑瘤类型中,GBM是最具侵袭性的,临床试验报告显示,从疾病确诊后,中位无进展生存期(PFS)和中位总生存期(OS)分别为6.2-7.5个月和14.6-16.7个月。对于复发性GBM患者,化疗方案的总有效率仅为4-9%,6个月PFS率为10-19%,中位OS为5-10个月。
Immunomedics首席医学官Loretta M.Itri博士表示:“随着我们努力扩大Trodelvy的临床应用,此次孤儿药资格认证是Immunomedics的一个重要里程碑。正如在最近的ESMO大会上报道的那样,Trodelvy治疗脑癌的一项早期研究中显示了令人鼓舞的活性,包括乳腺癌脑转移患者队列和复发性胶质母细胞瘤患者队列中观察到的部分缓解。我们期待着继续评估Trodelvy改善这些服务不足患者群体预后的潜力。”
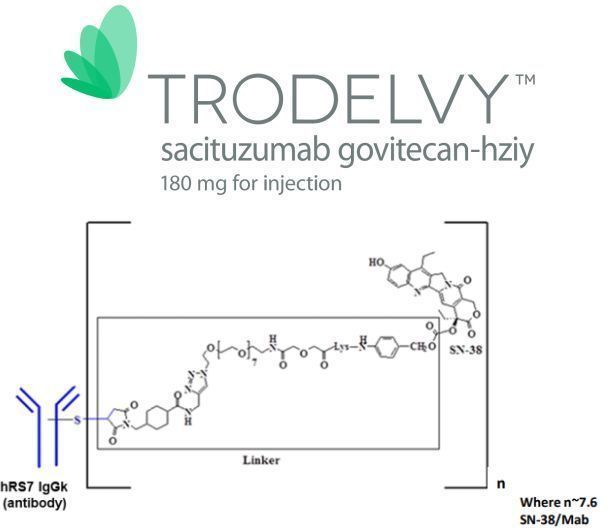
Trop-2是一种在多种实体瘤中表达的细胞表面糖蛋白。在三阴性乳腺癌(TNBC)中,Trop-2在90%以上的TNBC细胞中表达。Immunomedics针对Trodelvy有一个广泛的开发计划,包括三阴性乳腺癌(TNBC)、转移性尿路上皮癌(mUC)、激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)转移性乳腺癌、转移性非小细胞肺癌(NSCLC)的多项正在进行的研究,包括单药治疗以及与其他药物联合治疗。
Trodelvy有潜力改变转移性三阴性乳腺癌(mTNBC)的标准护理。在支持该药加速批准的单臂多中心II期研究中,Trodelvy治疗mTNBC的总缓解率(ORR)为33.3%、中位缓解持续时间(DOR)为7.7个月。今年7月,Trodelvy治疗mTNBC的验证性III期ASCENT研究(NCT02574455)达到主要终点和关键次要终点。数据显示,在先前接受过治疗的晚期mTNBC患者中,与化疗相比,Trodelvy;(1)显著延长了无进展生存期(中位PFS:5.6个月 vs 1.7个月)、将疾病进展风险显著降低59%(HR=0.41,95%CI:0.32-0.52,p<0.0001));(2)显著延长了总生存期(中位OS:12.1个月 vs 6.7个月)、将死亡风险降低了52%(HR=0.48,p<0.0001);(3)显著提高了总缓解率(ORR:35% vs 5%)和临床受益率(CBR:45% vs 9%)。
这些数据证实了先前II期临床中的结果,表明Trodelvy有潜力改变mTNBC的标准护理,并将为mTNBC患者的科学和临床创新树立一个新的基准,同时为临床实践常用药提供了一个新的替代品。
此前,有分析师指出,根据II期数据,与标准护理相比,Trodelvy代表着一个显著进步,该药上市后的销售峰值预计将达到10亿美元以上。而此次验证性III期临床的成功,无疑将进一步提升Trodelvy的商业潜力。Immunomedics公司计划在今年晚些时候向美国FDA提交一份补充生物制品许可申请(sBLA),将Trodelvy由加速批准转为完全批准。
TNBC治疗方面,值得一提的是,2019年3月罗氏PD-L1肿瘤免疫疗法Tecentriq(泰圣奇,通用名:atezolizumab,阿替利珠单抗)获美国FDA批准,联合化疗(Abraxane)一线治疗PD-L1阳性局部晚期或转移性三阴性乳腺癌(TNBC)患者。此次批准,使Tecentriq+Abraxane组合成为治疗TNBC的首个癌症免疫治疗方案。(生物谷Bioon.com)
原文出处:Immunomedics Announces FDA Orphan Drug Designation of Trodelvy™ for Adult and Pediatric Glioblastoma
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


