爆料!吉利德科学或豪掷200亿美元收购下一代抗体药物偶联物(ADC)开发商Immunomedics!
来源:本站原创 2020-09-13 19:23
今年以来,吉利德科学已达成数笔交易,投资肿瘤学领域。

2020年09月13日讯 /生物谷BIOON/ --路透社近日报道称,据《华尔街日报》周六报道,吉利德科学(Gilead Sciences)即将达成一项交易,以200亿美元收购Immunomedics公司。这笔交易将进一步扩大吉利德的癌症治疗产品组合。
《华尔街日报》援引知情人士消息称,吉利德与Immunomedics之间的讨论最初是围绕合作关系展开的,之后才转向了全面的收购谈判。目前,吉利德和Immunomedics尚未对路透社的置评请求做出回应。
今年以来,Immunomedics股价几乎翻了一番,市值接近100亿美元。而吉利德方面,在今年以来已经达成了数笔交易来扩展肿瘤学管线:(1)今年7月,对Tizona Therapeutics进行了3亿美元的股权投资;(2)今年6月,以2.75亿美元买进Pionyr Immunotherapeutics公司49.9%的股份,并拥有收购剩余50.1%股份的独家选择权;(3)今年5月,与Acrus Biosciences达成了总额20亿美元、长达10年的合作,开发针对PD-1、CD73、TIGIT等热门靶点在内的一系列免疫肿瘤学资产;(4)今年4月,以49亿美元收购主打CD47抗体的免疫肿瘤学公司Forty Seven,该公司的核心资产是靶向“别吃我”信号分子CD47的单抗药物magrolimab,在去年的ASH年会上一鸣惊人。

Immunomedics是下一代抗体药物偶联物(ADC)技术的先驱,致力于帮助癌症患者改变生活。其专有ADC平台的核心是使用一种新型的链接子,这种链接子不需要酶来释放有效荷载,可在肿瘤细胞内和肿瘤微环境中递送活性药物,从而产生近旁效应(bystander effect)。
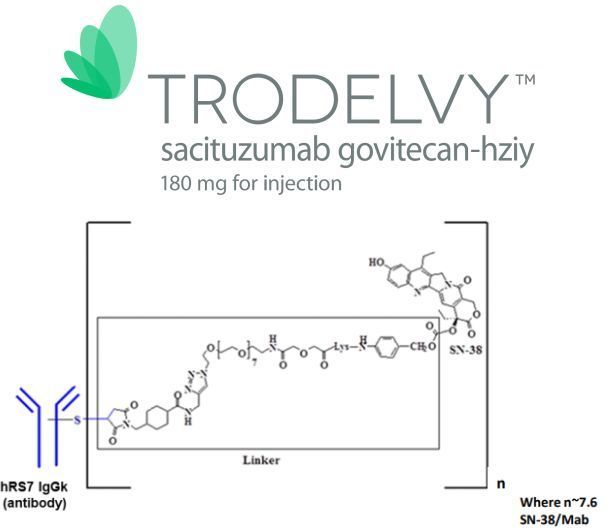
今年4月,该公司首个商业化ADC产品Trodelvy(sacituzumab govitecan-hziy)获得美国FDA加速批准,用于先前已接受过至少2种疗法治疗转移性疾病的转移性三阴性乳腺癌(mTNBC)成人患者。值得一提的是,Trodelvy是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个靶向Trop-2的ADC药物。该批准基于单臂多中心II期研究的总缓解率(ORR=33.3%)和缓解持续时间(中位DOR=7.7个月)数据。
Trodelvy的活性药物成分为sacituzumab govitecan,这是一种新型、首创的抗体药物偶联物(ADC)药物,由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。Trop-2是一种在许多实体瘤中表达的细胞表面糖蛋白,特别是,存在于90%以上的TNBC中。Trodelvy与Trop-2靶向结合并递送抗癌药SN-38来杀死癌细胞。
目前,Immunomedics公司针对Trodelvy有一个广泛的开发计划,包括正在进行的多项研究,将Trodelvy作为单药治疗或与其他药物联合用药,治疗TNBC、转移性尿路上皮癌、激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)转移性乳腺癌、转移性非小细胞肺癌(NSCLC)等。
今年7月,Immunomedics公司宣布,验证性III期ASCENT研究(NCT02574455)达到了主要终点和关键次要终点。该研究是在FDA特别方案评估(SPA)下设计的,目的是验证Trodelvy在支持其批准的II期研究中所显示出的有希望的疗效和安全性。ASCENT是一项国际性、开放标签III期研究,共入组了500多例mTNBC患者,这些患者脑转移呈阴性、先前接受过至少2种疗法治疗转移性疾病。研究中,患者被随机分为2组,一组接受Trodelvy,另一组接受医生选择的化疗。主要终点是无进展生存期(PFS),次要终点包括总生存期(OS)、ORR、DOR、发生缓解的时间、安全性和耐受性。
数据显示,研究达到了主要终点:Trodelvy组与化疗组相比在PFS方面有统计学意义的显著改善(中位PFS:5.6个月[95%CI:4.3-6.3] vs 1.7个月[95%CI:1.5-2.6])、疾病进展风险显著降低59%(HR=0.41,95%CI:0.32-0.52,p<0.0001)。此外研究也达到了关键次要终点(OS和ORR)。该研究中,Trodelvy的安全性与美国FDA批准的药物标签信息一致。最常见的3级或4级不良事件是中性粒细胞减少症和腹泻,没有观察到新的安全信号。研究的全部结果将在即将召开的医学会议上公布。
基于上述数据,Immunomedics公司计划在今年晚些时候提交一份补充生物制品许可申请(sBLA),将Trodelvy由加速批准转为完全批准。来自验证性III期ASCENT研究的数据证实了先前II期临床中的结果,表明Trodelvy有潜力改变mTNBC的标准护理。基于这些数据,Trodelvy将为mTNBC患者的科学和临床创新树立一个新的基准,同时为临床实践常用药提供了一个新的替代品。重要的是,该研究也验证了Trodelvy可管理的安全性,使其成为与其他疗法(包括免疫疗法)联合用药的一个很好的配伍药物。
乳腺癌是女性中最常见的癌症类型,全球每年确诊超过200万例。三阴乳腺癌(TNBC)约占所有乳腺癌比例的15%,与其他类型乳腺癌相比,TNBC在50岁以下女性中更为常见。TNBC特指雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(HER-2)三者均为阴性表达的乳腺癌,进展迅速,预后极差,5年生存率不到15%。TNBC对激素疗法和HER2靶向疗法(如罗氏赫赛汀Herceptin)均无效,临床治疗选择非常有限,主要依靠化疗。
Trodelvy通过加速审批程序获得批准,先前已被美国FDA授予突破性药物资格(BTD)和优先审查。Trodelvy有潜力成为mTNBC治疗的一个标准护理药物。此前,有分析师指出,根据II期数据,与标准护理相比,Trodelvy代表着一个显著进步,该药上市后的销售峰值预计将达到10亿美元以上。而此次验证性III期临床的成功,无疑将进一步提升Trodelvy的商业潜力。
TNBC治疗方面,2019年3月,罗氏PD-L1肿瘤免疫疗法Tecentriq(泰圣奇,通用名:atezolizumab,阿替利珠单抗)获美国FDA加速批准,联合化疗(Abraxane,注射用紫杉醇 [白蛋白结合型])一线治疗PD-L1阳性局部晚期或转移性TNBC患者。此次批准,使Tecentriq+Abraxane组合成为治疗TNBC的首个癌症免疫治疗方案。该批准基于III期IMpassion130研究的数据:与安慰剂+Abraxane相比,Tecentriq+Abraxane在PD-L1阳性患者中将疾病进展或死亡风险显著降低40%(中位PFS:7.4个月 vs 4.8个月,HR=0.60,95%CI:0.48-0.77,p<0.0001)。
然而,今年8月,Tecentriq+紫杉醇一线治疗转移性TNBC的III期IMpassion131研究失败:在PD-L1阳性患者群体中,与安慰剂+紫杉醇相比,Tecentriq+紫杉醇方案在主要终点无进展生存期(PFS)方面没有达到统计学意义。次要终点总生存期(OS)的数据呈负趋势,在分析时数据还不成熟。
就在最近,美国FDA发布一则警告信息,提醒医疗保健专业人员、肿瘤临床研究人员有关Tecentriq+紫杉醇III期IMpassion131临床的失败。FDA指出,在临床实践中,医护人员不应以紫杉醇取代Abraxane(白蛋白结合型紫杉醇)。(生物谷Bioon.com)
原文出处:Gilead nears deal to buy Immunomedics for more than $20 billion, WSJ reports
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


