全文编译!Science期刊发文揭示重症COVID-19中的细胞因子释放综合征,并探讨潜在的治疗方法
来源:本站原创 2020-04-24 13:52
2020年4月24日讯/生物谷BIOON/---2019年12月,一种新型冠状病毒---SARS-CoV-2---横空出世。除了严重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV)之外,SARS-CoV-2是第三种引起人类严重呼吸道疾病---称为2019年冠状病毒病(COVID-19)---的冠状
2020年4月24日讯/生物谷BIOON/---2019年12月,一种新型冠状病毒---SARS-CoV-2---横空出世。除了严重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV)之外,SARS-CoV-2是第三种引起人类严重呼吸道疾病---称为2019年冠状病毒病(COVID-19)---的冠状病毒。2020年3月,它被世界卫生组织(WHO)确认为大流行,对全球经济和健康产生了相当大的影响。尽管形势发展迅速,但在COVID-19病例中,有高达20%的COVID-19病例出现了以发热和肺炎为主要表现的严重疾病,从而导致急性呼吸窘迫综合征(ARDS)。这让人联想到在感染SARS-CoV和MERS-CoV的患者以及接受经过基因改造的T细胞治疗的白血病患者中观察到的细胞因子释放综合征(CRS)诱发的ARDS和继发性嗜血细胞增多症(sHLH)。鉴于这一经验,急需的基于抑制CRS的治疗药物(比如托珠单抗),已进入临床试验,用于治疗COVID-19。
SARS-CoV-2是一种与SARS-CoV关系最密切的β冠状病毒(betacoronavirus)。这两种病毒都是利用血管紧张素转换酶相关羧肽酶(ACE2)受体进入细胞。这种受体在心肺组织中广泛表达,但是在包括单核细胞和巨噬细胞在内的一些造血细胞中也有表达。SARS-CoV-2感染的一个重要特征是淋巴细胞减少(较低的血液淋巴细胞计数),这与临床严重程度有关。SARS-CoV能有效地感染原代人单核细胞和树突细胞,而MERS-CoV通过二肽基肽酶4(DPP4)感染单核细胞和T细胞。SARS-CoV-2也有可能感染树突细胞。由于树突细胞功能障碍,T细胞活化缺陷导致的T细胞凋亡和衰竭可能是COVID-19的免疫病理学的原因。然而,淋巴细胞减少作为COVID-19预后不良的生物标志物并不具有特异性,这是因为在2009年甲型H1N1流感大流行中,它也是与死亡相关的生物标志物。
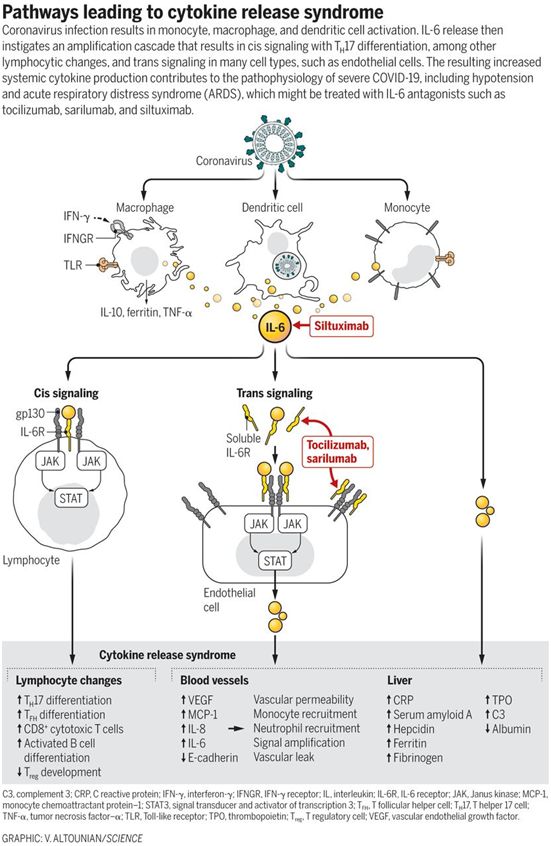
CRS被发现是SARS-CoV和MERS-CoV感染患者发病的主要原因。细胞因子IL-6和其他炎性细胞因子的血清浓度升高是严重的MERS-CoV感染的典型特征。CRS在COVID-19患者中很常见,血清IL-6升高与呼吸衰竭、ARDS和不良临床结果有关。血清C反应蛋白(CRP)升高也是严重的β冠状病毒感染的生物标志物,其中CRP的表达由IL-6驱动。
β冠状病毒对单核细胞、巨噬细胞和树突细胞的感染导致它们激活并分泌IL-6和其他炎性细胞因子。IL-6具有突出的促炎作用。IL-6可以通过两种主要途径发出信号,即经典的顺式信号转导和反式信号转导。在顺式信号转导中,IL-6与膜结合的IL-6受体(mIL-6R)结合,并与gp130形成复合物;下游的信号转导由JAK和STAT3介导。膜结合的gp130是广泛表达的,而mIL-6R的表达主要限于免疫细胞。激活顺式信号转导导致获得性免疫系统(B细胞和T细胞)以及先天性免疫系统[中性粒细胞、巨噬细胞和自然杀伤细胞(NK)]的多效性效应,这可能导致细胞因子释放综合征(CRS)。
在反式信号转导中,高循环浓度的IL-6与IL-6R的可溶性形式(sIL-6R)结合,在潜在的所有细胞表面上与gp130二聚体形成复合物。由此产生的IL-6-sIL-6R-JAK-STAT3信号转导在不表达mIL-6R的细胞(如内皮细胞)中被激活。这导致系统性的“细胞因子风暴”,涉及分泌血管内皮生长因子(VEGF)、单核细胞趋化蛋白-1(MCP-1)、IL-8和额外的IL-6,以及内皮细胞表面上的上皮型钙粘蛋白(E-cadherin)表达减少。VEGF和下降的上皮型钙粘蛋白表达导致血管通透性和渗漏,因而参与了ARDS中低血压和肺功能障碍的病理生理学过程。
sHLH是一种以CRS、低血细胞计数(cytopenias)和多器官衰竭(包括肝脏)为特征的高炎症综合征。在成年人中,sHLH最常由严重的病毒感染引发,但在接受经过基因改造的T细胞治疗的白血病患者中也会发生。除了血清细胞因子升高外,高浓度的铁蛋白也是sHLH的特征。鉴于表达CD163的巨噬细胞在网状内皮细胞铁信号转导中的作用,它们被认为是铁蛋白的来源,因此,sHLH又被称为巨噬细胞激活综合征。一项针对COVID-19患者的回顾性研究发现,血清铁蛋白和IL-6的升高与非生存者(nonsurvivor,指的是最终未存活下来的患者)相关。
接受嵌合抗原受体(CAR)-T(CAR-T)细胞治疗的患者也可发生CRS和sHLH。这种疗法涉及对患者T细胞进行基因改造,使之表达能识别肿瘤细胞表面抗原的CAR分子。当移植回患者体内后,这些经过基因改造的T细胞会靶向肿瘤细胞,从而激活免疫清除。Emily Whitehead是2012年第一个接受靶向CD19的CAR-T细胞治疗的小儿B细胞急性淋巴细胞白血病患者,她出现了严重的CRS和sHLH,从而导致ARDS,并伴有多器官功能衰竭和低血压,对标准的类固醇治疗难以耐受。由于这名患者的血清IL-6显著升高,她接受了托珠单抗的经验性治疗,其中托珠单抗是一种当时被批准用于治疗青少年特发性关节炎等风湿性疾病的IL-6R拮抗剂。在CAR-T细胞输注后的第7天,她接受了单剂量的托珠单抗,发热在数小时内迅速消退,随后停用血管紧张素(治疗低血压),并随着ARDS的消退而停用了呼吸机支持。托珠单抗目前已被美国食品药物管理局(FDA)批准用于治疗CAR-T细胞诱导的CRS,在数百名患者中已证实了它的疗效和最小的副作用。
IL-6/IL-6R拮抗剂治疗CRS和sHLH的疗效突显了IL-6信号转导在细胞因子驱动的高炎症综合征的病理生理学中的核心作用。鉴于相关的CRS样和sHLH样血清细胞因子升高,严重的COVID-19病例可能从抑制IL-6途径中获益。事实上,一项在中国21例COVID-19患者中使用托珠单抗治疗的开放标签研究的初步结果令人鼓舞。所有患者在接受托珠单抗治疗的第一天内,发热就已经消退。75%的患者对氧气的需求量减少。
全球范围内正在进行对照临床试验,以测试IL-6拮抗剂和IL-6R拮抗剂用于治疗伴有严重呼吸系统并发症的COVID-19患者。需要解决的一个问题是IL-6拮抗剂和IL-6R拮抗剂之间是否会有不同的疗效。与此相关的是,IL-6R抑制剂既可以抑制顺式和反式信号转导,也可以抑制反式呈递(trans presentation),即近期描述的第三种信号转导模式。反式呈递涉及IL-6与免疫细胞表面上表达的mIL-6R结合,并与在Th17细胞表面上的gp130形成复合物,从而导致可能参与ARDS产生的下游T细胞信号转导。然而,IL-6抑制剂只能抑制顺式和反式信号转导。IL-6拮抗的近期目标是改善严重的COVID-19病例,以便尽量减少高级护理的要求。长期目标应包括重点开发能够预防或改善感染的抗病毒药物和疫苗。
鉴于全球缓解COVID-19大流行的紧迫性,有一些注意事项需要考虑。在败血症相关的ARDS中,通常会使用皮质类固醇激素。然而,在SARS和MERS患者中使用皮质类固醇并没有改善死亡率,并导致病毒清除延迟。因此,目前传染病权威机构和世界卫生组织的专家共识是避免对COVID-19患者进行全身性皮质类固醇治疗。一个理论上的可能性是利用IL-6拮抗抑制炎症可能会延缓病毒清除。然而,IL-6阻断也会导致血清IL-10(一种由巨噬细胞分泌的免疫抑制性细胞因子)的快速降低,这可能会减轻对延长病毒清除时间的担忧。此外,一到两剂IL-6拮抗剂不太可能导致并发症,如真菌感染或下颌骨坏死等,这些并发症在每月服用这类药物治疗类风湿性关节炎等慢性疾病的患者中发生。值得注意的是,托珠单抗首先被批准用于治疗风湿性疾病,随后又被批准用于治疗接受CAR-T细胞治疗的患者中出现的CRS,现在又被进一步转用于遏制COVID-19大流行。在未来涉及流感病毒和埃博拉病毒等其他病毒的大流行中也有可能使用IL-6靶向疗法。(生物谷 Bioon.com)
参考资料:
John B. Moore et al. Cytokine release syndrome in severe COVID-19. Science, 2020, doi:10.1126/science.abb8925.
SARS-CoV-2是一种与SARS-CoV关系最密切的β冠状病毒(betacoronavirus)。这两种病毒都是利用血管紧张素转换酶相关羧肽酶(ACE2)受体进入细胞。这种受体在心肺组织中广泛表达,但是在包括单核细胞和巨噬细胞在内的一些造血细胞中也有表达。SARS-CoV-2感染的一个重要特征是淋巴细胞减少(较低的血液淋巴细胞计数),这与临床严重程度有关。SARS-CoV能有效地感染原代人单核细胞和树突细胞,而MERS-CoV通过二肽基肽酶4(DPP4)感染单核细胞和T细胞。SARS-CoV-2也有可能感染树突细胞。由于树突细胞功能障碍,T细胞活化缺陷导致的T细胞凋亡和衰竭可能是COVID-19的免疫病理学的原因。然而,淋巴细胞减少作为COVID-19预后不良的生物标志物并不具有特异性,这是因为在2009年甲型H1N1流感大流行中,它也是与死亡相关的生物标志物。

图片来自Science, 2020, doi:10.1126/science.abb8925。
CRS被发现是SARS-CoV和MERS-CoV感染患者发病的主要原因。细胞因子IL-6和其他炎性细胞因子的血清浓度升高是严重的MERS-CoV感染的典型特征。CRS在COVID-19患者中很常见,血清IL-6升高与呼吸衰竭、ARDS和不良临床结果有关。血清C反应蛋白(CRP)升高也是严重的β冠状病毒感染的生物标志物,其中CRP的表达由IL-6驱动。
β冠状病毒对单核细胞、巨噬细胞和树突细胞的感染导致它们激活并分泌IL-6和其他炎性细胞因子。IL-6具有突出的促炎作用。IL-6可以通过两种主要途径发出信号,即经典的顺式信号转导和反式信号转导。在顺式信号转导中,IL-6与膜结合的IL-6受体(mIL-6R)结合,并与gp130形成复合物;下游的信号转导由JAK和STAT3介导。膜结合的gp130是广泛表达的,而mIL-6R的表达主要限于免疫细胞。激活顺式信号转导导致获得性免疫系统(B细胞和T细胞)以及先天性免疫系统[中性粒细胞、巨噬细胞和自然杀伤细胞(NK)]的多效性效应,这可能导致细胞因子释放综合征(CRS)。
在反式信号转导中,高循环浓度的IL-6与IL-6R的可溶性形式(sIL-6R)结合,在潜在的所有细胞表面上与gp130二聚体形成复合物。由此产生的IL-6-sIL-6R-JAK-STAT3信号转导在不表达mIL-6R的细胞(如内皮细胞)中被激活。这导致系统性的“细胞因子风暴”,涉及分泌血管内皮生长因子(VEGF)、单核细胞趋化蛋白-1(MCP-1)、IL-8和额外的IL-6,以及内皮细胞表面上的上皮型钙粘蛋白(E-cadherin)表达减少。VEGF和下降的上皮型钙粘蛋白表达导致血管通透性和渗漏,因而参与了ARDS中低血压和肺功能障碍的病理生理学过程。
sHLH是一种以CRS、低血细胞计数(cytopenias)和多器官衰竭(包括肝脏)为特征的高炎症综合征。在成年人中,sHLH最常由严重的病毒感染引发,但在接受经过基因改造的T细胞治疗的白血病患者中也会发生。除了血清细胞因子升高外,高浓度的铁蛋白也是sHLH的特征。鉴于表达CD163的巨噬细胞在网状内皮细胞铁信号转导中的作用,它们被认为是铁蛋白的来源,因此,sHLH又被称为巨噬细胞激活综合征。一项针对COVID-19患者的回顾性研究发现,血清铁蛋白和IL-6的升高与非生存者(nonsurvivor,指的是最终未存活下来的患者)相关。
接受嵌合抗原受体(CAR)-T(CAR-T)细胞治疗的患者也可发生CRS和sHLH。这种疗法涉及对患者T细胞进行基因改造,使之表达能识别肿瘤细胞表面抗原的CAR分子。当移植回患者体内后,这些经过基因改造的T细胞会靶向肿瘤细胞,从而激活免疫清除。Emily Whitehead是2012年第一个接受靶向CD19的CAR-T细胞治疗的小儿B细胞急性淋巴细胞白血病患者,她出现了严重的CRS和sHLH,从而导致ARDS,并伴有多器官功能衰竭和低血压,对标准的类固醇治疗难以耐受。由于这名患者的血清IL-6显著升高,她接受了托珠单抗的经验性治疗,其中托珠单抗是一种当时被批准用于治疗青少年特发性关节炎等风湿性疾病的IL-6R拮抗剂。在CAR-T细胞输注后的第7天,她接受了单剂量的托珠单抗,发热在数小时内迅速消退,随后停用血管紧张素(治疗低血压),并随着ARDS的消退而停用了呼吸机支持。托珠单抗目前已被美国食品药物管理局(FDA)批准用于治疗CAR-T细胞诱导的CRS,在数百名患者中已证实了它的疗效和最小的副作用。
IL-6/IL-6R拮抗剂治疗CRS和sHLH的疗效突显了IL-6信号转导在细胞因子驱动的高炎症综合征的病理生理学中的核心作用。鉴于相关的CRS样和sHLH样血清细胞因子升高,严重的COVID-19病例可能从抑制IL-6途径中获益。事实上,一项在中国21例COVID-19患者中使用托珠单抗治疗的开放标签研究的初步结果令人鼓舞。所有患者在接受托珠单抗治疗的第一天内,发热就已经消退。75%的患者对氧气的需求量减少。
全球范围内正在进行对照临床试验,以测试IL-6拮抗剂和IL-6R拮抗剂用于治疗伴有严重呼吸系统并发症的COVID-19患者。需要解决的一个问题是IL-6拮抗剂和IL-6R拮抗剂之间是否会有不同的疗效。与此相关的是,IL-6R抑制剂既可以抑制顺式和反式信号转导,也可以抑制反式呈递(trans presentation),即近期描述的第三种信号转导模式。反式呈递涉及IL-6与免疫细胞表面上表达的mIL-6R结合,并与在Th17细胞表面上的gp130形成复合物,从而导致可能参与ARDS产生的下游T细胞信号转导。然而,IL-6抑制剂只能抑制顺式和反式信号转导。IL-6拮抗的近期目标是改善严重的COVID-19病例,以便尽量减少高级护理的要求。长期目标应包括重点开发能够预防或改善感染的抗病毒药物和疫苗。
鉴于全球缓解COVID-19大流行的紧迫性,有一些注意事项需要考虑。在败血症相关的ARDS中,通常会使用皮质类固醇激素。然而,在SARS和MERS患者中使用皮质类固醇并没有改善死亡率,并导致病毒清除延迟。因此,目前传染病权威机构和世界卫生组织的专家共识是避免对COVID-19患者进行全身性皮质类固醇治疗。一个理论上的可能性是利用IL-6拮抗抑制炎症可能会延缓病毒清除。然而,IL-6阻断也会导致血清IL-10(一种由巨噬细胞分泌的免疫抑制性细胞因子)的快速降低,这可能会减轻对延长病毒清除时间的担忧。此外,一到两剂IL-6拮抗剂不太可能导致并发症,如真菌感染或下颌骨坏死等,这些并发症在每月服用这类药物治疗类风湿性关节炎等慢性疾病的患者中发生。值得注意的是,托珠单抗首先被批准用于治疗风湿性疾病,随后又被批准用于治疗接受CAR-T细胞治疗的患者中出现的CRS,现在又被进一步转用于遏制COVID-19大流行。在未来涉及流感病毒和埃博拉病毒等其他病毒的大流行中也有可能使用IL-6靶向疗法。(生物谷 Bioon.com)
参考资料:
John B. Moore et al. Cytokine release syndrome in severe COVID-19. Science, 2020, doi:10.1126/science.abb8925.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


