中国尿路上皮癌(UC)PD-(L)1疗法!百济神州百泽安®(替雷利珠单抗)获批第2个适应症!
来源:本站原创 2020-04-11 21:26
2020年04月11日讯 /生物谷BIOON/ --百济神州(BeiGene)是一家处于商业阶段的生物科技公司,专注于用于癌症治疗的创新型分子靶向和免疫肿瘤药物的开发和商业化。近日,该公司宣布抗PD-1抗体药物百泽安®(通用名:替雷利珠单抗注射液)获得国家药品监督管理局(NMPA)批准,用于治疗接受含铂化疗失败包括新辅助或辅助化疗12个月内进展的局

2020年04月11日讯 /生物谷BIOON/ --百济神州(BeiGene)是一家处于商业阶段的生物科技公司,专注于用于癌症治疗的创新型分子靶向和免疫肿瘤药物的开发和商业化。近日,该公司宣布抗PD-1抗体药物百泽安®(通用名:替雷利珠单抗注射液)获得国家药品监督管理局(NMPA)批准,用于治疗接受含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性PD-L1高表达的尿路上皮癌(UC)患者。
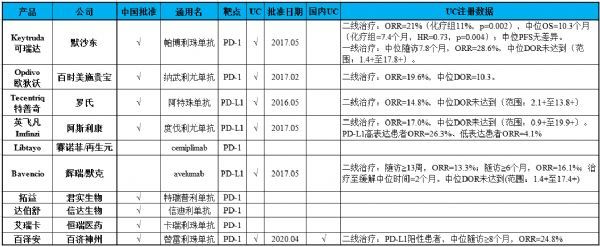
在全球范围内,目前已有10款PD-(L)1疗法获得批准,其中已有8款在中国获批。这10款疗法中,已有6款获批尿路上皮癌(UC)适应症。值得一提的是,百泽安®是国内首个被批准治疗UC的抗PD-(L)1疗法。
(点击图片,查看大图)
百泽安®于2019年12月首次获得NMPA批准用于治疗经典型霍奇金淋巴瘤患者,此项批准中的UC是百泽安®获批的第二项适应症,也是首项获批的实体瘤适应症。此前,该项新适应症上市申请(sNDA)已被国家药品监督管理局药品审评中心(CDE)纳入优先审评。
百济神州中国区总经理兼公司总裁吴晓滨博士表示:“百济神州一直以来致力于为全球患者带来有影响力、高质量的创新性药物。这是我们自主研发产品在过去五个月内获得的第三项上市批准,对百济神州这样一家年轻的生物科技公司来说是一项巨大的成就,也是对我们团队努力工作的肯定。公司针对百泽安®制定的长期战略计划是获得广泛适应症批准,以帮助与不同癌症作斗争的患者。这是百泽安®首项获批的实体瘤适应症,我们也因此对这款免疫肿瘤药物的前景倍感激动。”
复旦大学附属肿瘤医院副院长叶定伟教授评论道:“对国内晚期尿路上皮癌患者来说,现有的治疗方案十分有限。替雷利珠单抗注射液作为一款全新的免疫肿瘤治疗药物,在临床上获得了令人欣喜的有效性和安全性,客观缓解率高达24.8%,我们期待它能为国内肿瘤患者带来更深远的临床获益。”
百济神州高级副总裁、全球药政事务负责人闫小军女士表示:“我们很欣喜地看到百泽安®针对UC适应症的上市申请获得批准。今天的成果离不开参与这项试验的临床专家、那些将自己的抗癌治疗托付给我们的患者以及我们团队的付出。目前,百泽安®广泛的开发项目包括15 项潜在的注册性临床试验,除了已经获批的经典型霍奇金淋巴瘤和UC以外,覆盖肺癌、肝癌、食道癌、胃癌、鼻咽癌以及高位卫星不稳定(MSI-H)或错配修复缺陷性(dMMR)实体瘤在内的多项癌种。我们希望百泽安®能够再接再厉,为更多患者带来福音。”
此次百泽安®获得NMPA批准是基于一项在中国和韩国开展的用于治疗既往接受过含铂化疗且PD-L1高表达的局部晚期或转移性UC患者的单臂、多中心、关键性2期临床试验(clinicaltrials.gov登记号:NCT04004221;药物临床试验登记号:CRT20170071)。符合疗效评估的患者中,在随访时间至少为12个月、中位随访时间为14个月的情况下,经独立评审委员会(IRC)根据RECIST实体瘤疗效评估标准1.1版评估的客观缓解率(ORR)为24.8%,完全缓解(CR)率为9.9%。
百泽安®说明书中的安全性数据来自参与四项百泽安®单药临床试验的934位患者,包括前文提及的针对UC的关键性2期临床试验。最常见的不良反应(≥10%)为皮疹、疲乏及丙氨酸氨基转移酶升高。在至少1%患者中出现的三级或以上的不良反应包括γ-谷氨酰转移酶升高、贫血、天门冬氨酸氨基转移酶升高、丙氨酸氨基转移酶升高、肺炎(非感染性)、重度皮肤反应、低钾血症。
百泽安®与同类产品相似,可能会发生免疫相关不良反应,主要包括肺炎、腹泻及结肠炎、肝炎、内分泌疾病(甲状腺功能减退、亢进和甲状腺炎、肾上腺皮质功能不全、高血糖症及 I 型糖尿病)和皮肤不良反应,另外肾炎、胰腺炎、心肌炎、肌炎与其他免疫相关性不良反应也偶见发生。百泽安®采用静脉输注的方式给药,推荐剂量为200mg,每3周给药一次。用药直至疾病进展或出现不可耐受的毒性。
尿路上皮癌(UC):又称移行细胞癌(TCC),是目前最常见的一种膀胱癌,占所有膀胱癌病例的90%以上。膀胱癌是世界第十大最常见癌种,在2018年约有55万例新增病例。在中国,膀胱癌是男性中第八大最常见癌种,在2019年约有62000例新增病例。尽管UC最常见于膀胱中,但也可发生在泌尿系统的其他部位。
百泽安®(替雷利珠单抗):是一款人源化lgG4抗程序性死亡受体1(PD-1)单克隆抗体,设计目的是为最大限度地减少与巨噬细胞中的FcγR受体结合。临床前数据表明,巨噬细胞中的FcγR受体结合之后会激活抗体依赖细胞介导杀伤T细胞,从而降低了PD-1抗体的 抗肿瘤活性。替雷利珠单抗是第一款由百济神州的免疫肿瘤生物平台研发的药物,目前正进行单药及联合疗法临床试验,开发一系列针对实体瘤和血液肿瘤的广泛适应症。
百泽安®已获得中国国家药品监督管理局(NMPA)批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者,以及获批用于治疗PD-L1高表达的含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌患者。 (生物谷Bioon.com)
原文出处:百济神州、美国FDA新药数据库
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->