贫血新药!BMS首创红细胞成熟剂Reblozyl治疗骨髓增生异常综合症(MDS)贫血III期临床疗效显著!
来源:本站原创 2020-01-11 10:14
2020年01月11日讯 /生物谷BIOON/ --百时美施贵宝(BMS)与Acceleron制药公司近日联合宣布,评估红细胞成熟剂Reblozyl(luspatercept-aamt)用于骨髓增生异常综合症(MDS)患者治疗贫血的关键性III期MEDALIST研究(NCT02631070)的结果已发表于《新英格兰医学杂志》(NEJM)。MEDALIST是一

2020年01月11日讯 /生物谷BIOON/ --百时美施贵宝(BMS)与Acceleron制药公司近日联合宣布,评估红细胞成熟剂Reblozyl(luspatercept-aamt)用于骨髓增生异常综合症(MDS)患者治疗贫血的关键性III期MEDALIST研究(NCT02631070)的结果已发表于《新英格兰医学杂志》(NEJM),文章题目为:Luspatercept in Patients with Lower-Risk Myelodysplastic Syndromes。
MEDALIST是一项随机、双盲、安慰剂对照、多中心III期研究,在229例极低至中危MDS患者中开展,评估了luspatercept与安慰剂治疗贫血的疗效和安全性。这些患者存在环形铁粒幼细胞(RS+)、需要输注红细胞,并且接受红细胞生成刺激剂(ESA)治疗已失败、或对ESA不耐受、或不符合资格/不太可能对ESA治疗产生反应。研究中,患者以2:1的比例随机分配接受luspatercept(n=153,每3周一次皮下注射1.0-1.75mg/kg体重)或安慰剂(n=76)。主要终点是研究第1-24周期间脱离红细胞输注(即红细胞输注非依赖RBC-TI)8周或更长时间。关键次要终点是研究第1-24周期间、第1-48周期间脱离红细胞输注12周或更长时间。
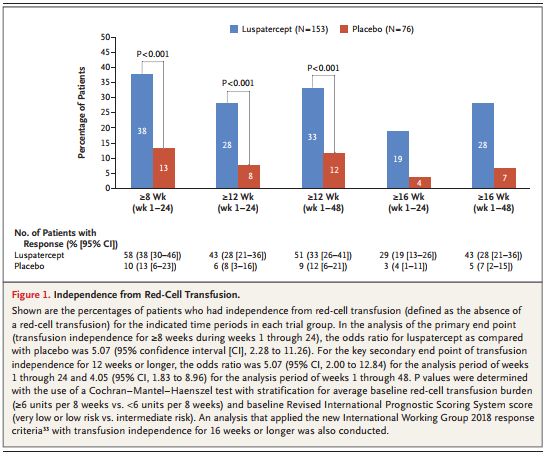
结果显示,该研究达到了主要终点:与安慰剂组相比,luspatercept治疗组在研究的前24周(第1-24周)脱离红细胞输注(RBC-TI)≥8周的患者比例具有统计学意义的显著提高(38% vs 18%,p<0.001)。此外,与安慰剂组相比,luspatercept治疗组患者达到关键次要终点的患者比例更高(第1-24周期间RBC-TI≥12周:28% vs 8%;第1-48周期间RBC-TI≥12周:33% vs 12%;两组比较p<0.001)。该研究中,与luspatercept相关的最常见不良事件(任何级别)包括疲劳、腹泻、乏力、恶心和头晕。不良事件发生率随着时间的推移而降低。
上述结果表明,接受常规红细胞输注、存在环形铁粒幼细胞(RS+)、对红细胞生成刺激剂(ESA)难治或不太可能产生治疗反应或由于不良事件而停止此类药物的极低至中位MDS患者中,luspatercept治疗降低了贫血的严重程度、患者输血负担显著减少。
Reblozyl是一种红细胞成熟剂,于2019年11月获得美国FDA批准,用于需要定期输注红细胞的β地中海贫血成人患者,治疗贫血。
值得一提的是,Reblozyl是首个获FDA批准治疗β地中海贫血相关贫血的药物,同时是首个获得DA批准的红细胞成熟剂,代表了新一类的疗法,通过调节红细胞成熟后期阶段来帮助患者减少红细胞输注负担。需要指出的是,Reblozyl在需要立即纠正贫血的患者中不适用于作为红细胞输注的替代品。
目前,Reblozyl治疗MDS贫血的生物制品许可申请(BLA)正在接受FDA的审查,该BLA申请批准Reblozyl用于骨髓涂片存在环形铁幼粒细胞(ring sideroblast,RS+)、需要常规输注红细胞(RBC)、极低危至中危MDS成人患者治疗贫血,处方药用户收费法(PDUFA)目标日期为2020年4月4日。在欧洲,Reblozyl治疗成人β地中海贫血和MDS贫血的营销授权申请(MAA)正在接受欧洲药品管理局(EMA)的审查。
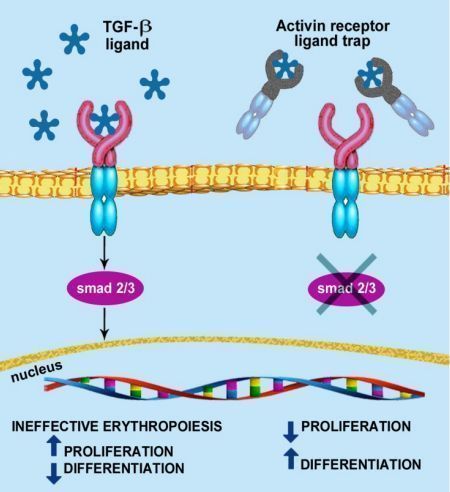
luspatercept的作用机制
Reblozyl的活性药物成分为luspatercept,这是一种首创的(first-in-class)红细胞成熟剂(EMA),可调节晚期红细胞的成熟。该药是一种可溶性融合蛋白,由人IgG1的Fc结构域与激活素IIB型受体(ActRIIB)胞外结构域融合而成,作为一种配体陷阱,通过靶向结合可调节晚期RBC成熟的转化生长因子(TGF)-β超家族的特定配体,减少Smad2/3信号通路的激活,改善无效红细胞的生成,促进晚期红细胞的成熟,提高血红蛋白水平。
luspatercept由新基(已被BMS收购)与Acceleron制药公司合作进行全球开发。目前,双方也正在评估luspatercept治疗促红细胞生成刺激剂(ESA)初治、低危MDS患者(III期COMMANDS研究)和非输血性β地中海贫血(II期BEYOND研究)以及骨髓纤维化的潜力。业界对luspatercept的商业前景也十分看好。去年底,EvaluatePharma发布报告《Vantage 2019 Preview》,盘点了全球20个更有价值的研发项目,luspatercept以31亿美元的净现值(NPV)位列第18位。
此前,华尔街著名投资银行Jefferies分析师指出,如果骨髓增生异常综合症(MDS)贫血也获得FDA批准,Reblozyl的年销售峰值将达到20亿美元。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


