胰腺癌重磅消息!阿斯利康/默沙东Lynparza(利普卓)治疗gBRCAm胰腺癌获美国FDA专家委员会支持!
来源:本站原创 2019-12-19 09:45
2019年12月19日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)与合作伙伴默沙东(Merck & Co)近日联合宣布,美国食品和药物管理局(FDA)肿瘤药物顾问委员会(ODAC)以7票对5票的投票结果,建议批准靶向抗癌药Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利),作为一线维持单药疗法,治疗接受一线

2019年12月19日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)与合作伙伴默沙东(Merck & Co)近日联合宣布,美国食品和药物管理局(FDA)肿瘤药物顾问委员会(ODAC)以7票对5票的投票结果,建议批准靶向抗癌药Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利),作为一线维持单药疗法,治疗接受一线铂类化疗后病情无进展、携带生殖系BRCA突变(gBRCAm)的转移性胰腺癌患者。
2019年8月,FDA受理了Lynparza针对上述适应症的补充新药申请(sNDA)并正对其进行优先审查,处方药用户收费法(PDUFA)目标日期为2019年第四季度。除了美国之外,Lynparza针对该适应症的申请正在接受欧盟、加拿大、其他司法管辖区的监管审查。
阿斯利康肿瘤学研发执行副总裁José Baselga表示:“我们很高兴ODAC推荐批准Lynparza,该药有潜力为携带gBRCA突变的转移性胰腺癌患者带来一种个体化的生物标志物靶向药物。过去几十年来,由于胰腺癌的侵袭性和有限的治疗进展,晚期胰腺癌患者的预后一直很差。我们期待着在FDA审查的过程中与其密切合作。”
默沙东研究实验室首席医疗官、高级副总裁兼全球临床开发主管Roy Baynes表示:“ODAC对Lynparza作为gBRCA突变转移性胰腺癌一线维持治疗的支持投票结果让我们感到鼓舞。这项建议是朝着帮助患有这种致命疾病的患者实现我们的目标迈出的重要一步。”
该sNDA的提交,基于III期临床研究POLO的阳性结果。相关结果已在今年6月举行的2019年美国临床肿瘤学会(ASCO)年会上公布,并发表于《新英格兰医学杂志》(NEJM)。值得一提的是,基于该研究结果,Lynparza成为在III期研究中在治疗gBRCAm转移性胰腺癌方面表现出生存益处的唯一PARP抑制剂。在美国,FDA之前已授予Lynparza治疗胰腺癌的孤儿药资格。
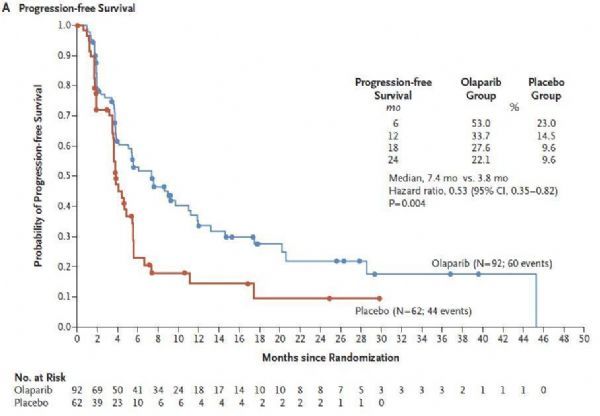
POLO研究是一项随机、双盲、安慰剂对照、多中心研究,在154例接受一线含铂化疗病情没有进展、并且携带生殖系BRCA突变(gBRCAm)的转移性胰腺癌患者中开展,评估了Lynparza(300mg,每日2次)相对于安慰作为一线维持单药疗法的疗效和安全性。研究中,患者以3:2的比例接受Lynparza或安慰剂治疗,直至病情进展。研究的主要终点是无进展生存期(PFS),关键次要终点包括总生存期(OS)、二次疾病进展时间、总缓解率、疾病控制率、健康相关生活质量。
结果显示,该研究达到了主要终点:与安慰剂组相比,Lynparza治疗组PFS表现出统计学意义和临床意义的改善(中位PFS:7.4个月 vs 3.8个月)、疾病进展或死亡风险降低了47%(HR=0.53[95%CI:0.35-0.82],p=0.004)。
在一系列有临床意义的终点中,使用Lynparza维持治疗的益处是一致的。从六个月开始,在每个时间点,没有出现疾病进展的患者比例,Lynparza治疗组均为安慰剂组的2倍多(1年:34% vs 15%;2年:22% vs 10%)。在基线检查时有可测量疾病的患者中,23%对Lynparza治疗有反应、12%对安慰剂治疗有反应,Lynparza中位疗程超过2年(24.9个月)、安慰剂为3.7个月。中期分析时,Lynparza治疗组的总生存期(OS)为18.9个月,安慰剂组为18.1个月,数据未达到统计学显著差异(HR=0.90,p=0.68)。该研究中,Lynparza的安全性和耐受性与先前的研究中一致。
POLO研究是评估任何PARP抑制剂治疗gBRCAm转移性胰腺癌方面的首个阳性III期研究,这是一种毁灭性的疾病,存在着严重的未满足医疗需求。来自POLO研究的结果为过去20年来进展甚微的患者群体带来了新的希望,并进一步证明了Lynparza在多种BRCA突变肿瘤类型中的临床疗效。
Lynparza(利普卓):中国2018年8月获批,标志着卵巢癌进入PARP抑制剂时代
胰腺癌是全球第12大最常见癌症类型和第七大癌症死亡原因,在最常见癌症中的生存率最差,在每个国家,确诊后的5年生存率仅为个位数(2-9%)。胰腺癌的早期诊断很困难,患者通常无症状,直至病情发展至晚期时才出现症状,大约80%的患者在转移性阶段被诊断出来,这些患者的平均存活时间不到一年。过去几十年来,胰腺癌诊断和治疗方面几乎没有进展,当前的治疗是手术(仅适用于10-20%的患者)、化疗和放疗,突显了对更有效治疗方案的关键未满足需求。在全球范围内,2018年约确诊46万新病例,gBRCAm胰腺癌占所有病例的5-7%。
Lynparza于2014年12月获美国FDA批准上市,成为全球获批的首个PARP抑制剂。Lynparza是一种首创、口服PARP抑制剂,利用DNA修复途径的缺陷优先杀死癌细胞,这种作用模式赋予了Lynparza具有治疗存在DNA修复缺陷的广泛类型肿瘤的潜力。PARP与广泛的肿瘤类型相关,尤其是乳腺癌和卵巢癌。目前,阿斯利康正开展多个临床研究,调查Lynparza用于广泛类型肿瘤的潜力,包括乳腺癌、前列腺癌、胰腺癌。
阿斯利康与默沙东于2017年7月达成肿瘤学全球战略合作,共同开发和商业化Lynparza及另一种MEK抑制剂selumetinib治疗多种类型肿瘤。阿斯利康对Lynparza寄予了非常高的期望,认为该药的年销售额将突破20亿美元。
在中国市场,Lynparza(利普卓)于2018年8月23日获得中国国家药品监督管理局(CNDA)批准,用于铂敏感复发性卵巢癌的维持治疗。此次批准,使Lynparza成为中国市场首个获批治疗卵巢癌的靶向药物,标志着中国卵巢癌治疗进入PARP抑制剂时代。
本月初,Lynparza(利普卓)再次获批,用于BRCA突变晚期卵巢癌患者的一线维持治疗。受益于中国大力支持医药创新及加速推进临床急需新药审批,Lynparza(利普卓)成为中国首个获批用于卵巢癌一线维持疗法的PARP抑制剂。2019年11月28日,Lynparza(利普卓)被列入国家医保目录。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->