2019年10月Cell期刊不得不看的亮点研究
来源:本站原创 2019-10-31 21:47
2019年10月31日讯/生物谷BIOON/---2019年10月份即将结束了,10月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:开发出光学混合筛选技术,可在几天内筛选人细胞中的数千个基因doi:10.1016/j.cell.2019.09.016如今,在一项新的研究中,来自美国麻省理工学院和布罗德研究所的研究人员开发出一种方法,该方法将大规模混合筛选与
2019年10月31日讯/生物谷BIOON/---2019年10月份即将结束了,10月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:开发出光学混合筛选技术,可在几天内筛选人细胞中的数千个基因
doi:10.1016/j.cell.2019.09.016
如今,在一项新的研究中,来自美国麻省理工学院和布罗德研究所的研究人员开发出一种方法,该方法将大规模混合筛选与基于图像的细胞行为分析相结合。这种称为光学混合筛选(optical pooled screen)的方法允许人们在空间和时间分辨率下研究基因如何影响细胞过程,而其他的混合筛选方法则无法做到这一点。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“Optical Pooled Screens in Human Cells”。论文通讯作者为布罗德研究所核心研究所成员、麻省理工学院生物工程系副教授Paul Blainey博士。论文第一作者为Blainey 实验室博士后研究员Avtar Singh和Blainey 实验室物前理学博士生David Feldman。基因编辑大牛张锋(Feng Zhang)也是这篇论文的共同作者。
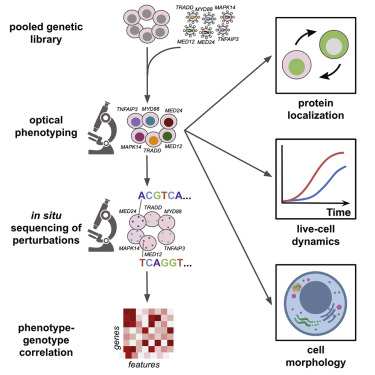
Singh说,“通过这种新方法,任何人都可以在无需专门设备的情况下使用显微镜在几天内筛查数千个基因。”
这些研究人员通过对数百万个细胞中一种称为p65的蛋白的细胞位置进行成像,研究了952个基因对一种称为NF-kB的免疫调节复合物的信号转导活性的影响。他们发现了两个基因---MED12和MED24---在NFkB信号弛豫过程中的新作用。
2.Cell:从拓扑学角度揭示DNA复制之谜
doi:10.1016/j.cell.2019.09.034
生命分子存在缠绕的现象。但是,DNA双螺旋中那两条熟悉的链是如何在没有缠绕的情况下成功复制的,这就很难解释了。在一项新的研究中,来自美国康奈尔大学的研究人员从拓扑学角度解决了这个问题。他们研究了这种双螺旋形状对DNA复制的影响。通过使用真核生物作为模型系统,他们发现染色质(由DNA、组蛋白和非组蛋白等成分组成)的内在机械性能决定着染色质纤维如何缠绕。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“Synergistic Coordination of Chromatin Torsional Mechanics and Topoisomerase Activity”。
在DNA复制过程--复制体(replisome)将两条DNA链分开并向前移动---中,DNA也必须绕双螺旋轴缠绕。这会让DNA承受很大的扭转应力(torsional stress),从而导致DNA发生额外的扭曲。问题在于:额外的扭曲在哪里发生?如果额外的扭曲仅发生在复制体的正面,那么两个子DNA分子将不会缠绕在一起,因此它们可以分开。但是,如果额外的扭曲发生在复制体的背面,那么两个子DNA分子将缠绕在一起,无法分开。这将为细胞分裂过程中的染色体分离创造一个主要问题,这可能导致DNA损伤并导致细胞死亡或癌症。
这些研究人员发现,缠绕单条染色质纤维比缠绕双条染色质纤维要容易得多。这意味着额外的扭曲将优先发生在复制体的正面,从而让两个子DNA分子之间的缠绕最小化。在一个单独的实验中,他们发现,一种能解开双螺旋DNA的酶(拓扑异构酶II)强烈偏爱正面的单条染色质纤维。染色质机械性能和拓扑异构酶活性似乎以协同方式协调,以减少子DNA分子之间的缠绕。
3.Cell:重大进展!开发出比CAR-T细胞更安全、用途更广的cCAR-T细胞技术
doi:10.1016/j.cell.2019.10.002
在一项新的研究中,来自美国格拉斯通研究所和Xyphos生物科学公司(Xyphos Biosciences, Inc.)的研究人员描述了一种攻击被HIV感染的细胞的新技术。这种新技术是CAR-T细胞免疫疗法的一种新的改进版本。近年来,这种疗法因在抵抗血癌上取得的成功而闻名于世。通过改进使得它具有更大的覆盖范围和多功能性,这种称为convertibleCAR T细胞(cCAR-T)的新技术在多个治疗领域显示出了巨大的前景,特别是在抗击HIV方面,这是因为它可以用来缩小在接受抗逆转录病毒疗法(ART)期间HIV感染者体内持续存在的受感染细胞的库存量。相关研究结果于2019年10月24日在线发表在Cell期刊上,论文标题为“Attacking Latent HIV with convertibleCAR-T Cells, a Highly Adaptable Killing Platform”。论文通讯作者为格拉斯通研究所HIV治愈研究中心主任Warner C. Greene博士。
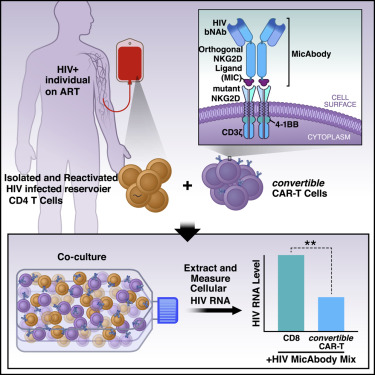
人们已证实传统的CAR-T细胞在诱导血癌(比如淋巴瘤和儿童白血病)缓解方面非常成功。但是作为抵抗HIV感染的疗法,传统的CAR-T细胞并不完美。论文第一作者、Greene实验室科学家Eytan Herzig说,“传统的CAR-T细胞的一些缺点是它们经过基因改造后靶向癌细胞表面上的单个分子,而且一旦被注射到患者体内,无法对它们进行控制。”
Xyphos生物科学公司通过从细胞毒杀伤细胞中分离出靶向抗体克服了这些缺陷。该公司首席科学家David W. Martin博士解释说:“我们对cCAR-T细胞进行了基因改造,使得这些T细胞可以在其表面上表达受到少量修饰的人类受体蛋白NKG2D。”这种受到修饰的NKG2D受体当与它的搭档结合时,可以将这些T细胞变成有效的杀手。它的搭档是一种叫做MIC-A的蛋白质,Xyphos生物科学公司的科学家对它进行了裁剪和修饰,使得它可以与cCAR-T细胞表面上这种经过修饰的NKG2D受体特异性结合。这些科学家随后将它与靶向抗体的底部融合在一起,从而构建出他们称为MicAbody的产物。因此,这种靶向性MicAbody紧密地和唯一地结合cCAR-T细胞。
为了清除潜伏性HIV病毒库,Herzig和Greene一直在实验室中测试称为广泛中和抗体(bNAb)的抗HIV抗体。他们与Xyphos生物科学公司的科学家合作,基于bNAb构建出MicAbody(称为Mic-bNAb),并在各种实验室分析中测试了cCAR-T细胞和Mic-bNAb的组合使用。
在实验室中,Herzig以感染了各种HIV毒株的多种CD4 T细胞(HIV的天然靶标)为研究对象测试了这些组合。特别是,他使用了源自人类扁桃体的细胞制剂;已知在HIV感染者中,扁桃体T细胞是潜伏性HIV病毒库。他想确保cCAR-T/Mic-bNAb组合使用能杀死代表潜伏性HIV病毒库的T细胞类型。
结果是显著的:cCAR-T细胞与Mic-bNAb的组合使用特异性地杀死了受到感染的CD4 T细胞,但未杀死未感染的细胞。它们仅与Mic-bNAb组合使用时才杀死受感染的细胞,然而,不论是单独使用还是与不靶向HIV的MicAbody组合使用都没有这种效果。他们杀死了在实验室中感染了多种HIV毒株的CD4 T细胞。当与靶向HIV的Mic-bNAb和靶向癌细胞的MicAbody组合使用时,cCAR-T细胞可以有效杀死在相同细胞培养物中混合在一起的癌细胞和受到HIV感染的细胞。换句话说,cCAR-T细胞精确地证明了它旨在实现的多功能性和特异性。
最后,Herzig和Greene测试了cCAR-T/Mic-bNAb平台是否可以攻击接受ART治疗的HIV感染者血液中存在的潜伏性HIV病毒库。为了让这些细胞对cCAR-T细胞可见,他们首先用强效的称为“潜伏逆转剂(latency-reversing agent)”的化合物活化这些细胞培养物。在接触后48小时内,一半以上活化的表达HIV靶抗原的细胞被清除。Greene总结道,“这个平台前景广阔。”
4.Cell:开发出BARseq技术,构建出更好的大脑图谱
doi:10.1016/j.cell.2019.09.023
美国冷泉港实验室Anthony Zador教授及其团队一直在研究大脑回路如何介导和控制复杂的行为,在10年前就着手绘制大脑功能的三个支柱:连接性、基因表达和生理活性。由于尚无有效地做到这一点的技术,他的团队开发出MAPseq,即一种用来绘制不同脑细胞之间的连接图谱并更好地了解它们彼此之间如何相互作用的技术。多年来,Zador和他的实验室持续地改进这种技术。
在一项新的研究中,在博士后研究员Xiaoyin Chen的领导中,Zador实验室介绍了下一代的MAPseq技术:BARseq。这种新技术可用于通过精确地指出神经元所在的位置来扩展大脑图谱。这使得BARseq不仅可以确定神经元的连接,还可以确定其基因表达模式和生理活性,这是MAPseq不能解决的两个难题。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“High-Throughput Mapping of Long-Range Neuronal Projection Using In Situ Sequencing”。
这些研究人员使用BARseq绘制了小鼠大脑听觉皮层中3579个神经元的连接图谱。将连接性模式与基因表达相匹配,可使科学家们表征不同的细胞类型并确定其在大脑中的特定功能。这将被证明是研究神经回路如何形成的一种有价值的工具。
5.Cell:有趣!雄性和雌性小鼠大脑中或存在不同类型的脑细胞!
doi:10.1016/j.cell.2019.09.020
近日,一项刊登在国际杂志Cell上的研究报告中,来自加州理工学院等机构的科学家们通过在雄性小鼠中发现了罕见的大脑细胞类型,同时在雌性小鼠中也发现了另外一种特殊类型的大脑细胞,这些存在于大脑特殊区域的性别特异性细胞在控制攻击性和交配行为上扮演着非常关键的角色。
下丘脑是包括人类在内所有脊椎动物大脑中的一个特殊区域,此前研究表明,下丘脑中特殊的解剖区域(VMHvl,腹内侧下丘脑腹外侧区域)含有能控制机体攻击性和交配行为的细胞;在这些研究中,对雄性和雌性小鼠大脑中的神经元进行强烈刺激或能促进小鼠变得更具攻击性(即使没有任何威胁),然而,微弱的刺激则会促进小鼠开始交配行为。
这项研究中,研究人员通过研究分析了VMHvl区域中单个细胞中的基因表达情况,利用先进的转录组学技术,研究人员就能识别出细胞中含有的RNA转录物,他们能利用这些信息来识别不同的细胞类型。此前研究中,研究人员分析了每个细胞中10%的转录物,而本文研究中,研究者则对大部分RNA转录组进行了分析,他们发现,这一小块区域中含有17种不同类型的大脑细胞,更重要的是,党对基因表达模式进行分析后,研究者发现,相比雌性小鼠而言,雄性小鼠机体中的这17种细胞类型更为丰富,而其它细胞类型则在雌性小鼠机体中更为丰富。
6.Cell:科学家阐明受精卵早期发育的分子机制 有望理解生命起源的奥秘
doi:10.1016/j.cell.2019.09.029
尽管从学校毕业、找到人生第一份工作和结婚可能是人生中重要的事情,但一些最重要的事情往往发生地更早,即在精子与卵子结合、细胞开始分裂的最初几天里。受精卵前100个细胞(囊胚)的组织方式对于妊娠是否成功、器官形成甚至以后对个体疾病(比如阿尔兹海默病等)的发生都有着非常深远的影响;然而,截止到目前为止,研究人员并没有找到一个好的方法来模拟囊胚形成的方式。
近日,一项刊登在国际杂志Cell上的研究报告中,来自索尔克研究所等机构的科学家们通过研究首次从单个培养的细胞创造出了小鼠囊胚样结构,这一过程绕过了研究者对自然胚胎的需求。这些囊胚样结构拥有和天然胚泡相同的结构,其甚至能植入到子宫中,这或许就有望帮助研究人员研究人类机体发育、怀孕及不孕等健康问题。
本文研究或有望帮助研究者深入探索早期发育缺陷的分子机制;这项研究中,研究人员利用胚胎样和成体小鼠细胞培育出了囊胚样结构,将成体细胞置于化学溶液中就能刺激其转变成为诱导多能干细胞(iPSCs),随后其就能分化称为几乎机体任何一种类型的组织。为了促进ips细胞转化称为囊胚样结构,研究人员将其置于特殊的培养物中,他们希望能够观察到在受精卵转变成囊胚前,细胞是如何开始形成与发育阶段类似的结构的。
随着时间延续,连接细胞会开始在内外两层形成球状结构,这些细胞面对着内部积累的蛋白质,这就使其与外部细胞变得不同,而向外的细胞也会开始激活一种名为YAP的蛋白,该蛋白能进入到细胞核中开始诱导多种蛋白质进行表达,最终形成胎盘。这种特殊的囊胚样结构能够模拟胚胎天然的发育过程,其中含有在原始囊胚中相同的三种原始细胞类型,其能够表现出类似的基因表达特征,进一步研究表明,这些囊培养结构最终会进一步发育称为类似于植入后早期胚胎的结构。
7.Cell:新发现!科学家揭示癌症药物紫杉醇的作用机制!
doi:10.1016/j.cell.2019.05.035
当化疗手段刚刚被开发时,它的前体似乎相对简单,即通过阻断肿瘤细胞的增殖来抑制癌症进展,如今很多药物能通过不同的机制来发挥这样的作用,而且已经被证明仅能针对某些肿瘤患者有用;就以药物紫杉醇为例,其是一种用来治疗一系列癌症的化疗药物,该药物能干扰细胞分裂,但却无法在每一位患者机体中产生想要的效应,这表明,该药物的作用机制要比我们想象之中更为复杂。
近日,一项刊登在国际杂志Cell上的研究报告中,来自洛克菲勒大学的科学家们通过研究揭示了药物紫杉醇的工作机制,同时研究者还阐明了为何紫杉醇对某些癌细胞并没有作用;相关研究结果或能帮助开发新方法来预测哪些患者能因紫杉醇而获益,同时还有望帮助开发更多癌症新型个体化疗法。
暴露于紫杉醇的细胞会有两种选择,其会通过一种称为“滑脱”(slippage)的过程产生异常的子代细胞,或者直接死亡;研究者发现,当暴露于紫杉醇后,高水平cGAS的细胞往往更易于通过细胞凋亡过程而死亡,相比之下,缺乏cGAS的细胞则会通过进入滑脱过程而在疗法中存活下来,这种对化学物质反应的差异性或许具有重要的医学研究意义。
研究者分析了紫杉醇在治疗小鼠肿瘤中的有效性,当携带cGAS分子时,肿瘤就会减缓生长速度,但在遗传修饰并不携带cGAS的肿瘤中,紫杉醇似乎并不会对肿瘤产生任何效应。随后研究者在接受紫杉醇或其它类似化合物治疗的非小细胞肺癌患者中分析了cGAS的活性水平,结果发现,相比低水平cGAS的患者而言,高水平cGAS的患者对药物的反应更好一些,而且研究者也并未在接受紫杉醇治疗的患者中观察到cGAS的水平与生存率之间的关联。
8.Cell:新方法纯化出高纯度的细胞类型
doi:10.1016/j.cell.2019.08.006
在一项新的研究中,荷兰胡布勒支研究所的Alexander van Oudenaarden及其团队开发出一种称为GateID的方法,该方法能够在不使用抗体或报告基因的情形下从组织中纯化出感兴趣的细胞类型。GateID允许科学家们分离出多种细胞类型,比如干细胞,以便对它们进行更详细的研究。相关研究结果发表在2019年10月3日的Cell期刊上,论文标题为“Cell Type Purification by Single-Cell Transcriptome-Trained Sorting”。
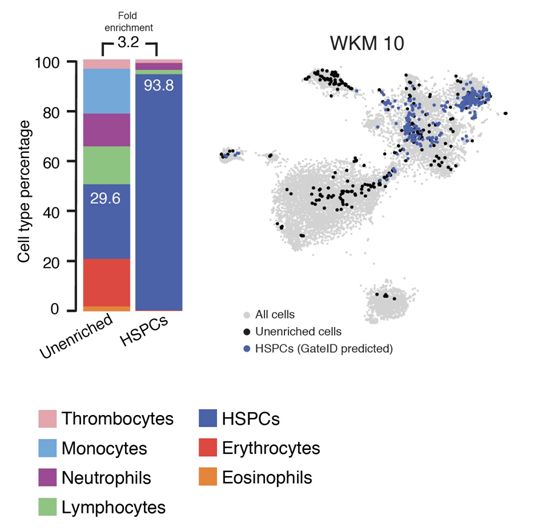
这些研究人员开发了一种新工具GateID,该工具可以仅根据细胞的天然特征(比如形状,大小和粒度)纯化细胞类型,这些天然特征可以通过流式细胞仪进行测量。这种新方法可以纯化感兴趣的细胞类型,而不必选择基因改造生物或市场上销售的抗体。
来自细胞内部和外部的GateID信息。首先,研究人员通过从所选择的器官或组织中收集单个细胞来产生数据集。对于每个细胞,对这些细胞的天然特征(它们从外面看起来的样子)和它们的特定基因表达谱(它们在内部的特征)都进行测量。然后,这些研究人员通过它们的基因表达谱来鉴定每个细胞所属的细胞类型。接着,他们将这些天然特征与鉴定出的细胞类型相偶联在一起。接下来,GateID能够选择最佳的天然特征,以在许多后续实验中纯化所需的细胞类型。他们发现GateID可以将几种细胞类型分离到较高的纯度。
9.Cell:首次发现针对III型CRISPR-Cas系统的蛋白抑制剂
doi:10.1016/j.cell.2019.09.003
在一项新的研究中,来自丹麦哥本哈根大学的研究人员发现一种针对III型CRISPR/Cas系统的抑制剂--- AcrIIIB1,它是由硫化叶菌病毒(Sulfolobus virus)SIRV2编码的。AcrIIIB1仅抑制由辅助蛋白Csx1的RNase活性介导的III-B CRISPR/Cas免疫反应。相关研究结果发表在2019年10月3日的Cell期刊上,论文标题为“Inhibition of Type III CRISPR-Cas Immunity by an Archaeal Virus-Encoded Anti-CRISPR Protein”。
这些研究人员发现AcrIIIB1似乎并不结合Csx1,但是与两种不同的III-B效应复合物--- Cmr-α和Cmr-γ相互作用。当结合前间隔序列转录本时,这两种III-B效应复合物合成环化寡腺苷酸(cyclic oligoadenylate, cOA),所产生的cOA激活Csx1的RNase活性。
综上所述,这些研究人员推断AcrIIIB1通过干扰一种Csx1 RNase相关过程来抑制III-B CRISPR/Cas免疫反应。
10.Cell:黑色素瘤的异质性阻碍了有效的免疫反应
doi:10.1016/j.cell.2019.08.032
至少癌细胞之间的多样性不是一件好事。在一项新的研究中,来自以色列魏茨曼科学研究所和美国国家癌症研究所等研究机构的研究人员发现在黑色素瘤中,如果肿瘤中的细胞能够分化为更加多样化的亚型,那么它就不太可能受到免疫系统的影响,这就降低了免疫疗法发挥疗效的机会。这些研究结果可能为设计针对癌症患者的个性化治疗方案提供了更好的工具,并且为研发抗癌疫苗指明了新的途径。相关研究结果近期发表在Cell期刊上,论文标题为“UVB-Induced Tumor Heterogeneity Diminishes Immune Response in Melanoma”。
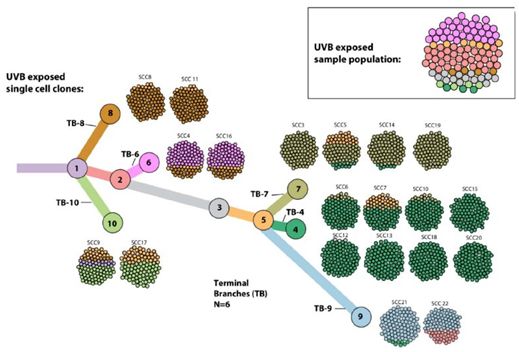
论文共同作者Osnat Bartok说,“我们展示了两个极端---高度同质性肿瘤和高度异质性肿瘤---之间的差异,但大多数癌症介于这两者之间。为了系统地产生具有中等水平遗传异质性的肿瘤,我们构建出亲本异种系的系统发育树,并绘制出随时间推移不同的细胞亚型是如何出现的。然后,我们基于这种系统发育树构建出同质性细胞系的‘混合物’,在体外培养过程中或多或少地会出现异质性,并将它们注射到小鼠体内。”如预料的那样,细胞混合物形成的肿瘤具有更高的同质性,小鼠的免疫系统就更容易根除癌症,然而,所形成的肿瘤具有更高的异质性,它们就变得更具侵袭性。
论文共同通讯作者、魏茨曼科学研究所分子细胞生物学系的Yardena Samuels说:“我们发现,测试细胞亚型的数量及其在系统发育树中的位置要比突变负担更好地预测免疫疗法是否取得成功。我们还分析了接受过免疫治疗的黑色素瘤患者的数据,发现这些因素与这种治疗的成功之间存在高度相关性。最终,我们打算使用我们构建的这种实验性系统来开发出适用于癌症患者的个性化治疗方案。”(生物谷 Bioon.com)
1.Cell:开发出光学混合筛选技术,可在几天内筛选人细胞中的数千个基因
doi:10.1016/j.cell.2019.09.016
如今,在一项新的研究中,来自美国麻省理工学院和布罗德研究所的研究人员开发出一种方法,该方法将大规模混合筛选与基于图像的细胞行为分析相结合。这种称为光学混合筛选(optical pooled screen)的方法允许人们在空间和时间分辨率下研究基因如何影响细胞过程,而其他的混合筛选方法则无法做到这一点。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“Optical Pooled Screens in Human Cells”。论文通讯作者为布罗德研究所核心研究所成员、麻省理工学院生物工程系副教授Paul Blainey博士。论文第一作者为Blainey 实验室博士后研究员Avtar Singh和Blainey 实验室物前理学博士生David Feldman。基因编辑大牛张锋(Feng Zhang)也是这篇论文的共同作者。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.09.016。
Singh说,“通过这种新方法,任何人都可以在无需专门设备的情况下使用显微镜在几天内筛查数千个基因。”
这些研究人员通过对数百万个细胞中一种称为p65的蛋白的细胞位置进行成像,研究了952个基因对一种称为NF-kB的免疫调节复合物的信号转导活性的影响。他们发现了两个基因---MED12和MED24---在NFkB信号弛豫过程中的新作用。
2.Cell:从拓扑学角度揭示DNA复制之谜
doi:10.1016/j.cell.2019.09.034
生命分子存在缠绕的现象。但是,DNA双螺旋中那两条熟悉的链是如何在没有缠绕的情况下成功复制的,这就很难解释了。在一项新的研究中,来自美国康奈尔大学的研究人员从拓扑学角度解决了这个问题。他们研究了这种双螺旋形状对DNA复制的影响。通过使用真核生物作为模型系统,他们发现染色质(由DNA、组蛋白和非组蛋白等成分组成)的内在机械性能决定着染色质纤维如何缠绕。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“Synergistic Coordination of Chromatin Torsional Mechanics and Topoisomerase Activity”。
在DNA复制过程--复制体(replisome)将两条DNA链分开并向前移动---中,DNA也必须绕双螺旋轴缠绕。这会让DNA承受很大的扭转应力(torsional stress),从而导致DNA发生额外的扭曲。问题在于:额外的扭曲在哪里发生?如果额外的扭曲仅发生在复制体的正面,那么两个子DNA分子将不会缠绕在一起,因此它们可以分开。但是,如果额外的扭曲发生在复制体的背面,那么两个子DNA分子将缠绕在一起,无法分开。这将为细胞分裂过程中的染色体分离创造一个主要问题,这可能导致DNA损伤并导致细胞死亡或癌症。
这些研究人员发现,缠绕单条染色质纤维比缠绕双条染色质纤维要容易得多。这意味着额外的扭曲将优先发生在复制体的正面,从而让两个子DNA分子之间的缠绕最小化。在一个单独的实验中,他们发现,一种能解开双螺旋DNA的酶(拓扑异构酶II)强烈偏爱正面的单条染色质纤维。染色质机械性能和拓扑异构酶活性似乎以协同方式协调,以减少子DNA分子之间的缠绕。
3.Cell:重大进展!开发出比CAR-T细胞更安全、用途更广的cCAR-T细胞技术
doi:10.1016/j.cell.2019.10.002
在一项新的研究中,来自美国格拉斯通研究所和Xyphos生物科学公司(Xyphos Biosciences, Inc.)的研究人员描述了一种攻击被HIV感染的细胞的新技术。这种新技术是CAR-T细胞免疫疗法的一种新的改进版本。近年来,这种疗法因在抵抗血癌上取得的成功而闻名于世。通过改进使得它具有更大的覆盖范围和多功能性,这种称为convertibleCAR T细胞(cCAR-T)的新技术在多个治疗领域显示出了巨大的前景,特别是在抗击HIV方面,这是因为它可以用来缩小在接受抗逆转录病毒疗法(ART)期间HIV感染者体内持续存在的受感染细胞的库存量。相关研究结果于2019年10月24日在线发表在Cell期刊上,论文标题为“Attacking Latent HIV with convertibleCAR-T Cells, a Highly Adaptable Killing Platform”。论文通讯作者为格拉斯通研究所HIV治愈研究中心主任Warner C. Greene博士。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.10.002。
人们已证实传统的CAR-T细胞在诱导血癌(比如淋巴瘤和儿童白血病)缓解方面非常成功。但是作为抵抗HIV感染的疗法,传统的CAR-T细胞并不完美。论文第一作者、Greene实验室科学家Eytan Herzig说,“传统的CAR-T细胞的一些缺点是它们经过基因改造后靶向癌细胞表面上的单个分子,而且一旦被注射到患者体内,无法对它们进行控制。”
Xyphos生物科学公司通过从细胞毒杀伤细胞中分离出靶向抗体克服了这些缺陷。该公司首席科学家David W. Martin博士解释说:“我们对cCAR-T细胞进行了基因改造,使得这些T细胞可以在其表面上表达受到少量修饰的人类受体蛋白NKG2D。”这种受到修饰的NKG2D受体当与它的搭档结合时,可以将这些T细胞变成有效的杀手。它的搭档是一种叫做MIC-A的蛋白质,Xyphos生物科学公司的科学家对它进行了裁剪和修饰,使得它可以与cCAR-T细胞表面上这种经过修饰的NKG2D受体特异性结合。这些科学家随后将它与靶向抗体的底部融合在一起,从而构建出他们称为MicAbody的产物。因此,这种靶向性MicAbody紧密地和唯一地结合cCAR-T细胞。
为了清除潜伏性HIV病毒库,Herzig和Greene一直在实验室中测试称为广泛中和抗体(bNAb)的抗HIV抗体。他们与Xyphos生物科学公司的科学家合作,基于bNAb构建出MicAbody(称为Mic-bNAb),并在各种实验室分析中测试了cCAR-T细胞和Mic-bNAb的组合使用。
在实验室中,Herzig以感染了各种HIV毒株的多种CD4 T细胞(HIV的天然靶标)为研究对象测试了这些组合。特别是,他使用了源自人类扁桃体的细胞制剂;已知在HIV感染者中,扁桃体T细胞是潜伏性HIV病毒库。他想确保cCAR-T/Mic-bNAb组合使用能杀死代表潜伏性HIV病毒库的T细胞类型。
结果是显著的:cCAR-T细胞与Mic-bNAb的组合使用特异性地杀死了受到感染的CD4 T细胞,但未杀死未感染的细胞。它们仅与Mic-bNAb组合使用时才杀死受感染的细胞,然而,不论是单独使用还是与不靶向HIV的MicAbody组合使用都没有这种效果。他们杀死了在实验室中感染了多种HIV毒株的CD4 T细胞。当与靶向HIV的Mic-bNAb和靶向癌细胞的MicAbody组合使用时,cCAR-T细胞可以有效杀死在相同细胞培养物中混合在一起的癌细胞和受到HIV感染的细胞。换句话说,cCAR-T细胞精确地证明了它旨在实现的多功能性和特异性。
最后,Herzig和Greene测试了cCAR-T/Mic-bNAb平台是否可以攻击接受ART治疗的HIV感染者血液中存在的潜伏性HIV病毒库。为了让这些细胞对cCAR-T细胞可见,他们首先用强效的称为“潜伏逆转剂(latency-reversing agent)”的化合物活化这些细胞培养物。在接触后48小时内,一半以上活化的表达HIV靶抗原的细胞被清除。Greene总结道,“这个平台前景广阔。”
4.Cell:开发出BARseq技术,构建出更好的大脑图谱
doi:10.1016/j.cell.2019.09.023
美国冷泉港实验室Anthony Zador教授及其团队一直在研究大脑回路如何介导和控制复杂的行为,在10年前就着手绘制大脑功能的三个支柱:连接性、基因表达和生理活性。由于尚无有效地做到这一点的技术,他的团队开发出MAPseq,即一种用来绘制不同脑细胞之间的连接图谱并更好地了解它们彼此之间如何相互作用的技术。多年来,Zador和他的实验室持续地改进这种技术。
在一项新的研究中,在博士后研究员Xiaoyin Chen的领导中,Zador实验室介绍了下一代的MAPseq技术:BARseq。这种新技术可用于通过精确地指出神经元所在的位置来扩展大脑图谱。这使得BARseq不仅可以确定神经元的连接,还可以确定其基因表达模式和生理活性,这是MAPseq不能解决的两个难题。相关研究结果发表在2019年10月17日的Cell期刊上,论文标题为“High-Throughput Mapping of Long-Range Neuronal Projection Using In Situ Sequencing”。
这些研究人员使用BARseq绘制了小鼠大脑听觉皮层中3579个神经元的连接图谱。将连接性模式与基因表达相匹配,可使科学家们表征不同的细胞类型并确定其在大脑中的特定功能。这将被证明是研究神经回路如何形成的一种有价值的工具。
5.Cell:有趣!雄性和雌性小鼠大脑中或存在不同类型的脑细胞!
doi:10.1016/j.cell.2019.09.020
近日,一项刊登在国际杂志Cell上的研究报告中,来自加州理工学院等机构的科学家们通过在雄性小鼠中发现了罕见的大脑细胞类型,同时在雌性小鼠中也发现了另外一种特殊类型的大脑细胞,这些存在于大脑特殊区域的性别特异性细胞在控制攻击性和交配行为上扮演着非常关键的角色。

图片来源:CC0 Public Domain。
下丘脑是包括人类在内所有脊椎动物大脑中的一个特殊区域,此前研究表明,下丘脑中特殊的解剖区域(VMHvl,腹内侧下丘脑腹外侧区域)含有能控制机体攻击性和交配行为的细胞;在这些研究中,对雄性和雌性小鼠大脑中的神经元进行强烈刺激或能促进小鼠变得更具攻击性(即使没有任何威胁),然而,微弱的刺激则会促进小鼠开始交配行为。
这项研究中,研究人员通过研究分析了VMHvl区域中单个细胞中的基因表达情况,利用先进的转录组学技术,研究人员就能识别出细胞中含有的RNA转录物,他们能利用这些信息来识别不同的细胞类型。此前研究中,研究人员分析了每个细胞中10%的转录物,而本文研究中,研究者则对大部分RNA转录组进行了分析,他们发现,这一小块区域中含有17种不同类型的大脑细胞,更重要的是,党对基因表达模式进行分析后,研究者发现,相比雌性小鼠而言,雄性小鼠机体中的这17种细胞类型更为丰富,而其它细胞类型则在雌性小鼠机体中更为丰富。
6.Cell:科学家阐明受精卵早期发育的分子机制 有望理解生命起源的奥秘
doi:10.1016/j.cell.2019.09.029
尽管从学校毕业、找到人生第一份工作和结婚可能是人生中重要的事情,但一些最重要的事情往往发生地更早,即在精子与卵子结合、细胞开始分裂的最初几天里。受精卵前100个细胞(囊胚)的组织方式对于妊娠是否成功、器官形成甚至以后对个体疾病(比如阿尔兹海默病等)的发生都有着非常深远的影响;然而,截止到目前为止,研究人员并没有找到一个好的方法来模拟囊胚形成的方式。
近日,一项刊登在国际杂志Cell上的研究报告中,来自索尔克研究所等机构的科学家们通过研究首次从单个培养的细胞创造出了小鼠囊胚样结构,这一过程绕过了研究者对自然胚胎的需求。这些囊胚样结构拥有和天然胚泡相同的结构,其甚至能植入到子宫中,这或许就有望帮助研究人员研究人类机体发育、怀孕及不孕等健康问题。
本文研究或有望帮助研究者深入探索早期发育缺陷的分子机制;这项研究中,研究人员利用胚胎样和成体小鼠细胞培育出了囊胚样结构,将成体细胞置于化学溶液中就能刺激其转变成为诱导多能干细胞(iPSCs),随后其就能分化称为几乎机体任何一种类型的组织。为了促进ips细胞转化称为囊胚样结构,研究人员将其置于特殊的培养物中,他们希望能够观察到在受精卵转变成囊胚前,细胞是如何开始形成与发育阶段类似的结构的。
随着时间延续,连接细胞会开始在内外两层形成球状结构,这些细胞面对着内部积累的蛋白质,这就使其与外部细胞变得不同,而向外的细胞也会开始激活一种名为YAP的蛋白,该蛋白能进入到细胞核中开始诱导多种蛋白质进行表达,最终形成胎盘。这种特殊的囊胚样结构能够模拟胚胎天然的发育过程,其中含有在原始囊胚中相同的三种原始细胞类型,其能够表现出类似的基因表达特征,进一步研究表明,这些囊培养结构最终会进一步发育称为类似于植入后早期胚胎的结构。
7.Cell:新发现!科学家揭示癌症药物紫杉醇的作用机制!
doi:10.1016/j.cell.2019.05.035
当化疗手段刚刚被开发时,它的前体似乎相对简单,即通过阻断肿瘤细胞的增殖来抑制癌症进展,如今很多药物能通过不同的机制来发挥这样的作用,而且已经被证明仅能针对某些肿瘤患者有用;就以药物紫杉醇为例,其是一种用来治疗一系列癌症的化疗药物,该药物能干扰细胞分裂,但却无法在每一位患者机体中产生想要的效应,这表明,该药物的作用机制要比我们想象之中更为复杂。
近日,一项刊登在国际杂志Cell上的研究报告中,来自洛克菲勒大学的科学家们通过研究揭示了药物紫杉醇的工作机制,同时研究者还阐明了为何紫杉醇对某些癌细胞并没有作用;相关研究结果或能帮助开发新方法来预测哪些患者能因紫杉醇而获益,同时还有望帮助开发更多癌症新型个体化疗法。
暴露于紫杉醇的细胞会有两种选择,其会通过一种称为“滑脱”(slippage)的过程产生异常的子代细胞,或者直接死亡;研究者发现,当暴露于紫杉醇后,高水平cGAS的细胞往往更易于通过细胞凋亡过程而死亡,相比之下,缺乏cGAS的细胞则会通过进入滑脱过程而在疗法中存活下来,这种对化学物质反应的差异性或许具有重要的医学研究意义。
研究者分析了紫杉醇在治疗小鼠肿瘤中的有效性,当携带cGAS分子时,肿瘤就会减缓生长速度,但在遗传修饰并不携带cGAS的肿瘤中,紫杉醇似乎并不会对肿瘤产生任何效应。随后研究者在接受紫杉醇或其它类似化合物治疗的非小细胞肺癌患者中分析了cGAS的活性水平,结果发现,相比低水平cGAS的患者而言,高水平cGAS的患者对药物的反应更好一些,而且研究者也并未在接受紫杉醇治疗的患者中观察到cGAS的水平与生存率之间的关联。
8.Cell:新方法纯化出高纯度的细胞类型
doi:10.1016/j.cell.2019.08.006
在一项新的研究中,荷兰胡布勒支研究所的Alexander van Oudenaarden及其团队开发出一种称为GateID的方法,该方法能够在不使用抗体或报告基因的情形下从组织中纯化出感兴趣的细胞类型。GateID允许科学家们分离出多种细胞类型,比如干细胞,以便对它们进行更详细的研究。相关研究结果发表在2019年10月3日的Cell期刊上,论文标题为“Cell Type Purification by Single-Cell Transcriptome-Trained Sorting”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.08.006。
这些研究人员开发了一种新工具GateID,该工具可以仅根据细胞的天然特征(比如形状,大小和粒度)纯化细胞类型,这些天然特征可以通过流式细胞仪进行测量。这种新方法可以纯化感兴趣的细胞类型,而不必选择基因改造生物或市场上销售的抗体。
来自细胞内部和外部的GateID信息。首先,研究人员通过从所选择的器官或组织中收集单个细胞来产生数据集。对于每个细胞,对这些细胞的天然特征(它们从外面看起来的样子)和它们的特定基因表达谱(它们在内部的特征)都进行测量。然后,这些研究人员通过它们的基因表达谱来鉴定每个细胞所属的细胞类型。接着,他们将这些天然特征与鉴定出的细胞类型相偶联在一起。接下来,GateID能够选择最佳的天然特征,以在许多后续实验中纯化所需的细胞类型。他们发现GateID可以将几种细胞类型分离到较高的纯度。
9.Cell:首次发现针对III型CRISPR-Cas系统的蛋白抑制剂
doi:10.1016/j.cell.2019.09.003
在一项新的研究中,来自丹麦哥本哈根大学的研究人员发现一种针对III型CRISPR/Cas系统的抑制剂--- AcrIIIB1,它是由硫化叶菌病毒(Sulfolobus virus)SIRV2编码的。AcrIIIB1仅抑制由辅助蛋白Csx1的RNase活性介导的III-B CRISPR/Cas免疫反应。相关研究结果发表在2019年10月3日的Cell期刊上,论文标题为“Inhibition of Type III CRISPR-Cas Immunity by an Archaeal Virus-Encoded Anti-CRISPR Protein”。
这些研究人员发现AcrIIIB1似乎并不结合Csx1,但是与两种不同的III-B效应复合物--- Cmr-α和Cmr-γ相互作用。当结合前间隔序列转录本时,这两种III-B效应复合物合成环化寡腺苷酸(cyclic oligoadenylate, cOA),所产生的cOA激活Csx1的RNase活性。
综上所述,这些研究人员推断AcrIIIB1通过干扰一种Csx1 RNase相关过程来抑制III-B CRISPR/Cas免疫反应。
10.Cell:黑色素瘤的异质性阻碍了有效的免疫反应
doi:10.1016/j.cell.2019.08.032
至少癌细胞之间的多样性不是一件好事。在一项新的研究中,来自以色列魏茨曼科学研究所和美国国家癌症研究所等研究机构的研究人员发现在黑色素瘤中,如果肿瘤中的细胞能够分化为更加多样化的亚型,那么它就不太可能受到免疫系统的影响,这就降低了免疫疗法发挥疗效的机会。这些研究结果可能为设计针对癌症患者的个性化治疗方案提供了更好的工具,并且为研发抗癌疫苗指明了新的途径。相关研究结果近期发表在Cell期刊上,论文标题为“UVB-Induced Tumor Heterogeneity Diminishes Immune Response in Melanoma”。

根据肿瘤细胞的异质性,绘制出它们的系统发育树,这能够让研究人员开展进一步的实验,图片Weizmann Institute of Science。
论文共同作者Osnat Bartok说,“我们展示了两个极端---高度同质性肿瘤和高度异质性肿瘤---之间的差异,但大多数癌症介于这两者之间。为了系统地产生具有中等水平遗传异质性的肿瘤,我们构建出亲本异种系的系统发育树,并绘制出随时间推移不同的细胞亚型是如何出现的。然后,我们基于这种系统发育树构建出同质性细胞系的‘混合物’,在体外培养过程中或多或少地会出现异质性,并将它们注射到小鼠体内。”如预料的那样,细胞混合物形成的肿瘤具有更高的同质性,小鼠的免疫系统就更容易根除癌症,然而,所形成的肿瘤具有更高的异质性,它们就变得更具侵袭性。
论文共同通讯作者、魏茨曼科学研究所分子细胞生物学系的Yardena Samuels说:“我们发现,测试细胞亚型的数量及其在系统发育树中的位置要比突变负担更好地预测免疫疗法是否取得成功。我们还分析了接受过免疫治疗的黑色素瘤患者的数据,发现这些因素与这种治疗的成功之间存在高度相关性。最终,我们打算使用我们构建的这种实验性系统来开发出适用于癌症患者的个性化治疗方案。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


