全球BCMA CAR-T细胞疗法!百时美施贵宝ide-cel治疗多发性骨髓瘤(MM)在欧盟进入加速评估!
来源:本站原创 2020-05-24 15:39
ide-cel是第一个提交监管审批针对BCMA靶点以及用于治疗MM的CAR-T细胞疗法,总缓解率(ORR)为73%,[严格]完全缓解率(sCR/CR)为33%。所有达到CR/sCR者均为MRD阴性。

2020年05月24日讯 /生物谷BIOON/ --百时美施贵宝(BMS)与合作伙伴蓝鸟生物(Bluebrid Bio)近日联合宣布,欧洲药品管理局(EMA)已受理idecabtagene vicleucel(ide-cel,bb2121)的营销授权申请(MAA)。EMA已确认MAA的完整性,并已启动集中审查程序。今年3月,ide-cel被EMA授予了加速评估资格,其MAA审查周期将缩短至150天。
ide-cel是一种研究性B细胞成熟抗原(anti-BCMA)导向的嵌合抗原受体(CAR)T细胞疗法,开发用于复发性/难治性多发性骨髓瘤(R/R MM)患者的治疗,具体为:用于既往接受至少三种疗法(包括免疫调节剂、蛋白酶体抑制剂、抗CD38抗体)的MM成人患者。
今年3月,BMS和蓝鸟生物向美国FDA提交了ide-cel用于相同适应症的生物制品许可申请(BLA)。但值得注意的是,今年5月中旬,FDA发布了一份拒绝受理通知书(refusal-to-file letter),拒绝受理BLA。经过初步审查后,FDA认为BLA中的化学、制造和控制(CMC)模块需要进一步细节来完成审查。但该机构没有要求提供额外的临床或非临床数据。BMS计划在2020年7月底之前重新提交BLA。
ide-cel监管申请文件基于关键II期KarMMa研究的结果。该研究中,128例先前接受过至少3种疗法且对最后一种疗法无效(根据国际骨髓瘤工作组[IMWG]的定义,治疗60天内对治疗无应答或病情进展)的过度预治疗(heavily pre-treated,即先前接受过多种疗法)复发和难治性多发性骨髓瘤患者接受了ide-cel剂量水平为150-450 x 10E6 CAR+ T细胞治疗。这些患者,先前接受过的治疗方案中位数为6种,84%的患者对所有三种常用治疗方案均难治,包括免疫调节剂(IMiD)、蛋白酶体抑制剂(PI)和抗CD38抗体;94%的患者对抗CD38抗体难治。中位随访时间为13.3个月。
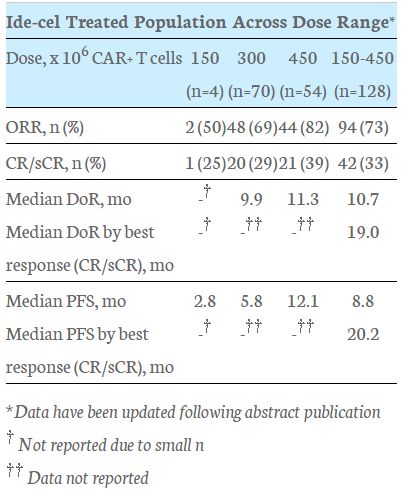
该研究研究达到了总缓解率(ORR)的主要终点和完全缓解率(CR)的关键次要终点。安全性结果与先前报道的ide-cel数据一致。数据显示:所有剂量水平的总缓解率(ORR)为73%,其中33%的患者获得完全缓解(CR)或严格缓解(sCR)。中位缓解持续时间(DoR)为10.7个月,有CR或sCR的患者中位DOR为19.0个月。中位无进展生存期(PFS)为8.8个月,有CR或sCR患者的中位PFS为20.2个月。所有达到CR或sCR且可评估最小残留病(MRD)的患者均为MRD阴性。
各亚组间观察到一致的临床意义的益处,几乎所有亚组的ORR均为50%或以上,包括老年和高危患者。总生存期(OS)数据继续趋于成熟,所有剂量水平的估计中值OS为19.4个月,12个月存活率为78%。结果支持ide-cel在150-450×10E6 CAR+T细胞的目标剂量水平上的有利风险预测。详细数据将在5月29日举行的美国临床肿瘤学会(ASCO)2020年虚拟科学项目上报告。
百时美施贵宝细胞疗法开发高级副总裁Stanley Franke医学博士表示:“欧洲是多发性骨髓瘤发病率最高的地区之一,病情复发且对标准治疗方案无效的患者需要新的治疗方案来改善预后。我们将继续与EMA合作,将ide-cel带给正在与这种侵袭性血癌作斗争的欧盟患者。”
ide-cel是第一个提交监管审批针对BCMA靶点以及用于治疗MM的CAR-T细胞疗法。BCMA是一种在多发性骨髓瘤(MM)癌细胞上广泛表达的蛋白质,这使其成为治疗这种侵袭性血液癌症的重要潜在靶点。
ide-cel的原理是在患者的T细胞上嵌合BCMA的受体,其制备过程为:从每例患者的血液中分离获得T细胞,使用编码BCMA抗原受体的慢病毒载体对T细胞进行修饰,使T细胞表面表达BCMA受体。治疗时,MM患者先接受2种化疗药物(环磷酰胺和氟达拉滨)预处理,以杀死患者体内现有的T细胞,随后输注bb2121,一旦输注回患者体内,ide-cel就开始寻找并杀死表达BCMA的细胞。
此前,ide-cel在2017年11月被美国FDA授予了治疗R/R MM的突破性药物资格(BTD),并且被欧盟EMA授予了治疗R/R MM的优先药物资格(PRIME)。
ide-cel是百时美施贵宝和蓝鸟生物共同开发、共同推广和利润分享协议的一部分。双方的ide-cel综合临床开发项目包括用于早期治疗MM的多项临床研究(KarMMa-2、KarMMa-3、KarMMa-4),包括新诊MM。
除了ide-cel之外,BMS和蓝鸟生物也正在开发第二代anti-BCMA CAR-T疗法bb2127,这是在第一代CAR-T疗法ide-cel基础上进一步开发的产品,结合了一种PI3K抑制信号,可生产出一种富集“记忆T细胞”的CAR-T产品,这是一种寿命更长、更强效的T细胞亚群,具有改善的抗肿瘤活性。
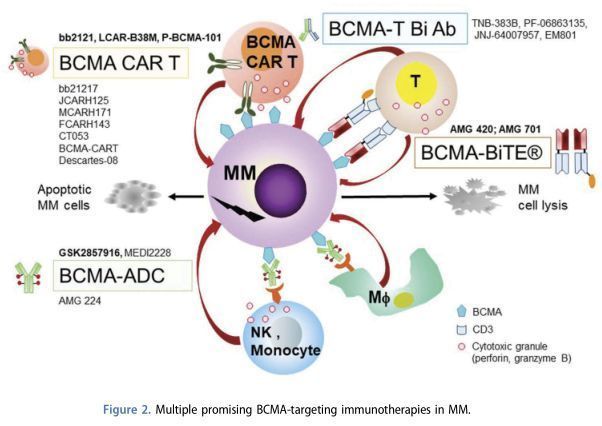
BCMA为靶点的在研MM免疫疗法(来源文献—PMID:31277554)
多发性骨髓瘤(MM)是仅次于非霍奇金淋巴瘤的第二大常见血液学恶性肿瘤。近年来,尽管在化疗、蛋白酶体抑制剂、免疫调节剂沙利度胺衍生物和CD38靶向抗体方面取得了很大的进展,但几乎所有患者最终仍会复发。因此,对新治疗方案存在着迫切需求。MM市场预计2027年将达到290亿美元。
BCMA是一种极其重要的B细胞生物标志物,广泛存在于MM细胞表面,近年来已成为MM和其他血液系统恶性肿瘤的一个非常热门的免疫治疗靶点。目前,针对BCMA开发的免疫疗法超过20种,主要分为3类:嵌合抗原受体T细胞疗法(CAR-T,BMS/蓝鸟生物、诺华为代表)、双特异性抗体(BsAb,安进为代表)、抗体药物偶联物(ADC,葛兰素史克为代表)。
今年1月和2月,葛兰素史克(GSK)B细胞成熟抗原(BCMA)靶向抗体药物偶联物(ADC)belantamab mafodotin(GSK2857916,2.5mg/kg剂量)分别获得了美国FDA的优先审查、欧盟EMA的加速评估,用于治疗既往已接受过多种疗法(包括一种免疫调节剂、一种蛋白酶体抑制剂、一种抗CD38抗体)的复发或难治性多发性骨髓瘤(R/R MM)患者。
belantamab mafodotin有潜力成为上市的首个BCMA靶向疗法。2017年,belantamab mafodotin获美国FDA授予突破性药物资格(BTD)以及欧盟EMA授予优先药物资格(PRIME),成为被授予BTD和PRIME的首个BCMA靶向制剂。
来自关键II期DREAMM-2研究的数据显示,在既往过度预治疗(接受过的治疗方案中位数:7种)的R/R MM患者中,belantamab mafodotin 2.5mg/kg剂量组的总缓解率(ORR)为31%(n=30/97),3.4mg/kg剂量组的ORR为34%(n=34/99),数据具有临床意义。来自DREAMM-1研究的数据显示,在BCMA阳性R/R MM患者中,belantamab mafodotin治疗的ORR达到了60%。(生物谷Bioon.com)
原文出处:European Medicines Agency Validates Bristol Myers Squibb’s applications for Idecabtagene Vicleucel (Ide-cel, bb2121)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



