药物机理研究盘点
来源:本站原创 2019-04-30 19:09
2019年4月30日讯/生物谷BIOON/---药物是用以预防、治疗及诊断疾病的物质。在理论上,药物是指凡能影响机体器官生理功能及细胞代谢活动的化学物质都属于药物的范畴,也包括避孕药。甚至,CAR-T细胞免疫疗法和干细胞疗法有时也按照药物加以管理。药物的作用机理多种多样,是不同药物分子与机体不同靶细胞间相互作用的结果。药物作用的性质首先取决于药物的化学结构,包括基本骨架、活性基团、侧链长短及立体构
2019年4月30日讯/生物谷BIOON/---药物是用以预防、治疗及诊断疾病的物质。在理论上,药物是指凡能影响机体器官生理功能及细胞代谢活动的化学物质都属于药物的范畴,也包括避孕药。甚至,CAR-T细胞免疫疗法和干细胞疗法有时也按照药物加以管理。
药物的作用机理多种多样,是不同药物分子与机体不同靶细胞间相互作用的结果。药物作用的性质首先取决于药物的化学结构,包括基本骨架、活性基团、侧链长短及立体构形等因素。这些结构-活性关系(structure-activity relationship)是药物化学研究的主要对象,也有助于加强人们对药物作用的理解。
影响药物的选择和应用的两个医学名词是药效学(药物对机体的作用)和药物动力学(机体对药物的作用)。除了探讨药物的作用(例如减轻疼痛、降低血压、降低血浆胆固醇水平)外,药物动力学还研究药物在什么部位和怎样发挥作用(即作用机制)。虽然药物作用比较容易显现,但其作用部位和机制不可能很快弄清楚。比如,阿片和吗啡用于镇痛和治疗抑郁已有几百年了,但仅仅是不久前才发现与镇痛欣快有关的大脑结构和脑化学成分。
药物必须到达发病部位才能起作用,这也是药代动力学的重要性所在。药物发挥作用时须在患部保持足够的量,但又不能产生严重不良反应,每个医生都知道选择正确剂量是一门复杂的平衡艺术。
许多药物通过血循环到达作用部位。药物显效时间和效应维持时间一般由该药进入血液的速度、进入量、清除的速度、肝脏代谢的效率以及被肾和肠道清除的速度所决定。
每个个体对药物的反应均有差异。为达到同一疗效,体重较重的人比较轻的人需要更多的药量。新生儿和老年人对药物的代谢慢于儿童和青年人。肝肾病患者对药物的清除亦比正常人困难。每种新药的标准剂量或平均剂量由动物试验和人的试验决定。但平均剂量表面上被定义为“适合所有人的剂量”,其实它只对一定范围的个体适用,并不完全适合每个个体。
药物体内过程因人而异,许多因素可影响药物的吸收、分布、代谢、排泄,从而影响最终的药效。其他一些因素也可影响药物的作用,如遗传、药物间的相互作用、疾病等。
遗传可影响药物的代谢过程。由于遗传差异,有些人代谢药物的速度慢,药物易蓄积并引起中毒,有些人代谢药物速度快,药物在体内不易达到有效浓度。遗传还可影响药物代谢的其他方面,比如:常用剂量下药物代谢速度正常,当药物剂量过高或和另一同类药物合用时,超过其代谢能力会导致药物蓄积中毒。
此外,当两种药物同时使用(药-药相互作用)或食用某些食物(药-食物相互作用),该药的作用可被其影响,称为药物的相互作用。尽管联合用药有时是有益的,但多数时候是无益的甚至是有害的。药物相互作用可以增强或减弱药效或不良反应。药物的相互作用多发生在处方药,但有时也会出现在非处方药中,最常见的有阿司匹林、抗酸剂及抗凝药。药物相互作用的危险性取决于用药的种类、数量及剂量。许多作用是在药物研制过程中发现的,医护人员有医药知识可减少相互作用危害的发生。不考虑药物特点用药会增加其危险性。医护人员指导用药,如发生不良相互作用是由于医护人员对药物了解不够。
鉴于很多药物的作用机理比较复杂,哪怕是明星药和重磅炸弹药,它们的作用机理也并未得到深入理解。了解药物的作用机理,有助指导科学家们进行个人化用药,并对现有的药物进行结构优化,增强它们的疗效,同时降低它们的毒副作用,从而更好地造福人类。基于此,让我们梳理一下药物作用机理研究方面取得的进展,以飨读者。
1.Neuron:科学家阐明青蒿素发挥作用的分子机制
尽管抗疟疾药青蒿素已经被广泛使用了几个世纪了,但是人们仍然并不清楚青蒿素发挥作用的分子机制。在一项刊登在2019年2月20日的Neuron期刊上的研究中,来自德国维尔茨堡大学的研究人员阐明了青蒿素发挥作用的分子机制。

这些研究人员首次揭示了两种不同的青蒿素衍生物---青蒿琥酯和青蒿素甲醚---与桥尾蛋白(gephyrin)结合在一起时的晶体结构。通过结合抑制性的甘氨酸和GABAA受体,桥尾蛋白在哺乳动物中枢神经系统中能够扮演抑制性突触后中央支架蛋白的角色,而且人们已发现桥尾蛋白是青蒿素的一种靶蛋白。在这项研究中,他们阐明了青蒿素如何靶向作用于桥尾蛋白中通用的受体结合槽以及如何与抑制性神经递质受体竞争来重叠的结合位点;这些研究结果或能作为一种有效的工具帮助科学家们理解人类大脑的生理学特性。
这些研究人员表示,将晶体学结构、生物化学、电生理学及相关数据进行结合,他们就能开发出受青蒿素抑制神经递质调控的综合模型,而这种模型就能清楚地描述蛋白质和药物之间的相互作用。
2.Sci Signal:科学家揭示CAR-T细胞发挥抗癌疗效的分子机制
在过去十年中,一种新型的抗癌疗法---免疫疗法---取得了巨大的成功,这是一种通过激活人体自身免疫系统来攻击癌细胞的疗法。其中的一种免疫疗法称为嵌合抗原受体(CAR)T细胞(CAR-T细胞)免疫疗法,已经在某些癌症病人身上取得了喜人的疗效,而两种CAR-T细胞免疫疗法(Kymriah和Yescarta)已经被美国FDA批准用于治疗急性成淋巴细胞性白血病和大B细胞淋巴瘤。尽管取得了如此巨大的成功,但是科学家们仍然没有完全搞清楚CAR-T细胞发挥功能的机制。如今,在一项新的研究中,来自美国莫菲特癌症研究中心的研究人员解决了这个问题,并阐明了CAR T细胞发挥作用的具体机制,相关研究成果发表在2019年2月12日的Science Signaling期刊上。
CAR-T细胞免疫疗法是一种独特的免疫疗法:首先收集和分离患者血液中的T细胞,在实验室中对分离后的T细胞进行仅修饰,从而给它们添加一种CAR的特殊受体用于识别癌细胞。这些经过基因修饰的T细胞会在体外进行培养和增殖,最后被灌注回相同的患者体内。
对T细胞中进行基因修饰已经被多个课题组加以优化以让它们发挥最佳的抗癌免疫反应。其中一个被插入到T细胞中的基因是T细胞受体(CD3ζ)的一部分,此外还包括其他的共刺激分子,最新的第三代CAR还包括了多个共刺激分子受体。但是一些研究表明嵌入多个共刺激分子受体并没有让第三代CAR-T细胞的疗效增强。此外,其它的基因修饰则聚焦于CAR受体的结构设计,比如将CAR受体结合在细胞表面上的区域。但是迄今为止,人们都还不清楚这些不同的基因修饰和结构设计会对生物学信号及T细胞反应产生怎样的影响。
考虑到CAR-T细胞免疫疗法的应用越来越广泛,这些研究人员认为理解这些疗法在病人体内发挥作用的具体机制至关重要。为了更好地理解CAR-T细胞如何发挥效应,他们使用了一系列基于蛋白组学的手段去比较靶向癌细胞上相同分子但是胞内设计和抗癌活性不同的CAR-T细胞。他们发现第二代和第三代CAR受体可以结合一系列分子,其中的一些分子甚至具有相反的功能。重要的是,只有第二代CAR受体能够刺激类似于自然版本的CD3ζ的表达。他们发现第二代CAR受体的这个活性依赖于胞内区域的结构设计,而与共刺激分子受体或者结合区域的结构无关。此外,通过详细的磷酸蛋白组学分析,他们发现与第三代CAR受体相比,第二代CAR受体能够更有效地激活下游信号分子。
这些结果表明第二代CAR受体可以激活其它来源的CD3信号,这也许导致了更强烈的信号和更有效的抗癌效应。通过系统分析与CAR受体相互作用的信号蛋白及不同CAR受体结构激活的信号通路,这些研究人员能够提供新工具用于开发功能更可控的新CAR受体。
3.FASEB J:揭示二甲双胍治疗2型糖尿病的新作用机制
几十年来,二甲双胍(metformin)一直是治疗2型糖尿病的一线药物,通过抑制肝脏中的葡萄糖产生来降低血糖水平。二甲双胍还可改善肌肉组织中的葡萄糖摄取和使用。二甲双胍对肝脏中的葡萄糖产生的影响很可能是通过线粒体呼吸链传递的。然而,这种药物增加肌肉组织中葡萄糖摄取的机制仍然是不清楚的。
如今,在一项新的研究中,芬兰赫尔辛基大学的Sanna Lehtonen教授及其团队在细胞培养物和动物模型中证实二甲双胍直接结合到脂质磷酸酶SHIP2上,降低它的活性。SHIP2活性的降低增加了肌肉细胞中的葡萄糖摄取并减少了足细胞或肾小球上皮细胞中的细胞死亡。相关研究结果发表在2019年2月的FASEB Journal期刊上。
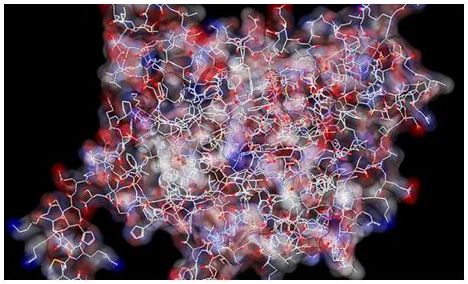
脂质磷酸酶SHIP2抑制胰岛素信号通路。之前的研究已通过动物模型证实患有糖尿病的个体在其肾脏、肌肉和脂肪组织中具有升高的SHIP2水平。这降低了组织对胰岛素信号作出反应并降低其葡萄糖摄取的能力。升高的SHIP2浓度也增加足细胞的程序性细胞死亡。除动物模型外,Lehtonen团队还在研究中使用了患者样本。他们的分析显示在未服用二甲双胍的2型糖尿病患者中,肾脏中的SHIP2活性升高了,此外足细胞丢失是显著的。在服用二甲双胍的患者中,肾脏中的SHIP2活性与非糖尿病患者中的一样,而且足细胞丢失也低于使用其他药物治疗的患者。
Lehtonen说,“我们的研究结果表明脂质磷酸酶SHIP2在调节足细胞中的葡萄糖代谢和细胞死亡中具有重要作用。因此,用二甲双胍或其他合适的药物调节SHIP2活性对于控制2型糖尿病尤其是预防相关的糖尿病肾病至关重要。”
二甲双胍的作用机制正在受到积极的研究,这是因为它对身体具有多种影响,这就使得它可能有助于治疗除糖尿病之外的疾病。更好地理解它的作用机制还有助于利用这种药物精确地治疗从中受益的患者群体。
4.Science:揭示为何氯胺酮是一种抗抑郁药
在一项新的研究中,来自日本东京大学、美国斯坦福大学和威尔康乃尔医学院的研究人员在小鼠中鉴定出氯胺酮(ketamine)诱导的大脑相关变化有助于维持与抑郁症有关的行为的缓解,这一发现可能有助于人们开发出促进人类抑郁症持续缓解的干预措施。相关研究结果发表在2019年4月12日的Science期刊上,论文标题为“Sustained rescue of prefrontal circuit dysfunction by antidepressant-induced spine formation”。
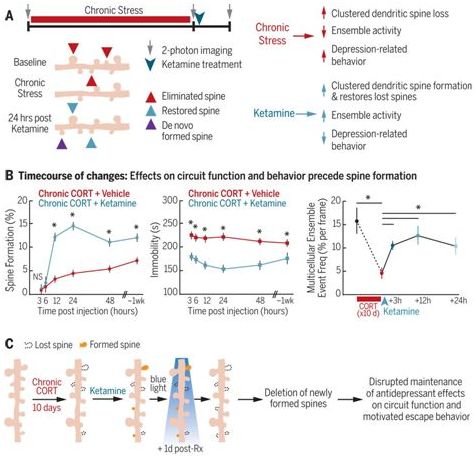
为了理解人体中从抑郁症发作到缓解转变背后的机制,这些研究人员在小鼠中研究了与抑郁相关的行为。在小鼠经历应激源之前和之后,他们获得了它们的前额叶皮质中的树突棘(dendritic spine)的高分辨率图像。树突棘是神经元中接收来自其他神经元的通信输入的突起。他们发现相比于没有暴露于应激源中的小鼠,显示出与抑郁有关的行为的小鼠在其前额皮质中的树突棘消除增加了和树突棘形成减少了。这一发现复制了之前开展的将与小鼠中抑郁相关的行为的出现与树突棘损失相关联在一起的研究。
除了对树突棘的影响外,应激还降低了小鼠前额叶皮质中神经元的功能性连接和同时活动。这种连接性和活动性的降低与应对应激源的抑郁症相关行为有关。Liston及其团队随后发现氯胺酮治疗快速恢复了神经元的功能连接和整体活动,并且消除了与抑郁有关的行为。相比于遭受应激但未接受氯胺酮治疗的小鼠,在接受单剂量氯胺酮治疗24小时后,遭受应激的小鼠表现出与抑郁相关的行为逆转和树突棘形成的增加。这些新的树突棘是功能性的,因而与其他神经元建立了工作上的关联性。
这些研究人员发现尽管小鼠的行为改变和神经活动变化发生很快(在接受氯胺酮治疗3小时后),但是树突棘的形成发生得更慢(在氯胺酮治疗12~24小时后)。虽然还需开展进一步的研究,但是他们认为这些发现可能表明树突棘再生是氯胺酮诱导的前额皮质回路活动恢复的结果。
5.Nature:迷幻剂MDMA可能有助治疗创伤后应激障碍
神经系统对特定环境刺激明显敏感的发育时期是一个关键时期,在这个时期,这些特定环境刺激是正确的神经回路形成和学习所必需的。对关键时期进行机制上的表征已揭示出活跃的大脑可塑性在早期发育期间的重要作用,以及随着大脑发育成熟对这些机制施加约束的重要作用。在疾病状态中,关键时期的关闭限制了大脑的适应能力,即使在恢复到最佳条件时也是如此。因此,鉴定重新开启关键时期的操作一直是转化神经科学领域的一个重点。
在一项新的研究中,来自美国约翰霍普金斯大学和麻省理工学院的研究人员提供证据表明对催产素(oxytocin)在大脑伏核(nucleus accumbens)中介导的突触可塑性(长期抑郁)进行发育调节为社会奖励学习建立了一个关键时期。相关研究结果于2019年4月3日在线发表在Nature期刊上,论文标题为“Oxytocin-dependent reopening of a social reward learning critical period with MDMA”。
这些研究人员还发现单剂量的(+/−)-3,4-亚甲基二氧甲基苯丙胺(3,4-methylendioxymethamphetamine, MDMA)重新开启社会奖励学习的关键时期,并导致催产素依赖性长期抑郁症的化生性上调(metaplastic upregulation)。MDMA诱导的这一关键时期重新开启需要激活大脑伏核中的催产素受体,并通过刺激大脑伏核中的催产素末端得以重现。
由此可见,这些发现对于理解以社交障碍为特征的神经发育性疾病、以及对社会影响作出反应或由社会伤害引起的疾病的发病机制具有重要意义。
6.Nature:重大突破!老药二甲双胍和血红素组合有望治愈三阴性乳腺癌!
据估计,大约15%~20%的乳腺癌患者为三阴性乳腺癌患者,即患者机体缺失三种关键的治疗靶点:雌激素受体、孕激素受体和人类表皮生长因子受体2,由于缺少这些靶点,大部分三阴性乳腺癌患者都会接受标准化疗,而不是首选靶向性药物。
由于缺少治疗三阴性乳腺癌的有效疗法,因此很多科学家们都在奋力研究寻找新型的药物靶点。在一项新的研究中,来自美国芝加哥大学的研究人员就发现一对新型武器—两种古老的药物,当其对患癌小鼠进行治疗时能够产生令人鼓舞的结果,相关研究结果发表在2019年4月11日的Nature期刊上。这意味着能够通过组合使用这两种古老药物(二甲双胍和血红素)来治疗当前无法靶向治疗的耐受性乳腺癌。
这些研究人员发现,血红素最主要的抗癌靶点是一种名为BACH1的转录因子,该蛋白在三阴性乳腺癌中高度表达,而且其也是癌症转移所需要的关键蛋白;高水平的BACH1会引发患者预后不良,但庆幸的是,BACH1并不是必要的。BACH1能靶向作用线粒体代谢,通过结合特殊的DNA序列控制DNA的转录速率,从而抑制线粒体电子传递链的转录(细胞能量的关键来源),当BACH1水平较高时,这种能量来源就会被切断。
当利用血红素处理癌细胞时,BACH1的水平就会下降,从而就会促进BACH1剔除的癌细胞改变它们的代谢通路,同时还会促进对二甲双胍易感的癌症抑制癌细胞中的线粒体呼吸链,因此将二甲双胍与血红素组合使用就能有效抑制肿瘤的生长,这些研究人员随后在小鼠肿瘤模型中证实了这一点。
BACH1低水平的三阴性乳腺癌患者和高水平线粒体基因表达的患者很有可能单独对二甲双胍产生反应,而高水平BACH1和线粒体基因表达水平较低的癌症患者或许会对二甲双胍产生耐受性,而本文研究结果表明,在二甲双胍疗法基础上加入血红素疗法就能使得癌症患者对二甲双胍再次产生反应;此外,这些研究人员指出,BACH1能够作为线粒体代谢的关键调节因子,同时也是三阴性乳腺癌患者对二甲双胍是否产生反应的主要决定因子。
这些研究结果或许能够扩展到对乳腺癌以外的癌症进行研究,BACH1不仅在三阴性乳腺癌中表达水平较高,其还在很多癌症中会发生高水平表达,包括肺癌、肾癌等,BACH1抑制线粒体电子传递链似乎是一种常见的机制。在未来,这些研究人员还将深入研究阐明二甲双胍和血红素联合疗法治疗三阴性乳腺癌的分子机理。
7.Cell:抗高血压药物氨氯地平可治疗先兆子痫
在全世界,每20名女性中就有一人在怀孕期间患有先兆子痫(preeclampsia)。它会导致血压升高和肾脏停止运作。先兆子痫是怀孕期间最常见的死亡原因之一---无论是母亲还是未出生的孩子。当前还没有治疗这种疾病的方法。医生采取的阻止子痫(eclampsia)---一种危及生命的癫痫发作---的唯一方法是提早分娩。
在一项新的研究中,来自瑞士苏黎世联邦理工学院的研究人员揭示了在先兆子痫中,导致血管增厚和失去弹性的信号通路。他们开发出的一种治疗方法能够治疗患有先兆子痫的孕妇。相关研究结果发表在2019年1月10日的Cell期刊上,论文标题为“Beta-Arrestin1 Prevents Preeclampsia by Downregulation of Mechanosensitive AT1-B2 Receptor Heteromers”。论文通讯作者为苏黎世联邦理工学院分子药理学教授Ursula Quitterer博士。
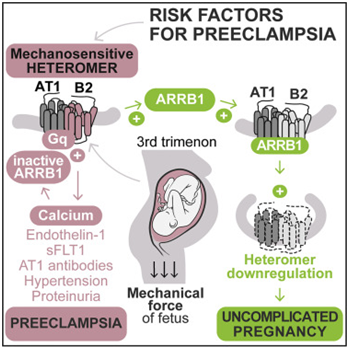
这项研究着重关注聚集在一起的两种G蛋白偶联受体(血管紧张素II AT1和血管舒缓激肽B2),即AT1-B2异源二聚体。它们不仅对激素冲动作出反应,而且还对机械刺激作出反应,从而触发信号级联反应在血管细胞内部发生,并从根本上改变这些细胞的外形和行为。健康的血管在需要时会收缩,但是在先兆子痫期间,血管细胞发生肿胀,血管失去弹性。
Quitterer及其同事们指出这是由于在怀孕的最后三个月期间腹部遭受很大的压力,这导致AT1-B2异源二聚体过度刺激。他们对小鼠进行基因改造,使得这两种负责感知血管细胞中的机械刺激的G蛋白偶联受体在它们体内聚集。在怀孕(小鼠的妊娠期为20天)18天之后,这些小鼠出现了与先兆子痫女性患者相同的症状:血压增加和尿液中的蛋白水平升高。
这些研究人员能够通过降低AT1-B2异源二聚体来延迟先兆子痫发作。他们用氨氯地平(amlodipine)来治疗这些小鼠。氨氯地平是一种旧的抗高血压药物,可阻断钙离子通道,因而破坏由AT1-B2异源二聚体触发的信号级联反应。这种治疗确保血管细胞不发生肿胀并且确保血管壁保持弹性。
8.PNAS:特殊药物或能通过诱发幽门螺杆菌基因突变来有效抑制胃癌发生
胃癌是引发癌症患者死亡的第三大原因,而幽门螺杆菌的感染是引发胃癌的主要原因之一。在一项新的研究中,来自德国范德堡大学医学中心的研究人员通发现,目前作为一种化疗制剂治疗多种类型疾病的药物或许在治疗胃癌上也表现出了巨大潜力;除了已知能阻断癌细胞的生长外,这种称为DFMO(二氟甲基鸟氨酸)的药物还能直接作用于幽门螺杆菌来降低其毒力,幽门螺杆菌的感染是引发胃癌的主要原因。相关研究结果发表在2019年3月12日的PNAS期刊上。
利用广泛使用的抗生素来消除幽门螺杆菌感染来预防胃癌似乎并不是一个好主意,在这项研究中,这些研究人员认为,或许可以通过降低幽门螺杆菌的毒力(并不必消灭幽门螺杆菌)来有效预防胃癌的发生。此前,当对幽门螺杆菌感染的动物模型进行研究时,他们已发现促进细胞生长的化合物多胺类或与胃癌的发生存在一定关联,而利用DFMO来治疗动物或能有效预防胃癌的发生,DFMO能够抑制对聚胺类产生非常关键的酶类的功能。
为了深入阐明DFMO的作用机制,这些研究人员从接受或不接受DFMO治疗的受感染动物身体中收集幽门螺杆菌,随后利用体外检测手段,评估了幽门螺杆菌的一个主要毒力因子---CagA蛋白---的活性,其中CagA蛋白能够“注入”胃部上皮细胞中促进致癌信号通路激活。研究者Sierra表示,来自接受DFMO治疗的动物身体中的幽门螺杆菌会降低将它们的毒力因子运输到胃部上皮细胞中的能力;不管在体外还是在动物体内试验中,DFMO治疗都能够引发幽门螺杆菌中编码CagY的基因发生突变,CagY是将CagA注入细胞的转位机制中的一部分。
此外,这些研究人员还发现,感染包含CagY突变的幽门螺杆菌的动物并不会发生胃癌,本文研究结果支持DFMO药物或其它工具来降低幽门螺杆菌的毒力,从而实现胃癌的有效预防;DFMO能抑制多种特殊的酶类通路,此外,它还会产生一些“偏离靶标”的效应,即促进幽门螺杆菌中的CagY基因发生突变;如今大部分胃癌都与CagA阳性的幽门螺杆菌菌株直接相关,如果利用药物来干预CagA的活性,或许就能获得额外的收益。
9.Cancer Cell:一类新型药物有望治疗卵巢癌
在一项新的研究中,来自英国曼彻斯特大学的研究人员通过研究发现了一类新型药物或能阻断卵巢癌细胞的生长;他们发现,一种称为PARG抑制剂的药物能够通过靶向作用癌细胞内DNA复制的弱点来杀灭卵巢癌细胞。相关研究结果发表在2019年3月18日的Cancer Cell期刊上。
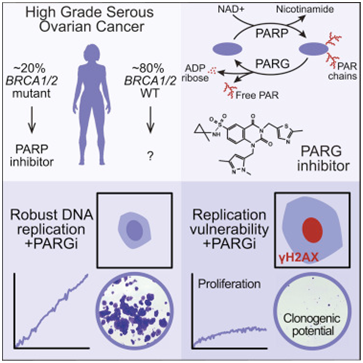
这些研究人员通过对卵巢癌细胞中多个特殊基因进行筛查并寻找合适的PARG抑制剂,最终鉴别出了一种关键基因能使得癌细胞对PDD00017273抑制剂变得敏感。他们深入分析了这种PARG抑制剂的作用机制,并发现在细胞分裂前,它会阻止DNA的复制。此外,他们发现了卵巢癌细胞进行DNA复制的缺陷,这或许就能被这种PARG抑制剂靶向作用,用以杀灭卵巢癌细胞。
这类新型抑制剂或能帮助抵抗性卵巢癌患者对标准化疗药物再次产生反应;这些研究人员发现,PARG抑制剂还能与临床上的其它药物联合使用来杀灭卵巢癌细胞,比如CHK1和WEE1抑制剂等。这些研究结果能够有助人们在未来开发出一种用于人类临床试验的PARG抑制剂。
10.Cell:新研究揭示抗体的一种意料之外的作用机制
在一项新的研究中,来自美国华盛顿大学等研究机构的研究人员通过研究从由冠状病毒引起的严重急性呼吸综合征(SARS)或中东呼吸综合征(MERS)的幸存者中分离出的人单克隆抗体,揭示出令人吃惊的抵抗致命病毒的免疫防御策略。针对这些高度强效的抗体的原子和分子信息可能为阻止这些严重的有时是致命性的肺部感染提供新的见解。相关研究结果发表在2019年2月21日的Cell期刊上,论文标题为“Unexpected Receptor Functional Mimicry Elucidates Activation of Coronavirus Fusion”。论文通讯作者为华盛顿大学医学院生物化学系的David Veesler。论文第一作者为华盛顿大学医学院生物化学系的Alexandra Walls和Xiaoli Xiong。
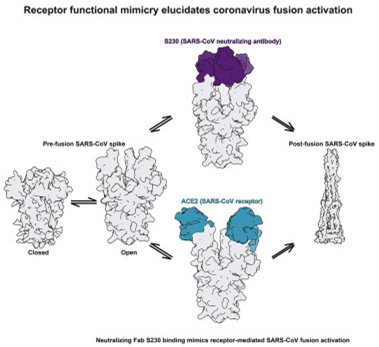
当前,还没有针对6种能够感染人类的冠状病毒---比如MERS冠状病毒(MERS-CoV)---的疫苗或特异性疗法。冠状病毒具有多功能性的表面刺突,这些由刺突糖蛋白(spike glycoprotein)组成的刺突识别和结合位于宿主细胞表面上的受体。它们随后将病毒和细胞膜融合在一起,因而也是是中和抗体的作用靶标,也是亚单位疫苗设计的重点。冠状病毒使用三聚体刺突糖蛋白作为它们的分子入侵工具。
在这项新的研究中,通过使用低温电镜和其他的强大技术,这些研究人员对来自SARS和MERS幸存者的中和性单克隆抗体在分子水平上如何抑制这两种冠状病毒(SARS-CoV和MERS-CoV)提供了新的见解。他们的发现也有助于阐明冠状病毒膜融合激活的不寻常性质。
这些研究人员发现来自SARS和MERS幸存者的中和性单克隆抗体都能阻止各自的病毒刺突与宿主细胞膜上的受体之间的相互作用。来自SARS幸存者的中和性单克隆抗体还具有某种意想不到的作用:它在功能上模拟受体结合并诱导病毒刺突经历构象变化,从而导致膜融合。这种触发似乎是由一种分子棘轮机制(molecular ratcheting mechanism)驱动的。
这些研究人员指出,“这一发现是功能模拟的一个前所未有的例子:抗体通过再现受体的作用来激活膜融合。”
其实,科学家们针对药物或潜在药物开展的作用机理研究不胜枚举,以上罗列的仅是其中的一小部分。当然,迄今为止,针对药物或潜在药物的作用机理研究仍然是在细胞水平、基因水平或蛋白水平上开展的,而且所揭示的药物作用机理仍然还有待进一步深入。不过,在未来,科学家们将从病理学、分子生物学、基因、蛋白和组学等不同角度深入探究药物或潜在药物的详细作用机理,人们最终有朝一日能够利用药物或潜在药物治疗HIV感染、癌症、血液系统疾病、神经系统疾病和遗传疾病等一系列疾病。(生物谷 Bioon.com)
参考文献:
1. Vikram Babu Kasaragod, Torben Johann Hausrat, Natascha Schaefer, et al. Elucidating the Molecular Basis for Inhibitory Neurotransmission Regulation by Artemisinins. Neuron, 2019, doi:10.1016/j.neuron.2019.01.001.
2. Maria C. Ramello et al, An immunoproteomic approach to characterize the CAR interactome and signalosome. Science Signaling , 2019, doi:10.1126/scisignal.aap9777.
3. Zydrune Polianskyte-Prause, Tuomas A. Tolvanen, Sonja Lindfors et al. Metformin increases glucose uptake and acts renoprotectively by reducing SHIP2 activity. FASEB Journal, Published Online: 15 October 2018, doi:10.1096/fj.201800529RR.
4. R.N. Moda-Sava el al. Sustained rescue of prefrontal circuit dysfunction by antidepressant-induced spine formation. Science, 2019, doi:10.1126/science.aat8078.
5. Romain Nardou et al. Oxytocin-dependent reopening of a social reward learning critical period with MDMA. Nature, 2019, doi:10.1038/s41586-019-1075-9.
6. Jiyoung Lee, Ali E. Yesilkanal, Joseph P. Wynne et al. Effective breast cancer combination therapy targeting BACH1 and mitochondrial metabolism. Nature, 2019, doi:10.1038/s41586-019-1005-x.
7. Johanna C. Sierra, Giovanni Suarez, M. Blanca Piazuelo et al. α-Difluoromethylornithine reduces gastric carcinogenesis by causing mutations in Helicobacter pylori cagY. PNAS, 2019, doi:10.1073/pnas.1814497116.
8. Ursula Quitterer et al. Beta-Arrestin1 Prevents Preeclampsia by Downregulation of Mechanosensitive AT1-B2 Receptor Heteromers. Cell, 2018, doi:10.1016/j.cell.2018.10.050.
9. Nisha Pillay et al. DNA Replication Vulnerabilities Render Ovarian Cancer Cells Sensitive to Poly(ADP-Ribose) Glycohydrolase Inhibitors. Cancer Cell, 2019, doi:10.1016/j.ccell.2019.02.004.
10. Alexandra C. Walls et al. Unexpected Receptor Functional Mimicry Elucidates Activation of Coronavirus Fusion. Cell, 2019, doi:10.1016/j.cell.2018.12.028.
药物的作用机理多种多样,是不同药物分子与机体不同靶细胞间相互作用的结果。药物作用的性质首先取决于药物的化学结构,包括基本骨架、活性基团、侧链长短及立体构形等因素。这些结构-活性关系(structure-activity relationship)是药物化学研究的主要对象,也有助于加强人们对药物作用的理解。
影响药物的选择和应用的两个医学名词是药效学(药物对机体的作用)和药物动力学(机体对药物的作用)。除了探讨药物的作用(例如减轻疼痛、降低血压、降低血浆胆固醇水平)外,药物动力学还研究药物在什么部位和怎样发挥作用(即作用机制)。虽然药物作用比较容易显现,但其作用部位和机制不可能很快弄清楚。比如,阿片和吗啡用于镇痛和治疗抑郁已有几百年了,但仅仅是不久前才发现与镇痛欣快有关的大脑结构和脑化学成分。
药物必须到达发病部位才能起作用,这也是药代动力学的重要性所在。药物发挥作用时须在患部保持足够的量,但又不能产生严重不良反应,每个医生都知道选择正确剂量是一门复杂的平衡艺术。
许多药物通过血循环到达作用部位。药物显效时间和效应维持时间一般由该药进入血液的速度、进入量、清除的速度、肝脏代谢的效率以及被肾和肠道清除的速度所决定。
每个个体对药物的反应均有差异。为达到同一疗效,体重较重的人比较轻的人需要更多的药量。新生儿和老年人对药物的代谢慢于儿童和青年人。肝肾病患者对药物的清除亦比正常人困难。每种新药的标准剂量或平均剂量由动物试验和人的试验决定。但平均剂量表面上被定义为“适合所有人的剂量”,其实它只对一定范围的个体适用,并不完全适合每个个体。
药物体内过程因人而异,许多因素可影响药物的吸收、分布、代谢、排泄,从而影响最终的药效。其他一些因素也可影响药物的作用,如遗传、药物间的相互作用、疾病等。
遗传可影响药物的代谢过程。由于遗传差异,有些人代谢药物的速度慢,药物易蓄积并引起中毒,有些人代谢药物速度快,药物在体内不易达到有效浓度。遗传还可影响药物代谢的其他方面,比如:常用剂量下药物代谢速度正常,当药物剂量过高或和另一同类药物合用时,超过其代谢能力会导致药物蓄积中毒。
此外,当两种药物同时使用(药-药相互作用)或食用某些食物(药-食物相互作用),该药的作用可被其影响,称为药物的相互作用。尽管联合用药有时是有益的,但多数时候是无益的甚至是有害的。药物相互作用可以增强或减弱药效或不良反应。药物的相互作用多发生在处方药,但有时也会出现在非处方药中,最常见的有阿司匹林、抗酸剂及抗凝药。药物相互作用的危险性取决于用药的种类、数量及剂量。许多作用是在药物研制过程中发现的,医护人员有医药知识可减少相互作用危害的发生。不考虑药物特点用药会增加其危险性。医护人员指导用药,如发生不良相互作用是由于医护人员对药物了解不够。
鉴于很多药物的作用机理比较复杂,哪怕是明星药和重磅炸弹药,它们的作用机理也并未得到深入理解。了解药物的作用机理,有助指导科学家们进行个人化用药,并对现有的药物进行结构优化,增强它们的疗效,同时降低它们的毒副作用,从而更好地造福人类。基于此,让我们梳理一下药物作用机理研究方面取得的进展,以飨读者。
1.Neuron:科学家阐明青蒿素发挥作用的分子机制
尽管抗疟疾药青蒿素已经被广泛使用了几个世纪了,但是人们仍然并不清楚青蒿素发挥作用的分子机制。在一项刊登在2019年2月20日的Neuron期刊上的研究中,来自德国维尔茨堡大学的研究人员阐明了青蒿素发挥作用的分子机制。

图片来自Neuron, 2019, doi:10.1016/j.neuron.2019.01.001。
这些研究人员首次揭示了两种不同的青蒿素衍生物---青蒿琥酯和青蒿素甲醚---与桥尾蛋白(gephyrin)结合在一起时的晶体结构。通过结合抑制性的甘氨酸和GABAA受体,桥尾蛋白在哺乳动物中枢神经系统中能够扮演抑制性突触后中央支架蛋白的角色,而且人们已发现桥尾蛋白是青蒿素的一种靶蛋白。在这项研究中,他们阐明了青蒿素如何靶向作用于桥尾蛋白中通用的受体结合槽以及如何与抑制性神经递质受体竞争来重叠的结合位点;这些研究结果或能作为一种有效的工具帮助科学家们理解人类大脑的生理学特性。
这些研究人员表示,将晶体学结构、生物化学、电生理学及相关数据进行结合,他们就能开发出受青蒿素抑制神经递质调控的综合模型,而这种模型就能清楚地描述蛋白质和药物之间的相互作用。
2.Sci Signal:科学家揭示CAR-T细胞发挥抗癌疗效的分子机制
在过去十年中,一种新型的抗癌疗法---免疫疗法---取得了巨大的成功,这是一种通过激活人体自身免疫系统来攻击癌细胞的疗法。其中的一种免疫疗法称为嵌合抗原受体(CAR)T细胞(CAR-T细胞)免疫疗法,已经在某些癌症病人身上取得了喜人的疗效,而两种CAR-T细胞免疫疗法(Kymriah和Yescarta)已经被美国FDA批准用于治疗急性成淋巴细胞性白血病和大B细胞淋巴瘤。尽管取得了如此巨大的成功,但是科学家们仍然没有完全搞清楚CAR-T细胞发挥功能的机制。如今,在一项新的研究中,来自美国莫菲特癌症研究中心的研究人员解决了这个问题,并阐明了CAR T细胞发挥作用的具体机制,相关研究成果发表在2019年2月12日的Science Signaling期刊上。
CAR-T细胞免疫疗法是一种独特的免疫疗法:首先收集和分离患者血液中的T细胞,在实验室中对分离后的T细胞进行仅修饰,从而给它们添加一种CAR的特殊受体用于识别癌细胞。这些经过基因修饰的T细胞会在体外进行培养和增殖,最后被灌注回相同的患者体内。
对T细胞中进行基因修饰已经被多个课题组加以优化以让它们发挥最佳的抗癌免疫反应。其中一个被插入到T细胞中的基因是T细胞受体(CD3ζ)的一部分,此外还包括其他的共刺激分子,最新的第三代CAR还包括了多个共刺激分子受体。但是一些研究表明嵌入多个共刺激分子受体并没有让第三代CAR-T细胞的疗效增强。此外,其它的基因修饰则聚焦于CAR受体的结构设计,比如将CAR受体结合在细胞表面上的区域。但是迄今为止,人们都还不清楚这些不同的基因修饰和结构设计会对生物学信号及T细胞反应产生怎样的影响。
考虑到CAR-T细胞免疫疗法的应用越来越广泛,这些研究人员认为理解这些疗法在病人体内发挥作用的具体机制至关重要。为了更好地理解CAR-T细胞如何发挥效应,他们使用了一系列基于蛋白组学的手段去比较靶向癌细胞上相同分子但是胞内设计和抗癌活性不同的CAR-T细胞。他们发现第二代和第三代CAR受体可以结合一系列分子,其中的一些分子甚至具有相反的功能。重要的是,只有第二代CAR受体能够刺激类似于自然版本的CD3ζ的表达。他们发现第二代CAR受体的这个活性依赖于胞内区域的结构设计,而与共刺激分子受体或者结合区域的结构无关。此外,通过详细的磷酸蛋白组学分析,他们发现与第三代CAR受体相比,第二代CAR受体能够更有效地激活下游信号分子。
这些结果表明第二代CAR受体可以激活其它来源的CD3信号,这也许导致了更强烈的信号和更有效的抗癌效应。通过系统分析与CAR受体相互作用的信号蛋白及不同CAR受体结构激活的信号通路,这些研究人员能够提供新工具用于开发功能更可控的新CAR受体。
3.FASEB J:揭示二甲双胍治疗2型糖尿病的新作用机制
几十年来,二甲双胍(metformin)一直是治疗2型糖尿病的一线药物,通过抑制肝脏中的葡萄糖产生来降低血糖水平。二甲双胍还可改善肌肉组织中的葡萄糖摄取和使用。二甲双胍对肝脏中的葡萄糖产生的影响很可能是通过线粒体呼吸链传递的。然而,这种药物增加肌肉组织中葡萄糖摄取的机制仍然是不清楚的。
如今,在一项新的研究中,芬兰赫尔辛基大学的Sanna Lehtonen教授及其团队在细胞培养物和动物模型中证实二甲双胍直接结合到脂质磷酸酶SHIP2上,降低它的活性。SHIP2活性的降低增加了肌肉细胞中的葡萄糖摄取并减少了足细胞或肾小球上皮细胞中的细胞死亡。相关研究结果发表在2019年2月的FASEB Journal期刊上。

图片来自Lehtonen Lab/University of Helsinki。
脂质磷酸酶SHIP2抑制胰岛素信号通路。之前的研究已通过动物模型证实患有糖尿病的个体在其肾脏、肌肉和脂肪组织中具有升高的SHIP2水平。这降低了组织对胰岛素信号作出反应并降低其葡萄糖摄取的能力。升高的SHIP2浓度也增加足细胞的程序性细胞死亡。除动物模型外,Lehtonen团队还在研究中使用了患者样本。他们的分析显示在未服用二甲双胍的2型糖尿病患者中,肾脏中的SHIP2活性升高了,此外足细胞丢失是显著的。在服用二甲双胍的患者中,肾脏中的SHIP2活性与非糖尿病患者中的一样,而且足细胞丢失也低于使用其他药物治疗的患者。
Lehtonen说,“我们的研究结果表明脂质磷酸酶SHIP2在调节足细胞中的葡萄糖代谢和细胞死亡中具有重要作用。因此,用二甲双胍或其他合适的药物调节SHIP2活性对于控制2型糖尿病尤其是预防相关的糖尿病肾病至关重要。”
二甲双胍的作用机制正在受到积极的研究,这是因为它对身体具有多种影响,这就使得它可能有助于治疗除糖尿病之外的疾病。更好地理解它的作用机制还有助于利用这种药物精确地治疗从中受益的患者群体。
4.Science:揭示为何氯胺酮是一种抗抑郁药
在一项新的研究中,来自日本东京大学、美国斯坦福大学和威尔康乃尔医学院的研究人员在小鼠中鉴定出氯胺酮(ketamine)诱导的大脑相关变化有助于维持与抑郁症有关的行为的缓解,这一发现可能有助于人们开发出促进人类抑郁症持续缓解的干预措施。相关研究结果发表在2019年4月12日的Science期刊上,论文标题为“Sustained rescue of prefrontal circuit dysfunction by antidepressant-induced spine formation”。

图片来自Science, 2019, doi:10.1126/science.aat8078。
为了理解人体中从抑郁症发作到缓解转变背后的机制,这些研究人员在小鼠中研究了与抑郁相关的行为。在小鼠经历应激源之前和之后,他们获得了它们的前额叶皮质中的树突棘(dendritic spine)的高分辨率图像。树突棘是神经元中接收来自其他神经元的通信输入的突起。他们发现相比于没有暴露于应激源中的小鼠,显示出与抑郁有关的行为的小鼠在其前额皮质中的树突棘消除增加了和树突棘形成减少了。这一发现复制了之前开展的将与小鼠中抑郁相关的行为的出现与树突棘损失相关联在一起的研究。
除了对树突棘的影响外,应激还降低了小鼠前额叶皮质中神经元的功能性连接和同时活动。这种连接性和活动性的降低与应对应激源的抑郁症相关行为有关。Liston及其团队随后发现氯胺酮治疗快速恢复了神经元的功能连接和整体活动,并且消除了与抑郁有关的行为。相比于遭受应激但未接受氯胺酮治疗的小鼠,在接受单剂量氯胺酮治疗24小时后,遭受应激的小鼠表现出与抑郁相关的行为逆转和树突棘形成的增加。这些新的树突棘是功能性的,因而与其他神经元建立了工作上的关联性。
这些研究人员发现尽管小鼠的行为改变和神经活动变化发生很快(在接受氯胺酮治疗3小时后),但是树突棘的形成发生得更慢(在氯胺酮治疗12~24小时后)。虽然还需开展进一步的研究,但是他们认为这些发现可能表明树突棘再生是氯胺酮诱导的前额皮质回路活动恢复的结果。
5.Nature:迷幻剂MDMA可能有助治疗创伤后应激障碍
神经系统对特定环境刺激明显敏感的发育时期是一个关键时期,在这个时期,这些特定环境刺激是正确的神经回路形成和学习所必需的。对关键时期进行机制上的表征已揭示出活跃的大脑可塑性在早期发育期间的重要作用,以及随着大脑发育成熟对这些机制施加约束的重要作用。在疾病状态中,关键时期的关闭限制了大脑的适应能力,即使在恢复到最佳条件时也是如此。因此,鉴定重新开启关键时期的操作一直是转化神经科学领域的一个重点。
在一项新的研究中,来自美国约翰霍普金斯大学和麻省理工学院的研究人员提供证据表明对催产素(oxytocin)在大脑伏核(nucleus accumbens)中介导的突触可塑性(长期抑郁)进行发育调节为社会奖励学习建立了一个关键时期。相关研究结果于2019年4月3日在线发表在Nature期刊上,论文标题为“Oxytocin-dependent reopening of a social reward learning critical period with MDMA”。
这些研究人员还发现单剂量的(+/−)-3,4-亚甲基二氧甲基苯丙胺(3,4-methylendioxymethamphetamine, MDMA)重新开启社会奖励学习的关键时期,并导致催产素依赖性长期抑郁症的化生性上调(metaplastic upregulation)。MDMA诱导的这一关键时期重新开启需要激活大脑伏核中的催产素受体,并通过刺激大脑伏核中的催产素末端得以重现。
由此可见,这些发现对于理解以社交障碍为特征的神经发育性疾病、以及对社会影响作出反应或由社会伤害引起的疾病的发病机制具有重要意义。
6.Nature:重大突破!老药二甲双胍和血红素组合有望治愈三阴性乳腺癌!
据估计,大约15%~20%的乳腺癌患者为三阴性乳腺癌患者,即患者机体缺失三种关键的治疗靶点:雌激素受体、孕激素受体和人类表皮生长因子受体2,由于缺少这些靶点,大部分三阴性乳腺癌患者都会接受标准化疗,而不是首选靶向性药物。
由于缺少治疗三阴性乳腺癌的有效疗法,因此很多科学家们都在奋力研究寻找新型的药物靶点。在一项新的研究中,来自美国芝加哥大学的研究人员就发现一对新型武器—两种古老的药物,当其对患癌小鼠进行治疗时能够产生令人鼓舞的结果,相关研究结果发表在2019年4月11日的Nature期刊上。这意味着能够通过组合使用这两种古老药物(二甲双胍和血红素)来治疗当前无法靶向治疗的耐受性乳腺癌。

图片来源:CC0 Public Domain。
这些研究人员发现,血红素最主要的抗癌靶点是一种名为BACH1的转录因子,该蛋白在三阴性乳腺癌中高度表达,而且其也是癌症转移所需要的关键蛋白;高水平的BACH1会引发患者预后不良,但庆幸的是,BACH1并不是必要的。BACH1能靶向作用线粒体代谢,通过结合特殊的DNA序列控制DNA的转录速率,从而抑制线粒体电子传递链的转录(细胞能量的关键来源),当BACH1水平较高时,这种能量来源就会被切断。
当利用血红素处理癌细胞时,BACH1的水平就会下降,从而就会促进BACH1剔除的癌细胞改变它们的代谢通路,同时还会促进对二甲双胍易感的癌症抑制癌细胞中的线粒体呼吸链,因此将二甲双胍与血红素组合使用就能有效抑制肿瘤的生长,这些研究人员随后在小鼠肿瘤模型中证实了这一点。
BACH1低水平的三阴性乳腺癌患者和高水平线粒体基因表达的患者很有可能单独对二甲双胍产生反应,而高水平BACH1和线粒体基因表达水平较低的癌症患者或许会对二甲双胍产生耐受性,而本文研究结果表明,在二甲双胍疗法基础上加入血红素疗法就能使得癌症患者对二甲双胍再次产生反应;此外,这些研究人员指出,BACH1能够作为线粒体代谢的关键调节因子,同时也是三阴性乳腺癌患者对二甲双胍是否产生反应的主要决定因子。
这些研究结果或许能够扩展到对乳腺癌以外的癌症进行研究,BACH1不仅在三阴性乳腺癌中表达水平较高,其还在很多癌症中会发生高水平表达,包括肺癌、肾癌等,BACH1抑制线粒体电子传递链似乎是一种常见的机制。在未来,这些研究人员还将深入研究阐明二甲双胍和血红素联合疗法治疗三阴性乳腺癌的分子机理。
7.Cell:抗高血压药物氨氯地平可治疗先兆子痫
在全世界,每20名女性中就有一人在怀孕期间患有先兆子痫(preeclampsia)。它会导致血压升高和肾脏停止运作。先兆子痫是怀孕期间最常见的死亡原因之一---无论是母亲还是未出生的孩子。当前还没有治疗这种疾病的方法。医生采取的阻止子痫(eclampsia)---一种危及生命的癫痫发作---的唯一方法是提早分娩。
在一项新的研究中,来自瑞士苏黎世联邦理工学院的研究人员揭示了在先兆子痫中,导致血管增厚和失去弹性的信号通路。他们开发出的一种治疗方法能够治疗患有先兆子痫的孕妇。相关研究结果发表在2019年1月10日的Cell期刊上,论文标题为“Beta-Arrestin1 Prevents Preeclampsia by Downregulation of Mechanosensitive AT1-B2 Receptor Heteromers”。论文通讯作者为苏黎世联邦理工学院分子药理学教授Ursula Quitterer博士。

图片来自Cell, doi:10.1016/j.cell.2018.10.050。
这项研究着重关注聚集在一起的两种G蛋白偶联受体(血管紧张素II AT1和血管舒缓激肽B2),即AT1-B2异源二聚体。它们不仅对激素冲动作出反应,而且还对机械刺激作出反应,从而触发信号级联反应在血管细胞内部发生,并从根本上改变这些细胞的外形和行为。健康的血管在需要时会收缩,但是在先兆子痫期间,血管细胞发生肿胀,血管失去弹性。
Quitterer及其同事们指出这是由于在怀孕的最后三个月期间腹部遭受很大的压力,这导致AT1-B2异源二聚体过度刺激。他们对小鼠进行基因改造,使得这两种负责感知血管细胞中的机械刺激的G蛋白偶联受体在它们体内聚集。在怀孕(小鼠的妊娠期为20天)18天之后,这些小鼠出现了与先兆子痫女性患者相同的症状:血压增加和尿液中的蛋白水平升高。
这些研究人员能够通过降低AT1-B2异源二聚体来延迟先兆子痫发作。他们用氨氯地平(amlodipine)来治疗这些小鼠。氨氯地平是一种旧的抗高血压药物,可阻断钙离子通道,因而破坏由AT1-B2异源二聚体触发的信号级联反应。这种治疗确保血管细胞不发生肿胀并且确保血管壁保持弹性。
8.PNAS:特殊药物或能通过诱发幽门螺杆菌基因突变来有效抑制胃癌发生
胃癌是引发癌症患者死亡的第三大原因,而幽门螺杆菌的感染是引发胃癌的主要原因之一。在一项新的研究中,来自德国范德堡大学医学中心的研究人员通发现,目前作为一种化疗制剂治疗多种类型疾病的药物或许在治疗胃癌上也表现出了巨大潜力;除了已知能阻断癌细胞的生长外,这种称为DFMO(二氟甲基鸟氨酸)的药物还能直接作用于幽门螺杆菌来降低其毒力,幽门螺杆菌的感染是引发胃癌的主要原因。相关研究结果发表在2019年3月12日的PNAS期刊上。
利用广泛使用的抗生素来消除幽门螺杆菌感染来预防胃癌似乎并不是一个好主意,在这项研究中,这些研究人员认为,或许可以通过降低幽门螺杆菌的毒力(并不必消灭幽门螺杆菌)来有效预防胃癌的发生。此前,当对幽门螺杆菌感染的动物模型进行研究时,他们已发现促进细胞生长的化合物多胺类或与胃癌的发生存在一定关联,而利用DFMO来治疗动物或能有效预防胃癌的发生,DFMO能够抑制对聚胺类产生非常关键的酶类的功能。
为了深入阐明DFMO的作用机制,这些研究人员从接受或不接受DFMO治疗的受感染动物身体中收集幽门螺杆菌,随后利用体外检测手段,评估了幽门螺杆菌的一个主要毒力因子---CagA蛋白---的活性,其中CagA蛋白能够“注入”胃部上皮细胞中促进致癌信号通路激活。研究者Sierra表示,来自接受DFMO治疗的动物身体中的幽门螺杆菌会降低将它们的毒力因子运输到胃部上皮细胞中的能力;不管在体外还是在动物体内试验中,DFMO治疗都能够引发幽门螺杆菌中编码CagY的基因发生突变,CagY是将CagA注入细胞的转位机制中的一部分。
此外,这些研究人员还发现,感染包含CagY突变的幽门螺杆菌的动物并不会发生胃癌,本文研究结果支持DFMO药物或其它工具来降低幽门螺杆菌的毒力,从而实现胃癌的有效预防;DFMO能抑制多种特殊的酶类通路,此外,它还会产生一些“偏离靶标”的效应,即促进幽门螺杆菌中的CagY基因发生突变;如今大部分胃癌都与CagA阳性的幽门螺杆菌菌株直接相关,如果利用药物来干预CagA的活性,或许就能获得额外的收益。
9.Cancer Cell:一类新型药物有望治疗卵巢癌
在一项新的研究中,来自英国曼彻斯特大学的研究人员通过研究发现了一类新型药物或能阻断卵巢癌细胞的生长;他们发现,一种称为PARG抑制剂的药物能够通过靶向作用癌细胞内DNA复制的弱点来杀灭卵巢癌细胞。相关研究结果发表在2019年3月18日的Cancer Cell期刊上。

图片来自Cancer Cell, 2019, doi:10.1016/j.ccell.2019.02.004。
这些研究人员通过对卵巢癌细胞中多个特殊基因进行筛查并寻找合适的PARG抑制剂,最终鉴别出了一种关键基因能使得癌细胞对PDD00017273抑制剂变得敏感。他们深入分析了这种PARG抑制剂的作用机制,并发现在细胞分裂前,它会阻止DNA的复制。此外,他们发现了卵巢癌细胞进行DNA复制的缺陷,这或许就能被这种PARG抑制剂靶向作用,用以杀灭卵巢癌细胞。
这类新型抑制剂或能帮助抵抗性卵巢癌患者对标准化疗药物再次产生反应;这些研究人员发现,PARG抑制剂还能与临床上的其它药物联合使用来杀灭卵巢癌细胞,比如CHK1和WEE1抑制剂等。这些研究结果能够有助人们在未来开发出一种用于人类临床试验的PARG抑制剂。
10.Cell:新研究揭示抗体的一种意料之外的作用机制
在一项新的研究中,来自美国华盛顿大学等研究机构的研究人员通过研究从由冠状病毒引起的严重急性呼吸综合征(SARS)或中东呼吸综合征(MERS)的幸存者中分离出的人单克隆抗体,揭示出令人吃惊的抵抗致命病毒的免疫防御策略。针对这些高度强效的抗体的原子和分子信息可能为阻止这些严重的有时是致命性的肺部感染提供新的见解。相关研究结果发表在2019年2月21日的Cell期刊上,论文标题为“Unexpected Receptor Functional Mimicry Elucidates Activation of Coronavirus Fusion”。论文通讯作者为华盛顿大学医学院生物化学系的David Veesler。论文第一作者为华盛顿大学医学院生物化学系的Alexandra Walls和Xiaoli Xiong。

图片来自Cell, 2019, doi:10.1016/j.cell.2018.12.028。
当前,还没有针对6种能够感染人类的冠状病毒---比如MERS冠状病毒(MERS-CoV)---的疫苗或特异性疗法。冠状病毒具有多功能性的表面刺突,这些由刺突糖蛋白(spike glycoprotein)组成的刺突识别和结合位于宿主细胞表面上的受体。它们随后将病毒和细胞膜融合在一起,因而也是是中和抗体的作用靶标,也是亚单位疫苗设计的重点。冠状病毒使用三聚体刺突糖蛋白作为它们的分子入侵工具。
在这项新的研究中,通过使用低温电镜和其他的强大技术,这些研究人员对来自SARS和MERS幸存者的中和性单克隆抗体在分子水平上如何抑制这两种冠状病毒(SARS-CoV和MERS-CoV)提供了新的见解。他们的发现也有助于阐明冠状病毒膜融合激活的不寻常性质。
这些研究人员发现来自SARS和MERS幸存者的中和性单克隆抗体都能阻止各自的病毒刺突与宿主细胞膜上的受体之间的相互作用。来自SARS幸存者的中和性单克隆抗体还具有某种意想不到的作用:它在功能上模拟受体结合并诱导病毒刺突经历构象变化,从而导致膜融合。这种触发似乎是由一种分子棘轮机制(molecular ratcheting mechanism)驱动的。
这些研究人员指出,“这一发现是功能模拟的一个前所未有的例子:抗体通过再现受体的作用来激活膜融合。”
其实,科学家们针对药物或潜在药物开展的作用机理研究不胜枚举,以上罗列的仅是其中的一小部分。当然,迄今为止,针对药物或潜在药物的作用机理研究仍然是在细胞水平、基因水平或蛋白水平上开展的,而且所揭示的药物作用机理仍然还有待进一步深入。不过,在未来,科学家们将从病理学、分子生物学、基因、蛋白和组学等不同角度深入探究药物或潜在药物的详细作用机理,人们最终有朝一日能够利用药物或潜在药物治疗HIV感染、癌症、血液系统疾病、神经系统疾病和遗传疾病等一系列疾病。(生物谷 Bioon.com)
参考文献:
1. Vikram Babu Kasaragod, Torben Johann Hausrat, Natascha Schaefer, et al. Elucidating the Molecular Basis for Inhibitory Neurotransmission Regulation by Artemisinins. Neuron, 2019, doi:10.1016/j.neuron.2019.01.001.
2. Maria C. Ramello et al, An immunoproteomic approach to characterize the CAR interactome and signalosome. Science Signaling , 2019, doi:10.1126/scisignal.aap9777.
3. Zydrune Polianskyte-Prause, Tuomas A. Tolvanen, Sonja Lindfors et al. Metformin increases glucose uptake and acts renoprotectively by reducing SHIP2 activity. FASEB Journal, Published Online: 15 October 2018, doi:10.1096/fj.201800529RR.
4. R.N. Moda-Sava el al. Sustained rescue of prefrontal circuit dysfunction by antidepressant-induced spine formation. Science, 2019, doi:10.1126/science.aat8078.
5. Romain Nardou et al. Oxytocin-dependent reopening of a social reward learning critical period with MDMA. Nature, 2019, doi:10.1038/s41586-019-1075-9.
6. Jiyoung Lee, Ali E. Yesilkanal, Joseph P. Wynne et al. Effective breast cancer combination therapy targeting BACH1 and mitochondrial metabolism. Nature, 2019, doi:10.1038/s41586-019-1005-x.
7. Johanna C. Sierra, Giovanni Suarez, M. Blanca Piazuelo et al. α-Difluoromethylornithine reduces gastric carcinogenesis by causing mutations in Helicobacter pylori cagY. PNAS, 2019, doi:10.1073/pnas.1814497116.
8. Ursula Quitterer et al. Beta-Arrestin1 Prevents Preeclampsia by Downregulation of Mechanosensitive AT1-B2 Receptor Heteromers. Cell, 2018, doi:10.1016/j.cell.2018.10.050.
9. Nisha Pillay et al. DNA Replication Vulnerabilities Render Ovarian Cancer Cells Sensitive to Poly(ADP-Ribose) Glycohydrolase Inhibitors. Cancer Cell, 2019, doi:10.1016/j.ccell.2019.02.004.
10. Alexandra C. Walls et al. Unexpected Receptor Functional Mimicry Elucidates Activation of Coronavirus Fusion. Cell, 2019, doi:10.1016/j.cell.2018.12.028.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


