Nat Med:双靶向CAR NK细胞有望阻止NK细胞功能衰竭和肿瘤逃逸
来源:生物谷原创 2022-10-25 10:52
研究人员开发了一种新方法:除了对NK细胞进行基因改造使之表达一种识别肿瘤抗原的嵌合抗原受体(CAR)之外,还让它们表达一种抑制NK细胞自我识别的CAR,从而阻止NK细胞功能障碍和肿瘤复发。
在一项新的研究中,来自美国德克萨斯大学MD安德森癌症中心的研究人员开发了一种新方法:除了对自然杀伤细胞(NK细胞)进行基因改造使之表达一种识别肿瘤抗原的嵌合抗原受体(CAR)之外,还对它们进行进一步基因改造使之表达一种抑制NK细胞自我识别的作为逻辑门起作用的CAR,这样就使得这种双靶向CAR NK细胞需要两种信号才能杀死靶细胞。在临床前实验中,这种下一代CAR NK细胞通过克服一种导致NK细胞功能障碍和肿瘤复发的过程,改善了肿瘤的特异性并增强了抗肿瘤活性。相关研究结果发表在2022年10月的Nature Medicine期刊上,论文标题为“KIR-based inhibitory CARs overcome CAR-NK cell trogocytosis-mediated fratricide and tumor escape”。

这项新的研究表明,一种称为“胞啃作用(trogocytosis)”的正常生理过程通过导致肿瘤抗原丢失、CAR NK细胞功能衰竭和自相残杀,导致了肿瘤逃逸和CAR NK细胞治疗后反应不佳。
论文通讯作者、德克萨斯大学MD安德森癌症中心干细胞移植与细胞治疗学教授Katayoun Rezvani博士说,“我们发现了CAR NK细胞治疗后肿瘤复发的新机制,我们还开发了一种策略来缓解这一过程。为此,我们设计了具有这种双靶向CAR NK细胞,它们能够忽略它们的同伴NK细胞表面因胞啃作用而获得的肿瘤抗原,并选择性地消除肿瘤细胞。”
在胞啃作用中,来自靶细胞的表面蛋白被转移到诸如NK细胞或T细胞之类的免疫细胞的表面上以调节后者的活性。论文第一作者、Rezvani实验室的研究生Ye Li及其同事们利用临床前模型发现,CAR激活促进了胞啃作用,从而导致肿瘤抗原转移和呈递到CAR NK细胞表面上。
这导致肿瘤细胞表面上的靶抗原减少,以及CAR NK细胞因自我靶向而出现的自相残杀。这种自我靶向导致NK细胞功能衰竭、代谢功能紊乱和抗肿瘤反应减弱。
通过研究临床试验中接受靶向CD19的CAR NK细胞(CD19 CAR NK)治疗的淋巴性恶性肿瘤患者的临床样本,这些作者证实,CAR NK细胞表面上CD19抗原水平较高与肿瘤细胞上CD19水平较低和肿瘤复发概率较高有关。
为了阻止这一过程的发生,这些作者给CD19 CAR NK细胞添加了一种旨在识别NK细胞特有的标志物的抑制性CAR,导致CAR NK细胞彼此之间在互动时收到“不要杀我”的信号,即使它们的表面携带肿瘤抗原。在临床前模型中,这些受到逻辑门控制的双靶向CAR NK细胞能够更好地专注于并只攻击肿瘤细胞,减少NK细胞功能衰竭和自相残杀的频率,并提高抗肿瘤活性。
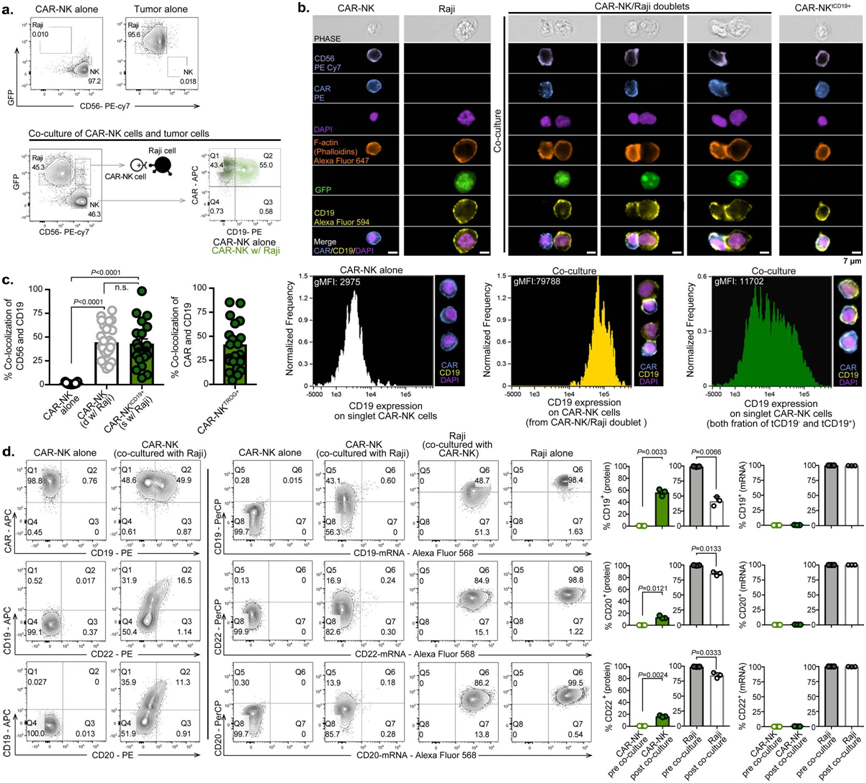
在体外,CAR介导的NK细胞中的CD19胞啃作用。图片来自Nature Medicine, 2022, doi:10.1038/s41591-022-02003-x。
Rezvani说,“阻止CAR NK细胞治疗后的肿瘤逃逸很重要,因为这导致了一些患者出现肿瘤复发。通过组织CAR NK细胞的功能衰竭和自相残杀,我们可以进一步提高它们的活性和功能。我们很高兴将这项研究转化为临床,因为这是可以任何CAR NK细胞疗法真正发挥作用的地方。”
这项新的研究建立在Rezvani实验室以前为推进和改进CAR NK细胞疗法所做的研究工作之上,包括一项针对白血病和淋巴瘤患者的临床试验,以及设计能够克服胶质母细胞瘤免疫抑制的CAR NK细胞的临床前研究。这项新的研究提供了对CAR NK生物学特性的进一步理解,并表明有必要对这种双靶向CAR策略进行临床评估。(生物谷 Bioon.com)
参考资料:
Ye Li et al. KIR-based inhibitory CARs overcome CAR-NK cell trogocytosis-mediated fratricide and tumor escape. Nature Medicine, 2022, doi:10.1038/s41591-022-02003-x.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


