新洞察!靶向p53介导的铁死亡或可治疗人类癌症和其他疾病
来源:本站原创 2022-02-18 18:45
虽然p53的常规活动如细胞周期阻滞、衰老和凋亡被公认为是应激反应中的主要检查点,但越来越多的证据表明,p53在其他肿瘤抑制机制中起到重要作用。
虽然p53的常规活动如细胞周期阻滞、衰老和凋亡被公认为是应激反应中的主要检查点,但越来越多的证据表明,p53在其他肿瘤抑制机制中起到重要作用。在这些非常规的活动中,一种铁依赖形式的非凋亡细胞死亡,称为铁死亡,引起了研究者们极大的兴趣。、
近日,哥伦比亚大学研究者在Cell Death &
Differentiation杂志上发表了题为“p53 in ferroptosis regulation:
the new weapon for the old guardian” 的综述性文章,本文综述了铁死亡在p53介导的肿瘤抑制中的作用,重点关注了肿瘤抑制过程中哪些细胞因子对p53依赖的铁死亡起关键作用,以及p53如何调节典型(gpx4依赖)和非典型(gpx4不依赖)铁死亡通路。
图片来源: https://doi.org/10.1038/s41418-022-00943-y
P53在调节铁死亡中起着重要而复杂的作用
各种应激可以激活p53发挥多种功能,包括经典功能(诱导细胞周期阻滞、衰老、凋亡、维持基因组稳定、调节代谢和自噬)。P53还影响肿瘤微环境和新出现的功能(调节铁死亡和干细胞),所有这些功能都有助于p53的肿瘤抑制作用。
典型的铁死亡途径
铁死亡有三个基本元素:脂质过氧化底物、脂质过氧化执行体和抗铁死亡系统,而破坏这些元素的平衡可导致铁死亡。
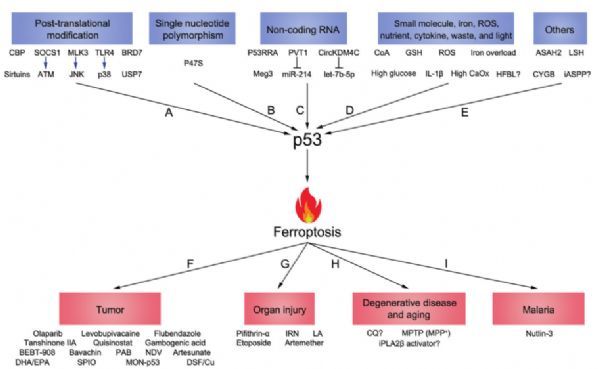
P53介导的铁死亡可以通过翻译后修饰、单核苷酸多态性、非编码RNA和营养因子等多种方式调节。目前,许多药物被证实可以在不同的疾病中影响p53-铁死亡途径,包括肿瘤、器官损伤、退行性疾病和衰老和疟疾。
P53介导的铁死亡的复杂性
图片来源:
https://doi.org/10.1038/s41418-022-00943-y
经过40多年的研究,p53作为肿瘤抑制因子的关键作用已是不争的事实。然而,关于p53究竟利用哪一种功能作为其抑制肿瘤生长的最终武器,一直存在争议。p53领域必须寻找这个关键问题的答案。铁死亡是一种新的调控细胞死亡的模式,已有大量研究结果表明p53在调节铁死亡中具有关键作用,为这一问题提供了新的线索。
本文简要介绍了铁死亡的经典模型。然后本研究还重点研究p53如何介导典型和非典型铁死亡通路,以及这些过程是如何被调控的。此外,研究者讨论了目前靶向p53调控的铁死亡治疗各种疾病,特别是肿瘤的方法。
综上所述,p53和铁死亡领域发展迅速,但仍有许多核心问题有待解决。随着研究成果的不断涌现,研究者们对p53和铁死亡的认识也越来越深入。出于科学和临床的原因,这些领域需要更多的研究来获得更丰硕的成果。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。