新冠疫情:3.4亿例!美国FDA批准扩大Veklury(瑞德西韦)适应症:治疗高危非住院COVID-19患者!
来源:本站原创 2022-01-23 01:34
在3期研究中,与安慰剂相比,Veklury将COVID-19相关住院或全因死亡的风险显著降低了87%。
2022年01月22日讯 /生物谷BIOON/ --根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2022年01月22日20时,全球累计确诊超过3.4亿例(3.4729亿),死亡超过560万例。
近日,吉利德科学(Gilead Sciences)宣布,美国食品和药物管理局(FDA)已加快批准抗病毒药物Veklury(remdesivir,瑞德西韦)的补充新药申请(sNDA):用于治疗病情有高风险进展为严重COVID-19(包括住院或死亡)的非住院成人和青少年患者。此次批准扩大了Veklury的作用,该药目前是治疗COVID-19住院患者的标准抗病毒疗法。此次扩大适应症,允许Veklury在符合资格的门诊患者中使用,进行3天疗程的静脉输液治疗。FDA还扩大了Veklury的儿科紧急使用授权(EUA):纳入有高风险发生疾病进展的12岁及以下非住院儿童患者。
FDA的这些行动,正值奥密克戎(Omicron)变体导致COVID-19病例激增以及对多款抗SARS-CoV-2单抗药物(mAb)的敏感性降低。相反,Veklury靶向高度保守的病毒RNA聚合酶,从而保留了对现有受关注的SARS-CoV-2变异株的活性。体外实验室测试表明,Veklury保留了对抗奥密克戎(Omicron)变异株的活性。迄今为止,在已知的受关注的任何变异株中,还没有发现会显著改变Veklury靶向的病毒RNA聚合酶的重大基因改变。
在欧盟,Veklury于2021年12月获得批准扩大适应症:纳入不需要补氧、有升高的风险发展为严重COVID-19的成人患者。此前,Veklury在欧盟获得附条件批准,用于治疗需要补氧、伴有肺炎的COVID-19成人和青少年(年龄≥12岁,体重≥40公斤)患者。
此次FDA对sNDA的批准、儿科EUA扩展、以及最近美国国立卫生研究院(NIH)推荐将Veklury用于治疗非住院患者的更新治疗指南,均基于PINETREE 3期随机双盲安慰剂对照试验的结果。该试验在有高风险发生疾病进展的非住院COVID-19患者中开展,评估了3天疗程Veklury通过静脉(IV)给药治疗的疗效和安全性。562例患者以1:1的比例被随机分配,接受Veklury或安慰剂治疗。
结果显示:到第28天,与安慰剂组相比,Veklury治疗组发生COVID-19相关住院或全因死亡复合终点的风险显著降低了87%(0.7%[2/279] vs 5.3%[15/283],p=0.008)。在这项研究中,到第28天,2组均未观察到死亡。在该研究中,Veklury和安慰剂在各种门诊环境中的安全性相似,接受Veklury治疗的患者中最常见的治疗期不良事件(≥5%)为恶心和头痛。
吉利德董事长兼首席执行官Daniel O'Day表示:“瑞德西韦现在已帮助治疗了世界各地超过1000万COVID-19患者,并继续在减轻大流行方面发挥关键作用。基于最新数据,我们现在还了解到,除了帮助住院患者外,瑞德西韦在COVID-19感染的早期阶段也有效。在我们继续推进瑞德西韦以使更多患者在多种情况下受益的同时,我们也在推进我们的在研口服化合物。这是基于与瑞德西韦相同的抗病毒机制,目前我们的口服COVID-19抗病毒药物GS-5245的1期临床试验正在进行中。”
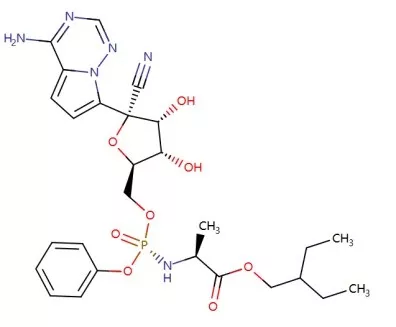
瑞德西韦-remdesivir化学结构式
Veklury(瑞德西韦)是吉利德科学公司的一款抗病毒药物,可以阻止新型冠状病毒(SARS-CoV-2)的复制,这种病毒可引起新型冠状病毒肺炎(COVID-19)。Veklury一种核苷酸类似物,通过靶向病毒RNA聚合酶直接抑制SARS-CoV-2在受感染的细胞内复制。进入人体后,Veklury被转化为活性代谢物瑞德西韦三磷酸,然后结合到病毒RNA中,阻断病毒在宿主细胞内的复制。
迄今为止,在所有已知的病毒关注变异株和存疑变异株中,包括奥密克戎变异株,尚未发现任何可显著改变瑞德西韦靶向的病毒RNA聚合酶的重大基因变化。这提示瑞德西韦对奥密克戎变异株仍具有活性。
在美国,Veklury适用于治疗:年龄在12岁及以上、体重至少40公斤、住院、或非住院但有高风险进展为严重COVID-19(包括住院或死亡)的成人和儿童患者。根据紧急使用授权(EUA),Veklury还被授权用于体重3.5公斤至40公斤以下的儿科患者、或体重至少3.5公斤的12岁以下儿科患者。
在Veklury的扩大适应症下,证实有SARS-COV-2感染、有高风险发生COVID-19疾病进展的非住院成人和儿科患者(12岁及以上、体重至少40公斤),可推荐3天疗程治疗,以防止COVID-19疾病进展。对于未使用机械通气和/或ECMO的住院患者,建议使用5天疗程,并可根据需要延长至总共10天。需要机械通气和/或ECMO的危重患者应接受10天疗程的治疗。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


