gd2适配体介导的自组装纳米药物在神经母细胞瘤治疗中的靶向多重治疗
来源:本站原创 2021-11-18 14:14
目前主流的抗糖脂GD2治疗神经母细胞瘤(NB)存在不良反应严重等局限性,需要改进治疗方法。
目前主流的抗糖脂GD2治疗神经母细胞瘤(NB)存在不良反应严重等局限性,需要改进治疗方法。在本研究中,作者开发了一种GD2适配体(DB99),并构建了一种有效、精确、生物相容性好的多功能纳米药物(ANM),用于NB的化疗和基因治疗。DB99能与GD2+ NB肿瘤细胞结合,但与GD2细胞的交叉反应极小。
此外,ANM是通过自组装合成的适配体DB99和nb特异性MYCN小干扰RNA (siRNA),然后自组装化疗药物阿霉素(Dox)而形成的。ANM在体外能特异性识别、结合和内化GD2+,但不能识别GD2,NB肿瘤细胞。ANM细胞内传递可激活Dox释放用于化疗和MYCN- sirna诱导的MYCN沉默。ANM特异性靶向并选择性聚集于体内GD2+肿瘤位点,进而诱导体内GD2+肿瘤的生长抑制; 此外,ANM在健康组织中产生的副作用更少或没有副作用,从而导致显著的更长的生存期和更少的副作用。这些结果表明,gd2适配体介导的靶向给药系统可能在NB的精准治疗中具有潜在的应用价值。
图片来源:https://doi.org/10.1016/j.omtn.2021.08.021.
神经母细胞瘤 (NB) 是婴儿和儿童最常见的颅外实体瘤,起源于交感神经系统,占儿童癌症死亡人数的 15%,是全球儿科医学死亡的主要原因。根据国际神经母细胞瘤危险组(INRG)的分类,NB分为低、中、高危险组。虽然高危NB (HRNB)是最普遍的,但与低危和中危组相比,高危组的预后相当差。临床HRNB主要包括大于18个月的儿童,伴有MYCN癌基因的远处转移和/或扩增。
目前,尽管有常规或大剂量化疗、手术切除、放疗、分化治疗和免疫治疗等多种联合治疗,HRNB的5年总生存期(OS)尚未发生实质性变化。高强度、高剂量的化疗通常会导致严重的后遗症,如听力损失、认知障碍和内分泌疾病。此外,有一半的HRNB患者可能会复发,5年后的存活率甚至更低,不到10%。与当前的护理标准治疗相关的高死亡率和与治疗相关的高发病率表明迫切需要对该疾病进行毒性更小、更有效的治疗。因此,迫切需要利用 NB 的分子病理学并提高靶向能力以降低长期毒性的新药物来治疗诊断时的高危 NB 以及复发或难治性疾病患者。
尽管以NB为重点的早期临床试验中有前景的药物越来越多,但用于小儿NB的新药开发仍然非常有限。糖脂 GD2 是 NB 治疗的有希望的靶点之一,但迄今为止,只有一类抗 GD2 单克隆抗体 dinutuximab 的免疫疗法已被纳入一线治疗(2015 年获得美国食品和药物管理局的批准 [FDA ]) 用于自 1980 年代以来患有 HRNB 的儿科患者。迪努妥昔单抗与糖脂GD2结合,糖脂GD2在NB细胞和神经外胚层来源的正常细胞中过表达,包括中枢神经系统和周围神经。
Dinutuximab在细胞表面与GD2结合,诱导抗体依赖的细胞介导的细胞毒性(ADCC)和补体依赖的细胞毒性(CDC)。尽管迪努昔单抗有强大的作用,但仍然存在挑战。首先,超过50%的患者会复发,很少有复发患者能治愈。第二,虽然GD2在NB肿瘤细胞上高表达,是NB治疗的理想靶点,但在其他正常组织中也存在GD2。
因此,迪努妥昔单抗刺激正常的GD2+细胞,导致严重疼痛、发热、血小板计数低、输液反应、低血压、肝酶升高、贫血、腹泻、低钾血症、毛细血管漏综合征、中性粒细胞减少和淋巴减少。迪努妥昔单抗治疗可能导致神经损伤、感染、眼部问题、电解质异常和骨髓抑制。因此,迫切需要开发一种替代的gd2靶向制剂来克服这些障碍。
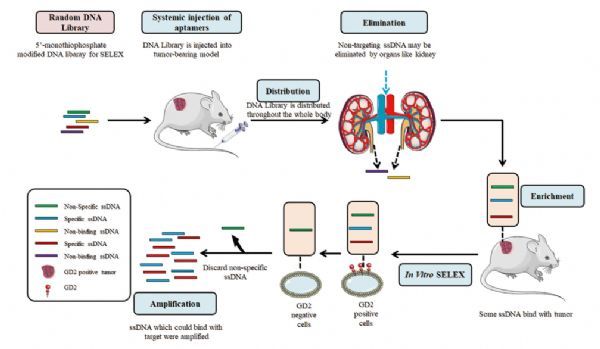
组合SELEX选择系统的示意图。
图片来源:https://doi.org/10.1016/j.omtn.2021.08.021
在本研究中,作者试图构建一个gd2 -适配体靶向系统。作者成功地选择了一个DNA适配体(DB99)对抗GD2。经验证,DB99可以与GD2+细胞结合,具有很高的特异性和亲和力。进一步,作者构建了基于GD2适配体的多功能生物可降解适配体纳米药物(ANM)。由于大约20%的NB病例和大约50%的高危病例中观察到MYCN癌基因的扩增,MYCN扩增被定义为最不利的预后标志之一。
MYCN mRNA表达的降低可能抑制NB肿瘤细胞增殖,防止多药耐药(MDR),并诱导细胞凋亡。此外,阿霉素(Dox)是一种标准的NB化疗药物,阿霉素可以插入胞嘧啶/鸟嘌呤(CG)碱基对。因此,作者构建了一个包含GD2适配体、MYCN siRNA和Dox的生物稳定和生物相容性ANM。作者假设ANM能够识别并结合GD2+细胞是因为GD2适配体。
然后,ANM被GD2+细胞内化,Dox和MYCN siRNA被释放执行其功能。因此ANM可抑制GD2+ NB肿瘤的生长。多项体内、体外功能研究表明,ANM既能实现GD2+细胞靶向化疗,又能实现mycn基因特异性治疗,是一种联合治疗,不仅疗效更佳,而且对正常细胞和组织的非特异性毒副作用更小。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。