免疫学新药!赛诺菲首创口服可逆BTK抑制剂rilzabrutinib治疗天疱疮3期临床失败!
来源:本站原创 2021-09-10 02:45
rilzabrutinib是一款口服可逆共价BTK抑制剂,正开发用于治疗免疫介导性疾病。
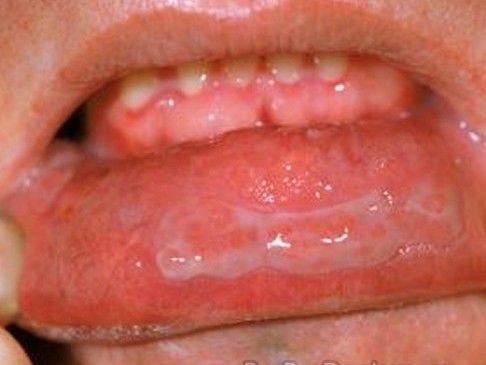
寻常型天疱疮(图片来源:healthfoxx.com)
2021年09月09日讯 /生物谷BIOON/ --赛诺菲(Sanofi)近日宣布,评估rilzabrutinib治疗天疱疮(pemphigus)的3期PEGASUS研究没有达到主要终点和关键次要终点。该研究中,rilzabrutinib的安全性与以前的结果一致,没有发现新的安全信号。天疱疮是一种罕见的自身免疫性疾病,特征是皮肤和粘膜出现水疱和溃疡。
rilzabrutinib是一款潜在首创(first-in-class)口服布鲁顿酪氨酸激酶(BTK)抑制剂,融入了赛诺菲的TAILORED COVALENCY®技术,目前正被开发用于治疗免疫介导性疾病。BTK是一种细胞内信号分子,参与某些免疫介导性疾病的先天性和适应性免疫反应。通过抑制BTK,rilzabrutinib具有靶向疾病发病机制的潜力。此前,美国FDA已授予rilzabrutinib治疗寻常型天疱疮和免疫性血小板减少症(ITP)的孤儿药资格(ODD)和快速通道资格(FTD)。在欧盟,rilzabrutinib被授予治疗天疱疮的孤儿药资格。
值得一提的是,3期PEGASUS研究是首个BTK抑制剂治疗天疱疮的安慰剂对照研究,入组的是患有中度至重度寻常型天疱疮(pemphigus vulgaris)或落叶型天疱疮(pemphigus foliaceus) 的成人患者。主要终点是从第29周至第37周期间使用最小剂量皮质类固醇的完全缓解(≤10mg/天)。完全缓解定义为没有新的和已存在的皮损。结果显示,rilzabrutinib治疗组达到主要终点的患者比例与安慰剂组无显著差异。目前,赛诺菲正在继续评估数据,并计划在未来的医学会议上分享详细结果。
赛诺菲全球发展、免疫学和炎症主管Naimish Patel表示:“虽然这些结果令人失望,但我们相信rilzabrutinib临床项目在解决免疫介导疾病患者中未满足的治疗需求方面具有巨大潜力。我们的使命是通过探索新的科学方法和新疗法来提高护理水平,从而改善治疗结局。我们致力于进一步研究rilzabrutinib,并推进我们的临床项目,为患者提供新的治疗选择。”
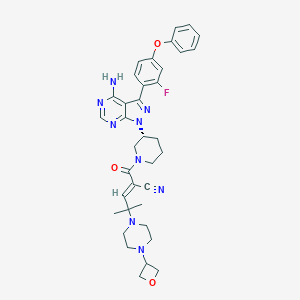
rilzabrutinib化学结构式(图片来源:pubchem)
天疱疮是一组潜在的危及生命的疾病,其特征是皮肤和粘膜出现水疱和溃疡。目前,天疱疮(包括寻常型天疱疮和落叶型天疱疮)的治疗选择有限,系统性皮质类固醇治疗仍然是标准护理方案。
rilzabrutinib是一种潜在的首创、可逆、共价、口服布鲁顿酪氨酸激酶(BTK)抑制剂,用于治疗免疫介导疾病。BTK酶在许多免疫过程中起着关键作用,包括B细胞扩增、免疫球蛋白的产生和固有免疫细胞(如肥大细胞、嗜酸性粒细胞和嗜碱性粒细胞)的激活。
来自BTK抑制剂安慰剂对照研究的阳性临床试验数据显示,BTK在类风湿性关节炎和慢性自发性荨麻疹中具有潜在作用。因此,BTK的功能在生物学上是多样的,并支持对一系列涉及BTK的严重未满足需求的疾病进行持续研究。
目前,rilzabrutinib正在3期临床试验中评估治疗罕见血液疾病免疫性血小板减少症(ITP),在2期临床试验中评估治疗自身免疫性IgG4相关疾病。rilzabrutinib治疗哮喘、特应性皮炎、慢性自发性荨麻疹和温热性自身免疫性溶血性贫血在内的免疫性疾病的额外2期研究预计在2021年启动。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


