Neurobiology of Stress:童年不幸意味着与压力和情绪增加相关的脑肠改变
来源:本站原创 2021-06-25 16:18
大脑-肠道系统的改变与各种疾病状态有关,但对早期生活逆境(ELA)如何通过大脑-肠道相互作用影响发育和成人健康知之甚少。作者假设,ELA扰乱了大脑-肠道系统的组成部分,从而增加了对情绪紊乱的易感性。在128名健康成年参与者的样本中,使用有效问卷评估了ELA病史和目前的压力、抑郁和焦虑。粪便代谢物的测定使用基于液相色谱-串联质谱法的非靶向代谢组谱。通过磁共振成
大脑-肠道系统的改变与各种疾病状态有关,但对早期生活逆境(ELA)如何通过大脑-肠道相互作用影响发育和成人健康知之甚少。作者假设,ELA扰乱了大脑-肠道系统的组成部分,从而增加了对情绪紊乱的易感性。在128名健康成年参与者的样本中,使用有效问卷评估了ELA病史和目前的压力、抑郁和焦虑。粪便代谢物的测定使用基于液相色谱-串联质谱法的非靶向代谢组谱。通过磁共振成像评价脑功能连接性。稀疏偏最小二乘判别分析,控制了性别、体重指数、年龄和饮食,作为ELA的函数被用来预测大脑-肠道的变化。ELA与谷氨酸途径中的四种肠道调节代谢物(5-氧脯氨酸、苹果酸、尿酸和谷氨酸γ-甲酯)以及主要感觉运动、突起和中央执行网络内功能性大脑连通性的改变相关。综合分析显示,这些代谢物、大脑功能连通性和感觉到的压力、焦虑和抑郁得分之间存在显著的相关性。这项研究揭示了ELA病史、大脑-肠轴的改变,以及对负面情绪和压力的易感性增加之间的一种新的联系。这项研究的结果提出了一种假设,即选择肠道调节的代谢物可能通过与谷氨酸兴奋毒性和氧化应激相关的途径,参与关键时期应激对神经发育的不利影响。
图片来源:https://doi.org/10.1016/j.ynstr.2021.100348
早年逆境(ELA)是一种已知的能够引起一系列发育变化的干扰因素,并与晚年对各种健康状况和精神障碍的易感性增加有关。在关键时期应对压力的系统变化包括外周基因表达、免疫功能和激素水平的失调,此外还有微生物群的扰动,所有这些都可能导致发育中的中枢神经系统(Cns)的直接变化。在这一早期编程阶段,肠道微生物群的参与及其与大脑的相互作用仍未被完全了解。作者之前已经提出,这可能是双向的:虽然大脑可能会影响肠道生理和微生物群的组成和功能的改变,但由此引起的肠道微生物群功能输出的改变可能会导致大脑的神经可塑性改变。从肥胖到肠易激综合征和炎症,ELA的历史都有报道,但到目前为止,很少有研究使用系统方法来研究暴露在ELA中的人类肠道代谢组和大脑的扰动。
ELA影响终生轨迹的一个主要途径是通过塑造大脑发育。先前的研究表明,ELA的病史主要与情绪调节和突显网络区域的改变有关,这些改变反过来可以影响与髓鞘形成和神经发生相关的表观遗传过程。这些神经变化也与过度觉醒和情绪调节困难,以及后来的负面情绪状态的发展有关。特别是,在从国际孤儿院领养的青少年中,前额叶皮质和海马体积持续减少,有童年虐待史的女性青少年表现出皮层网络组织的改变,这介导了精神结果。啮齿动物的研究也显示了类似的发现,但分辨率提高了:例如,母体分离与杏仁核基底外侧轴突向前额叶皮质的神经支配加速相关,雌性在成熟过程中表现出这些区域之间的功能连通性降低,焦虑样行为增加。
除了神经发育,肠道对ELA也很敏感。肠道微生物群的发育与许多早期发育因素有关,特别是与母亲压力、饮食和疾病、分娩方式、早期营养/母乳喂养和抗生素接触有关的因素。在青年队列中,早期的生活逆境不仅与胃肠道症状和后来的焦虑有关,而且与微生物多样性有关,分类学上的丰富可以预测前额叶皮质的活性。在孕妇样本中,早期逆境与普氏杆菌呈正相关,皮质醇与Rikenellaceae和Dialister呈正相关,与类杆菌呈负相关,提示早期逆境、当前应激与肠道微生物区系之间存在交互作用。此外,肠道向大脑发出的信号可以由肠道微生物直接产生的代谢物介导,也可以通过宿主细胞对微生物信号的反应间接产生。例如,与移植了非抑郁微生物区系的无菌鼠相比,将抑郁症患者的微生物区系移植到无菌小鼠可促进焦虑和抑郁相关的行为;这些相互作用是通过选择性调节涉及碳水化合物和氨基酸新陈代谢的微生物和宿主基因来实现的。此外,微生物群衍生的短链脂肪酸在直接输送到结肠时可改善人类应激诱导的皮质醇释放,在口服时可缓解啮齿动物的早期慢性应激,进一步强调了脑-肠道-微生物群轴与应激之间的潜在关系。
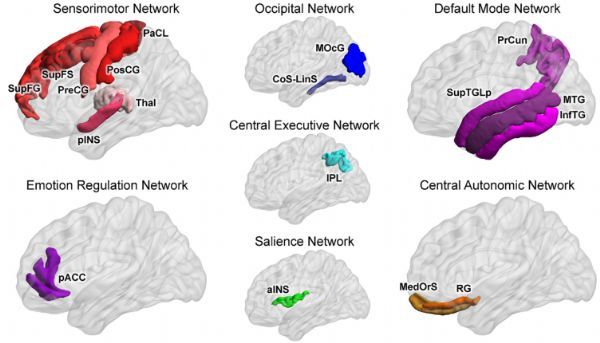
早年逆境影响多个大脑网络大脑区域
图片来源:https://doi.org/10.1016/j.ynstr.2021.100348
虽然动物模型的发现支持肠道微生物群在调节ELA对神经发育的不利影响方面的作用,但在人类中缺乏对这些相互作用的全面调查。尽管横断面和回顾性数据存在众所周知的局限性,但在这里,作者测试了主要假设,即肠道微生物代谢物中ELA相关的改变与大脑连通性的改变、情绪紊乱以及成年后对压力的易感性增加有关。
作者在有ELA病史的人类受试者中的发现表明,可能支持这样一种假设,即大脑和肠道发育关键时期的创伤经历塑造了大脑-肠道相互作用的长期变化。作者认为,这可能是通过ELA对参与情绪调节和自主神经系统输出的大脑网络的特征性影响,以微生物调节的代谢物的形式潜在地改变肠道微生物功能而发生的。观察到的谷氨酸通路的失调可能会导致兴奋性毒性和氧化应激,扰乱神经回路组装和现有的大脑网络连接,并增加患焦虑和抑郁的风险。总体而言,这项研究的结果提供了ELA对大脑-肠道改变的临床证据,并进一步为评估微生物群在介导ELA对大脑发育和晚年行为的不利影响方面的潜在作用奠定了坚实的基础。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。