4月Nature杂志不得不看的重磅级亮点研究
来源:本站原创 2021-04-30 16:42
时间总是匆匆易逝,转眼间4月份即将结束,在即将过去的4月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!皮质酮可恢复ADX小鼠正常的毛发周期进展。图片来源:Nature, 2021, doi:10.1038/s41586-021-03417-2。【1】Nature:放轻松也许可以治疗脱发!新研究揭示慢性压力调控毛囊干
时间总是匆匆易逝,转眼间4月份即将结束,在即将过去的4月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!
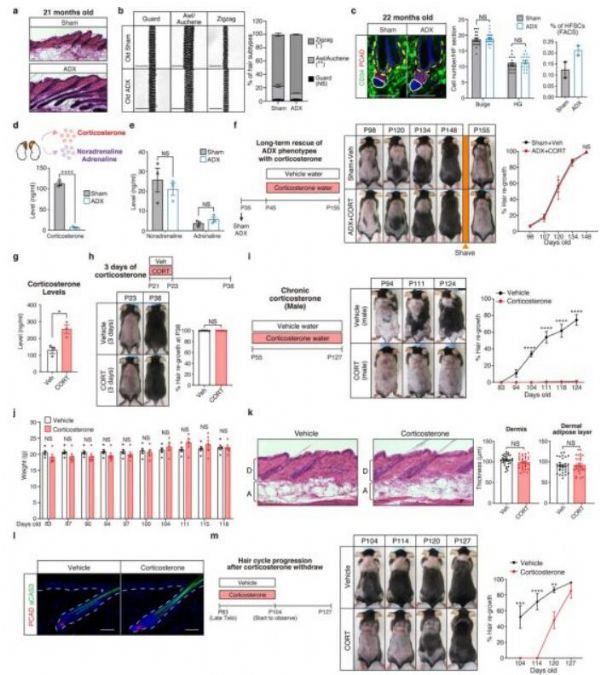
皮质酮可恢复ADX小鼠正常的毛发周期进展。
图片来源:Nature, 2021, doi:10.1038/s41586-021-03417-2。
【1】Nature:放轻松也许可以治疗脱发!新研究揭示慢性压力调控毛囊干细胞机制
doi:10.1038/s41586-021-03417-2
当美式橄榄球四分卫Aaron Rodgers在一个赛季糟糕的开局后告诉球迷们放松一下时,他几乎不知道自己这也是给出头发护理建议。在COVID-19大流行一年后,他的建议现在特别有用。约有四分之一感染新冠病毒的人在症状发生六个月后出现脱发,这可能是由于感染和恢复的折磨导致的全身性冲击。长期以来,慢性压力(也称为慢性应激)与脱发有关,但是将压力与毛囊干细胞功能障碍联系起来的内在机制尚不清楚。美国哈佛大学的Ya-Chieh Hsu博士及其团队在一项针对小鼠的新研究中揭示了这种联系。相关研究结果于2021年3月31日在线发表在Nature期刊上,论文标题为“Corticosterone inhibits GAS6 to govern hair follicle stem-cell quiescence”。
在一个人的一生中,毛发生长周期经历三个阶段:生长期(anagen)、退行期(catagen)和休止期(telogen)。在生长期中,毛囊不断地把正在生长的毛干(hair shaft)推出去。在退行期,毛发生长停止并且毛囊的下部收缩,但毛发(如今称为杵状毛)保持在原位。在休止期,杵状毛(club hair)保持休眠状态一段时间,最终脱落。在严重的压力下,许多毛囊会过早进入休止期,毛发会迅速脱落。
毛囊干细胞(HFSC)位于毛囊的一个隆起区域。这些干细胞通过解释内部和外部信号在控制毛发生长中起着至关重要的作用。比如,在休止期,HFSC保持静止状态,因此不会发生分裂。当在下一个生长期开始毛发生长时,HFSC经信号指导后发生分裂并产生祖细胞。然后,这些祖细胞开始分化的过程,产生几层毛囊,最终形成毛干。
自HFSC在30年前在这个隆起区域发现以来,许多调节分子,比如基因转录因子和信号蛋白,已显示出可控制这些干细胞的静止和激活。几乎所有这些调节物都是由HFSC或其邻近细胞(包括真皮乳头细胞)产生的,其中真皮乳头细胞通常充当HFSC的支持性“壁龛(niche)”。但是,诸如慢性压力之类的系统性疾病如何影响HFSC的活性尚不完全清楚。
为了回答这个问题,Hsu团队首先通过外科手术将肾上腺从小鼠身上移除,以便测试它在调节毛发生长中的作用,其中肾上腺产生压力激素(也称为应激激素)并是一种重要的内分泌器官。这些移除肾上腺的小鼠(该团队称为ADX小鼠)的毛囊的休止期要短于对照组(少于20天,而对照组为60~100天),毛囊参与毛发生长的频率大约是对照组的三倍。通过给ADX小鼠喂食皮质酮(一种通常由小鼠肾上腺产生的应激激素),他们能够抑制这种频繁的毛发生长并恢复正常的毛发周期。有趣的是,当他们不可预知地对正常小鼠施加各种轻度压力达九周之久时,他们观察到皮质酮水平升高,并伴随毛发生长减少,这支持了肾上腺在慢性压力下产生的皮质酮抑制毛发生长的想法。
最后,Hsu团队发现GAS6可以促进HFSC中参与细胞分裂的几个基因的表达,而不干扰已知的转录因子和信号通路。因此,他们可能发现了一个以前未知的通过促进细胞分裂直接刺激HFSC激活的机制。在老化的皮肤中,大多数祖细胞携带DNA突变---包括经常在皮肤癌中发现的有害突变---而不形成肿瘤。观察强制GAS6表达是否可以在无意中释放这些静止的但可能含有突变的HFSC的生长潜力,这一点将是至关重要的。
【2】Nature:重磅!揭秘神经细胞如何进行DNA损伤修复的过程
doi:10.1038/s41586-021-03468-5
DNA修复缺陷常常导致神经发育异常和神经退行性疾病,这就强调了DNA修复在神经元有丝分裂的特殊重要性。细胞基因组持续不断地受到攻击,导致内源性DNA损伤。但令人惊讶的是,很少有人知道DNA修复缺陷累积在神经元病变中的作用以及它们是否在整个过程中累积形成特定基因组。基于此,美国国立卫生院癌症研究中心 (NIH/NCI) André Nussenzweig课题组,国家神经疾病与中风研究所 (NIH/NINDS) Michael Ward课题组和英国萨塞克斯大学Keith W。 Caldecott教授合作在《Nature》以Accelerated Article Preview形式发表了题为“Neuronal enhancers are hotspots for DNA single-strand break repair”的文章来尝试回答以下几个问题:是否能够检测神经细胞内源的DNA损伤修复过程,定位它们在基因组上什么位置,损伤的类型是什么,是如何被修复的以及来源。
DNA修复的一个必要和特征性的步骤是填补缺口使用长链作为模板替换切除或缺失的核苷酸。 如果足够数量的核苷酸是结合,DNA修复合成可以用作程度的代理和内源性DNA损伤的位置。 鉴于此,该研究团队开发了一种通过测序绘制DNA修复合成位点的方法(与repair测序相关的合成;SAR-seq)。该研究团队标记了有丝分裂后ipsC衍生的谷氨酸能神经元在一天用EdU分化18小时后,生物素化标记的DNA,通过超声波将其降低到150-200 bp。
接下来,该研究团队在复发基因组中发现了55000个SAR-seq峰神经元的位置,这是高度重复性之间的不同实验。没有引起峰值通过S期的DNA合成因为i3神经元是有丝分裂后的和SAR-seq峰不受复制性DNA聚合酶α抑制的影响。相比之下,正如预期的那样,神经元SAR在很大程度上被阻止羟基脲(HU),其降低了脱氧核糖核苷酸的可用性。SAR-seq峰宽约200-2000 bp(平均901 bp),每个峰可能包含多个DNA修复聚集位点。最突出的用EdU脉冲标记法检测神经元SAR-seq峰仅1小时,EdU掺入后接近饱和标记18小时。
最后,该研究团队发现与SAR-seq峰值相关的SSB是富含C/G核苷酸,该研究团队发现这些ssb可能是胞嘧啶的位点去甲基化。与此观点一致,CpG位点胞嘧啶的活性DNA去甲基化优先发生在增强子,是有丝分裂后神经元的活性比外周细胞类型高10倍,并生成SSB,它们是XRCC1关联的中间体,但是不与PNKP相关,BER32。通过十一主动去甲基化易位(TET)家族(TET1,TET2和TET3)酶通过5mC逐渐氧化成5hmC,5fC或5caC来启动,并且5hmC的稳态水平约占修改后的40%大脑中的胞嘧啶。虽然未来需要进行研究以确定SSB的确切来源神经元增强子,该研究团队的数据暗示胞嘧啶甲基化和神经元增强子去甲基化的循环是潜在的来源神经元位点特异性DNA单链断裂的研究。
【3】Nature:科学家揭示克罗恩病发病的新型遗传和细胞分子机制
doi:10.1038/s41586-021-03484-5
克罗恩病(CD,Crohn’s disease)是一种慢性炎性肠病,该病常伴随有患者机体的异常愈合和消化道通道狭窄或收缩的并发症,与克罗恩病相关的疾病并发症常常是由能检测并破坏有害细菌等病原体的巨噬细胞和能促进伤口愈合的成纤维细胞之间的相互交流所驱动的。近日,一篇发表在国际杂志Nature上题为“A myeloid–stromal niche and gp130 rescue in NOD2-driven Crohn’s disease”的研究报告中,来自美国西奈山伊坎医学院等机构的科学家们通过研究识别出了克罗恩病发病的遗传和细胞分子机制,相关研究结果有望帮助开发新型疗法来治疗诸如克罗恩病等慢性炎性疾病。
研究人员发现,阻断常见的细胞因子受体亚单位gp130或能让部分克罗恩病患者获益,同时也能补充针对中度至重度克罗恩病患者的标准化疗法,即抗肿瘤坏死因子疗法(抗TNF疗法),该疗法能利用TNF抑制剂作为药物来阻断产生TNF蛋白的白细胞,后者能够诱发机体炎症发生。研究人员分析了来自人类小肠和斑马鱼模型损伤小肠中的炎性和正常组织,结果发现,异常的巨噬细胞-成纤维细胞生境或许是由克罗恩病相关的NOD2基因突变所驱动的。
研究者Cho表示,这项研究我们阐明了一种全新的分子机制,即随着时间推移,NOD2突变如何通过改变新招募的血液中单核细胞的功能来介导机体的患病风险。同时研究结果还加强了目前研究人员进行一系列组织和血液分析的思路,旨在解决如何改善某些患者对抗TNF疗法无反应的状况。研究人员还开发了一种全新的体内和体外模型来定义克罗恩病进展的机制,这或能帮助开发新型疗法来有效治疗携带NOD2基因突变的患者。
综上所述,本文研究为阐明NOD2驱动的克罗恩病发病的分子机制及患者机体纤维化的发生提供了新的生物学见解,且阻断gp130蛋白的功能或能让克罗恩病患者获益,尤其是能够作为抗TNF疗法的补充疗法来改善患者的进一步治疗。
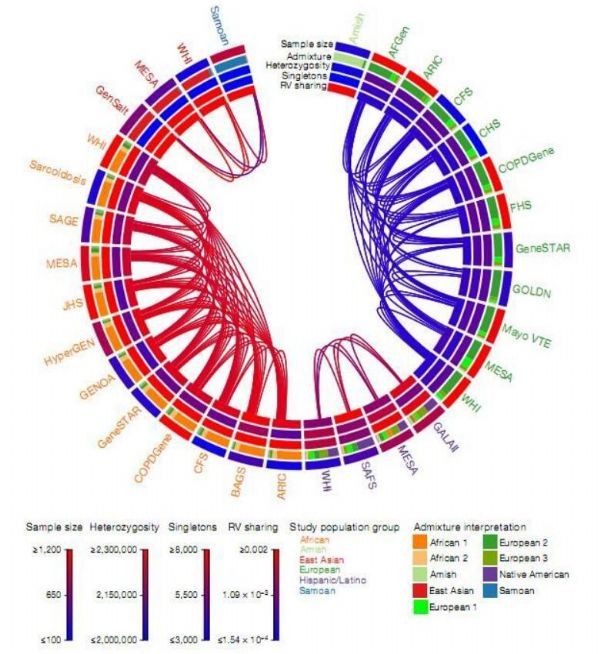
TOPMed研究中祖先、遗传多样性和罕见突变之间的遗传关联性。
图片来源:Taliun, D., et al. Nature 590, 290–299 (2021).doi:10.1038/s41586-021-03205-y
【4】Nature:通过对5万多人不同的全基因组进行测序来探究人类危险性疾病的成因
doi:10.1038/s41586-021-03205-y
先进DNA测序技术的开发及测序成本的降低让科学家们能以前所未有的规模来深入剖析并研究人类遗传突变,为了改善对人类健康的研究和理解,这些先进技术就应该被应用到表型良好的人类样本中,并用于建立一定的资源,比如变异目录、控制集合和推算参考面板等。日前,一篇发表在国际杂志Nature上题为“Sequencing of 53,831 diverse genomes from the NHLBI TOPMed Program”的研究报告中,来自弗吉尼亚大学等机构的科学家们通过对超过5.3万人机体全部遗传组成进行全新的分析,为了解影响人类心脏、肺脏、血液的功能和睡眠障碍的风险因素提供了新的见解,相关研究结果也能帮助研究人员找到更好的方法来治疗并预防引起机体残疾和死亡最常见的原因。
这项研究中,研究人员利用精准医学跨组学(TOPMed,Trans-Omics for Precision Medicine)项目分析了来自不同大洲的53,831名拥有不同背景的人群机体的完整基因组,其中大多数参与者都来自少数群体,而这些群体在遗传学研究中的代表性向来不足;所选代表人数的增加意味着科学家们能够更好地理解心脏、肺脏、血液和睡眠障碍影响少数群体的机制,并能有助于帮助减少这些人群长期存在的健康差距。
在所研究的参与者中,非洲裔人群机体中的基因变异水平最大,而本文中所得到的数据是科学家们有史以来得到的关于非洲裔人群的最好的研究数据。此外本文研究结果还为对特定基因突变的研究提供了新的思路,这些基因突变会降低人类因处方药而获益的能力,这或许是因种族和民族而异的。
TOPMed是一项重要的历史性努力成果,其旨在将代表性不足的少数群体参与者纳入到基因组学的研究中来,TOPMed的全基因组数据能为开发和检测调查人类突变的方法、腿短人类人口统计学和探索基因组的功能约束提供了非常宝贵的资源,除了这些用途外,研究者还推测,TOPMed数据未来将能够改善几乎所有正在进行的常见和罕见的疾病,其会提供关于健康个体的深入突变目录和相应资源,从而就能促进基于阵列的研究来实现此前只能通过直接测序来实现的数据完成性。
综上,TOPMed研究中广泛的遗传变异目录为探索罕见和非编码序列突变对表型突变的贡献提供了非常重要的研究线索和机会,此外,将TOPMed与现代手段相结合还能够改善全基因组关联性研究的能力和范围,其或会将突变的发生率降低到大约0.01%。
【5】Nature:重大进展!揭示T细胞耐受小肠中高浓度胆汁酸机制
doi:10.1038/s41586-021-03421-6
克罗恩病(Crohn's disease)起源于消化道(通常是小肠)的慢性炎症。在美国有超过50万人患有这种疾病。克罗恩病使人衰弱,需要反复手术来清除不可逆的受损肠道组织。克罗恩病患者通常使用强效的抗炎药物进行治疗,这些药物作用于患者的整个身体,而不仅仅作用于他们的消化道,这可能会产生意想不到的、通常是严重的副作用,比如降低对感染的抵抗力或减缓对癌症的抑制。在一项新的研究中,来自美国斯克里普斯研究所的Mark Sundrud博士及其团队发现小肠中的某些免疫细胞进化出一种分子感应机制,以保护它们自己免受那里高浓度胆汁酸的毒性作用。这种感应机制可以用药物类小分子来操纵,施加这类小分子后可减少Rag1或Rag2缺失的小鼠的小肠炎症。相关研究结果于2021年4月7日在线发表在Nature期刊上,论文标题为“CAR directs T cell adaptation to bile acids in the small intestine”。
这些作者指出这些称为效应T细胞的免疫细胞似乎学会了如何保护它们自身免受胆汁酸影响。这些T细胞利用整个基因网络与小肠中的胆汁酸安全互动,但是这种途径可能在至少一些克罗恩病患者中失灵了。胆汁酸在肝脏中制造,并在进餐时释放,以帮助消化和吸收脂肪和脂溶性维生素。它们在小肠末端的一个叫做回肠的区域中被活跃地重新捕获,在回肠那里它们穿过包含人体密集的肠道免疫细胞网络的组织层,最终重新进入血液并返回肝脏。由于胆汁酸是洗涤剂,如果系统变得不平衡,它就会引起毒性和炎症。这整个过程是靠一个复杂的信号系统来维持的。肝细胞和肠屏障细胞的细胞核中的受体都能感知到胆汁酸的存在,并在胆汁酸过多时告诉肝脏减少胆汁酸的产生,或者在胆汁酸不足以消化一顿牛排大餐时告诉肝脏产生更多的胆汁酸。
综上所述,这些作者发现CAR在浸润到小肠的T细胞中局部发挥作用,解毒胆汁酸,消解炎症。激活这种途径为治疗小肠克罗恩病提供了一种意想不到的策略。
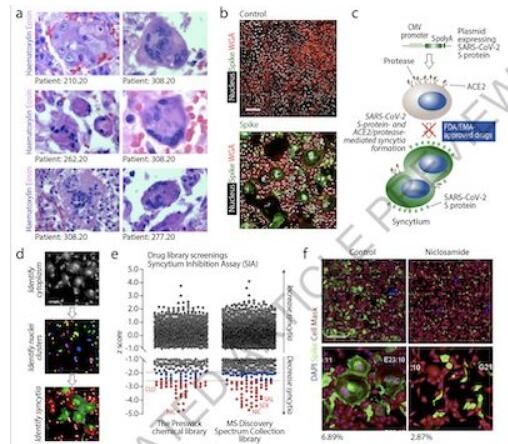
高通量筛选揭示能够抑制SARS-CoV-2感染引发合胞体产生的药物。
图片来源:Braga, L., et al. Nature (2021). doi:10.1038/s41586-021-03491-6
【6】Nature: 抑制TMEM16可有效阻断SARS-CoV-2感染引发的合胞体产生
doi:10.1038/s41586-021-03491-6
COVID-19疫情自爆发以来,仍旧严重影响着我们的生活,因此,对COVID19的疾病发生机理的研究以及相关药物的开发有助于缓解疫情,从而有助于使我们的生活尽快恢复正常。此前研究已经表明:COVID19是一种具有独特特征的疾病,包括肺血栓形成,频繁腹泻,炎症反应异常激活和肺泡水肿,肺功能快速恶化等。然而这些现象背后的病理基础仍然难以捉摸。
在最近发表在《Nature》杂志上的一项研究中,英国伦敦国王学院的Mauro Giacca团队对COVID-19患者的肺中受到感染的肺细胞进行了形态特征的分析,发现其形态异常且经常出现多核现象。这些合胞体的产生是由于SARS-CoV-2 Spike蛋白对受体细胞的刺激所致。基于这些观察结果,作者对超过3000种已批准的药物进行了两次高倍镜检,以寻找抑制Spike导致的合胞体产生的抑制剂。作者集中鉴定了抑制Spike介导的细胞融合的83种药物,并且将注意力集中在可以防止病毒复制和相关细胞病变的有效药物上。
作者希望找到抑制SARS-CoV-2 Spike介导的细胞融合的,已经被临床批准的药物。对此,他们开发了两种使用高内涵成像进行高通量筛选(HTS)的检测方法。第一个基于Vero和表达Spike的U2OS细胞之间的异源融合(细胞融合抑制分析,CFIA),第二个基于Vero细胞中Spike直接表达(合胞体抑制分析,SIA)。通过这两种方法,作者筛选了两个获得FDA / EMA批准的药物库(Prestwick化学库和The Spectrum Collection,MS Discovery)中的3825种药物。除去共同存在的药物分子之外,这两个库中共计3049种不同的小分子接受了筛选。
CFIA结果表明,Prestwick的57种药物和MS Discovery库的84种药物能够抑制Spike介导的融合,其中Niclosamide的命中排名在Prestwick库中最高,在MS Discovery库中排名第二。后续研究发现,其中最有效的分子之一是Niclosamide,它可以通过抑制TMEM16F / Anoctamin6(钙激活的离子通道和scramblase的活性,使细胞表面的磷脂酰丝氨酸暴露)而显著减弱Spike表达细胞中的钙振荡和膜电导反应。这些发现提示了COVID-19疾病发病机制的潜在机制,并强调了使用Niclosamide进行COVID-19治疗的潜力。
【7】Nature:科学家开发出了一种新型模型 或能绘制出与疾病基因相关的风险突变的多种图谱
doi:10.1038/s41586-021-03446-x
如今,全基因组关联性研究(GWAS)已经确定了数千种与多种人类疾病发生相关的遗传突变,但这些研究往往并不能确定基因突变到底会带来哪种特定的特征或疾病;近日,一篇发表在国际杂志Nature上题为“Genome-wide enhancer maps link risk variants to disease genes”的研究报告中,来自MIT博德研究所和哈佛大学等机构的科学家们通过研究开发了一种名为ABC模型(activity-by-contact)的新型模型绘制出了131种人类细胞类型和组织中的增强子-基因图谱。利用这些图谱,研究人员还将GWAS研究中超过5000种信号与包括癌症和心脏病在内的72种形状和疾病中近2250个基因联系了起来。
研究者表示,一般情况下我们很难解释疾病发生过程中出现的一些突变,当基因突变处于并不编码蛋白质的基因组特殊区域中时,其往往就很难被解释,比如被称之为增强子的区域,这些非编码元件能调节位于增强子较远距离的基因的活性,而且其在不同的细胞类型中作用也并不相同。如今在这种新型模型的帮助下,研究人员就实现了首次全面观察多种细胞类型的目的,同时研究人员还能准确预测这些非编码增强子和突变体的具体功能。
这种ABC模型能准确预测哪些增强子中含有可能会引发炎性肠病的基因突变,同时本文研究还提出了炎性肠病发病背后的一种可能性的生物学机制,同时为研究人员进一步研究其它疾病的调节性元件的功能奠定了一定的基础。研究人员开发的ABC模型能根据两种相对简单的因子来预测哪个增强子会调节哪个基因,即增强子与其靶向基因启动子接触的频率,以及增强子的活性水平。文章中,研究人员将这种模型应用到了能代表不同细胞类型、组织和细胞系的131份样本中,最终他们绘制出了100多张图谱来预测每一种样本中的增强子及其潜在的基因靶点。
这项研究帮助科学家们深入研究炎性肠病的发病机制向前又迈进了一步,如今炎性肠病在美国影响着大约300万成年人的健康,更广泛地讲,本文研究还能帮助研究人员锁定可能对特定疾病或特征非常重要的人类基因组的关键部分,本文研究或将加速理解突变功能的过程,因为如今研究人员能成功锁定所要研究的确切细胞类型和基因组合。如今研究人员利用来自其中一名参与者的数据产生了100多张增强子-基因图谱,后期他们希望能继续深入研究改进这种模型,并利用更多不同人群和细胞类型生成更多这样的图谱,从而为揭开人类疾病的发病机制提供更多线索。
综上,本文中研究人员开发了一种新型模型来预测哪些增强子会调节哪些基因的功能,并在多种细胞类型中利用CRISPR干扰证实了这种模型的有效性。此外研究人员还揭示了基因组调节的原则,并识别出了可能影响炎性肠病发生的关键基因,提出了一种资源和概括性的策略来将常见疾病的风险突变与特殊分子和细胞功能相联系起来。
doi:10.1038/s41586-021-03553-9
据Worldometers世界实时统计数据显示,截至北京时间2021年4月23日6时41分,全球累计确诊新冠肺炎(COVID-19)病例超过1亿4527万例,累计死亡病例超308.3万例,康复为1亿2324例。然而,多项研究显示,多数COVID-19康复者面临着各种各样的健康问题。近日,发表在 Nature杂志的一项研究显示,在确诊后六个月内,即使是轻度感染COVID-19的患者,死亡风险显著增加,而且随着病情的加重,死亡风险越来越高。另外,新冠不仅仅影响着呼吸道系统,可能长期影响着神经系统、心理健康、代谢疾病、心血管系统、胃肠道系统、肾脏、凝血调节、肌肉骨骼系统以及总体健康状况等。
在这项研究中,研究人员分析了美国退伍军人事务部的国家医疗数据库的数据,对73435例确诊COVID-19但未住院的患者进行死亡率以及后遗症全面探索,其中男性占88%。结果显示,初次感染30天后,COVID-19患者表现出更高的死亡风险,在随后的六个月内死亡风险增加了近60%。在6个月的时间里,所有COVID-19康复者中,估计每千名就有8例死亡。在病情严重到住院治疗的COVID-19患者中,在前30天都幸免于难,然而,在接下来的6个月中,每千名患者中有29例死亡。
研究人员进一步强调,“与流感相比,COVID-19在疾病的严重程度和器官系统受累范围方面均显示出更高的疾病负担。同时,随着COVID-19疾病的进展,患者将面临着更严重的健康风险。当然,随着时间的推移,有些健康问题会改善,比如呼吸急促以及咳嗦等,但有些疾病可能会变得更糟。”
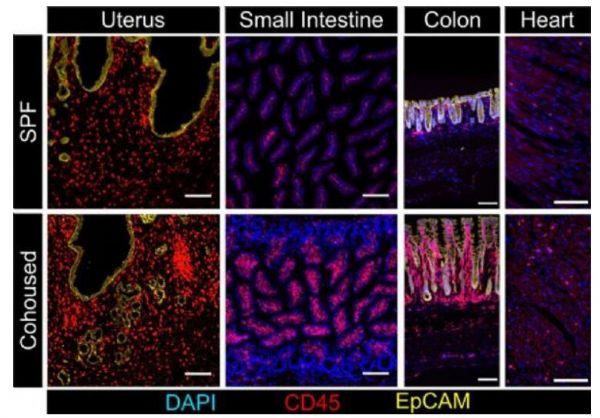
与宠物店小鼠共同居住的无特异性病原体的小鼠揭示了机体组织免疫力的扩大现象,
从而来响应人类样的微生物经历。
图片来源:Wijeyesinghe, S., et al. Nature 592, 457–462 (2021).
doi:10.1038/s41586-021-03351-3
【9】Nature:器官组织或在整个生命阶段会变得越来越有免疫力
doi:10.1038/s41586-021-03351-3
在后生动物中,特定任务往往会被放置到专门的器官中,而这些器官在发育早期就已经被建立起来了,其占据着离散的位置,通常能保持固定的大小;成人的免疫系统起源于一种能维持自我更新潜能的集中化的造血生境中,并能在成熟后分布于全身,从而来监测环境的扰动,并调节组织稳态及介导整个有机体的防御能力。近日,一篇发表在国际杂志Nature上题为“Expansible residence decentralizes immune homeostasis”的研究报告中,来自明尼苏达大学医学院等机构的科学家们通过研究发现,机体的器官或许会在整个生命过程中变得越来越具有免疫力,而这一观点或许会改变科学家们关于免疫接种规则和机体免疫系统功能方面的观点。
文章中,研究人员重点对T细胞免疫力进行了相关研究,他们旨在理解器官组织中T细胞的寿命,T细胞通常被认为能帮助机体抵御病毒侵袭的同时还能保护自身免受同一病毒的再次感染。研究者Saythi Wijeyesinghe说道,从历史来看,对机体免疫系统的研究一直强调利用骨髓、淋巴器官和血液的再生特性。而本文研究结果揭示了这种模式或许在很大程度上没有考虑到许多分布在机体其它器官中的免疫细胞,而大多数感染和肿瘤就是在这些器官中发生的,同时研究人员还揭示了免疫系统是如何来保护整个机体的健康并时刻监督外来病原体、组织损伤和肿瘤发生的。
综上,本文研究结果表明,“居住”(而并非更新或再循环)或能成为非淋巴细胞监视的重要特征,而器官作为适应性的存储库,或能容纳细胞免疫系统在整个生命阶段的持续扩张;尽管造血功能够帮助恢复免疫系统的某些功能,但非淋巴器官则能维持持续的组织自主化的细胞免疫积累,从而就会导致机体免疫平衡的逐渐分散。
【10】三篇Nature论文揭示细胞中细胞周期蛋白D降解机制,为开发新型抗癌药物奠定基础
doi:10.1038/s41586-021-03445-y doi:10.1038/s41586-021-03474-7 doi:10.1038/s41586-021-03422-5 doi:10.1038/d41586-021-00889-0
称为细胞周期蛋白D(细胞周期蛋白D1、D2和D3)的蛋白是驱动细胞分裂的细胞周期核心引擎的关键组成部分。如今,三项新研究对细胞周期蛋白D如何正常降解提供了寻找已久的答案。相关研究结果近期发表在Nature期刊上,论文标题分别为“CRL4AMBRA1 is a master regulator of D-type cyclins”、“The AMBRA1 E3 ligase adaptor regulates the stability of cyclin D”和“AMBRA1 regulates cyclin D to guard S-phase entry and genomic integrity”。
在细胞分裂过程中,细胞周期蛋白D结合并激活细胞周期蛋白依赖性激酶4(CDK4)和细胞周期蛋白依赖性激酶6(CDK6)。这些细胞周期蛋白-CDK4/6激酶给肿瘤抑制蛋白RB1、RBL1和RBL2添加磷酸基团,从而推动了细胞分裂。细胞周期蛋白D-CDK4/6激酶的不受控制激活是许多类型癌症发展的驱动力。
最近,随着CDK4/6激酶的小分子抑制剂进入临床,人们对细胞周期蛋白D-CDK4/6生物学的兴趣越来越大。这些化合物的临床试验结果令人瞩目,证明它们有能力延长乳腺癌患者的生存时间。CDK4/6抑制剂帕博西尼(palbociclib)、瑞博西尼(ribociclib)和阿贝西利(abemaciclib)被批准用于治疗晚期乳腺癌。此外,这些药物正在几百项临床试验中对许多不同类型的癌症进行测试。
第一项研究和第二项研究观察到在AMBRA1耗尽的细胞中形成抵抗CDK4/6抑制剂的细胞周期蛋白D-CDK2复合物,这很耐人寻味。这种“非典型”复合物以前被发现是对CDK4/6抑制产生获得性抵抗性的基础。这些作者推测,AMBRA1耗尽在某种程度上促进了这些细胞周期蛋白D-CDK2复合物的形成,这与细胞周期蛋白D水平的升高一起,导致了对CDK4/6抑制剂的抵抗性。第三项研究提出的一个特别令人兴奋的可能性是,CHK1抑制剂可用于治疗AMBRA1水平较低的对CDK4/6抑制剂有抵抗性的肿瘤。
对AMBRA1在人类癌症中的作用开展进一步研究是有必要的。AMBRA1的肿瘤抑制功能主要是由细胞周期蛋白D1或c-MYC介导的,还是也由其他靶标介导的?不再产生RB1的肿瘤细胞不需要细胞周期蛋白D来促进细胞周期进展,因此,如果细胞周期蛋白D是AMBRA1的主要靶标,那么预计在产生RB1的肿瘤中会观察到AMBRA1的缺失。此外,人类肿瘤中的AMBRA1缺失是否与影响细胞周期蛋白D羧基末端的突变相互排斥仍有待确定,这可能会使细胞周期蛋白D对AMBRA1介导的降解产生抵抗性。另一个未解决的问题是,正如第二项研究报告的那样,为何AMBRA1的低表达与高水平的细胞周期蛋白D1相关,并与具有特定类型基因改变(如Kras突变)的肺部肿瘤的不良生存率相关。对于那些具有编码EGFR蛋白的基因突变版本或具有野生型Kras的肺部肿瘤则没有观察到这种影响。不管这些问题的答案如何,这三项新的研究令人印象深刻,改善了科学家们对细胞周期进展机制的理解。(生物谷Bioon.com)
更多精彩阅读:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。