390亿美元!阿斯利康收购亚力兄(Alexion)顺利通过美国反垄断审查!
来源:本站原创 2021-04-18 01:10
此次收购,将充分扩展阿斯利康的治疗版图,进入医疗需求严重得不到满足、但高速增长的罕见病领域。

2021年04月17日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日宣布,随着《哈特-斯科特-罗迪诺反托拉斯改进法案》规定的等待期结束,对美国亚力兄制药(Alexion Pharmaceuticals)的收购已通过美国联邦贸易委员会(FTC)的审查,这标志着朝完成收购目标迈出了重要一步。
值得一提的是,这是阿斯利康于1999年由英国和瑞典的两家制药商合并成立以来,开展的最大一笔收购。此前,该笔收购案已在加拿大、巴西、俄罗斯和全球其他国家通过了竞争审查。目前,该笔收购案也正在等待额外的全球监管许可,包括限不限于英国、欧盟和日本。
阿斯利康执行董事兼首席财务官Marc Dunoyer表示:“这些批准进一步推动我们完成对Alexion的收购。我们仍然专注于阿斯利康和Alexion的下一个篇章,以我们在免疫学和精密药物方面的综合专业知识为基础,以及我们为全球患者带来更多创新药物的共同愿望。我们期待着在实现这一目标的过程中与其他全球权威机构密切合作。”
该收购计划于2020年12月首次宣布,以390亿美元的现金和股票形式。该收购将通过带来Alexion公司创新性的补体技术平台和强大的管线,增强阿斯利康在免疫学领域的科学地位。罕见疾病是一个高增长、迅速创新的疾病领域,医疗需求严重得不到满足。该收购预计将于2021年第3季度完成,但需获得额外的全球监管许可,并获得2家公司股东的批准,预计股东投票日期为2021年5月11日。
在成功完成收购的前提下,阿斯利康将成立一个专门的业务部门,即总部位于美国波士顿的“Alexion-阿斯利康罕见病部门”。阿斯利康将在初级、专科和高度专科护理领域扩大全球覆盖范围,预计到2025年实现2位数的收入增长、头3年实现2位数的核心每股收益(EPS)增长,以及强劲的现金流和增加股息。
目前,已知的罕见疾病超过7000种,只有约5%的疾病有获得美国FDA批准的治疗药物。预计未来全球罕见疾病领域的需求将以低2位数的百分比增长。
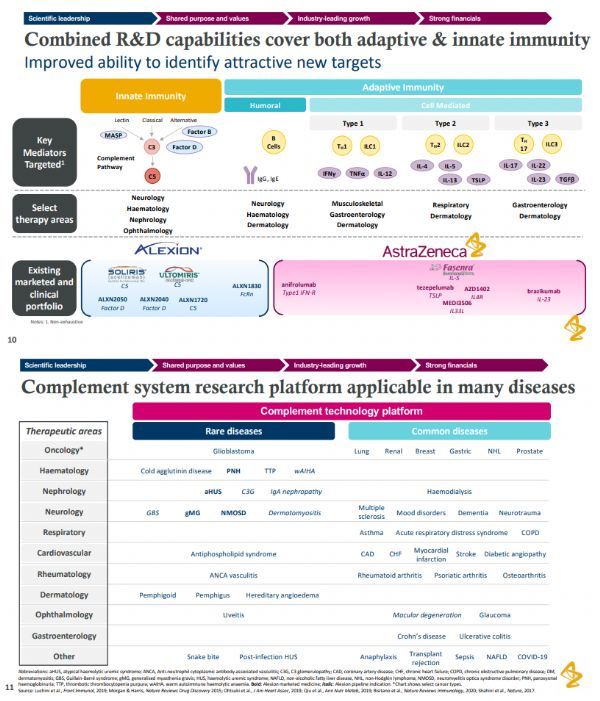
Alexion的产品、研发实力、补体技术平台(点击图片,查看大图)
Alexion是一家专注于罕见病创新药物开发的生物制药公司,其主要产品为2款补体抑制剂Soliris和Ultomiris。
Soliris是一种首创的C5补体抑制剂,通过抑制补体级联反应终端部分的C5蛋白发挥作用。补体级联反应是免疫系统的一部分,其不受控激活在多种严重的罕见病和超级罕见病中发挥了重要作用。
Soliris于2007年首次获准上市,目前已批准多种超级罕见病,包括:阵发性睡眠性血红蛋白尿(PNH)、非典型溶血尿毒症综合征(aHUS)、全身型重症肌无力(gMG)、视神经脊髓炎谱系障碍(NMOSD)。Ultomiris是Soliris的升级版产品,是第二代、长效C5补体抑制剂,于2018年底首次获批上市,已批准的适应症包括:PNH、aHUS。
Soliris是全球最畅销的罕见病药物之一,2020年销售额达到了40.65亿美元。Ultomiris在2020年的销售额已达到了10.77亿美元。2款C5抑制剂的销售总额达51.42亿美元。
除了上述2款C5补体抑制剂之外,Alexion还有2款罕见病药物Kanuma(sebelipase alfa)和Strensiq(asfotase alfa),前者治疗溶酶体脂肪酶缺乏症(LAL-D),后者治疗低磷酸酯酶症(HPP)。此外,Alexion公司管线中还有10多个资产,涵盖多个疾病领域。(生物谷Bioon.com)
原文出处:AstraZeneca receives US clearance of proposed acquisition of Alexion
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->