CAR-T细胞疗法研究进展(第20期)
来源:生物谷 2021-03-27 15:59
2021年3月27日讯/生物谷BIOON/---CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被 认为是最有前景的肿瘤治疗方式之一。正如所有的技术一
2021年3月27日讯/生物谷BIOON/---CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被 认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,CAR-T技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实 验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产 生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
近年来,CAR-T免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和心脏病等疾病,具有更广阔的应用空间。基于此,针对CAR-T 细胞疗法取得的最新进展,小编进行一番盘点,以飨读者。
1.Science:重大突破!开发出识别癌细胞表面上蛋白抗原表达水平的 CAR-T细胞,有望用于实体瘤治疗
doi:10.1126/science.abc1855
在CAR-T细胞疗法中,从患者体内提取T细胞进行基因改造:利用病毒载体将嵌合抗原受体(CAR)递送到T细胞中形成CAR-T细胞,使之更好地识别和杀死癌细胞。当CAR-T细胞在患者细胞中识别出所需的表面结构时,它们就会开始增殖并杀死靶细胞。CAR-T细胞疗法于2018年被引入芬兰,它已用于治疗白血病患者和淋巴瘤患者。到目前为止,CAR-T细胞疗法在实体瘤中的应用是困难的:当癌症类型与任何特定的表面结构不存在对应关系时,仅针对肿瘤进行治疗是困难的。在许多癌症类型中,肿瘤表面存在大量的特定蛋白,但该蛋白在正常组织中也存在较低的水平,重要的是,CAR-T细胞治疗无法区分不同细胞中同一种靶蛋白的表达水平。这就是为什么常规的经过基因改造的CAR-T细胞会迅速攻击健康的细胞和器官,从而导致治疗相关的致命不良反应。

人淋巴细胞的电子显微图,图片来自Dr. Triche/National Cancer Institute。
在一项新的研究中,来自美国加州大学旧金山分校和芬兰赫尔辛基大学的研究人员为CAR-T细胞用于治疗实体瘤找到了一种解决方案:他们发现了一种新的对CAR-T细胞进行编程的方法,使它们只杀死癌细胞,而放过与癌细胞具有相同蛋白标志物的健康细胞。
2.eLife论文解读!利用深度学习技术驱动的三维全息照相显微镜追踪和分析CAR-T细胞的免疫突触
doi:10.7554/eLife.49023
实时跟踪和分析嵌合抗原受体(CAR)T细胞(CAR-T)靶向癌细胞的动态变化,可以为癌症免疫疗法的开发开辟新的途径。然而,通过传统的显微镜方法进行成像可能会导致细胞损伤,而且对细胞与细胞之间的相互作用进行评估是非常困难和耗费人力的。然而,当将深度学习和三维全息显微镜应用于这项任务时,这不仅避免了这些困难,而且还发现人工智能(AI)比人类表现得更好。
人工智能正在帮助科学家们破译一种新的全息显微镜技术所获得的图像,以便调查癌症免疫疗法中“实时”发生的关键过程。人工智能将那些如果科学家们手动开展的非常耗费人力和时间的工作转变为不仅毫不费力,而且比他们自己做得更好。这项由韩国科学技术院(KAIST)的研究人员开展的研究近期发表在eLife期刊上,论文标题为“Deep-learning-based three-dimensional label-free tracking and analysis of immunological synapses of CAR-T cells”。
3.PNAS解析!开发出能靶向作用常见遗传突变的新型癌症免疫疗法!
doi:10.1073/pnas.2022410118
近日,一项刊登在国际杂志PNAS上题为“Targeting loss of heterozygosity for cancer-specific immunotherapy”的研究报告中,来自约翰霍普金斯大学医学院等机构的科学家们通过研究开发出了一种新型癌症免疫疗法原型,其或能对T细胞进行工程化修饰来靶向作用所有癌症中常见的遗传变异(genetic alteration);这种新方法能够刺激机体的免疫反应来抵御缺失一种基因拷贝的细胞,即杂合性丢失(loss of heterozygosity,LOH)的细胞。
基因拥有两个等位基因或拷贝,两个拷贝分别来自父母机体;癌症相关的基因改变通常就会涉及其中一个基因拷贝的丢失。研究者Kenneth Kinzler博士指出,这种拷贝丢失或LOH,是癌症发生过程中最为常见的遗传事件。新型癌症免疫疗法往往能将缺失的基因拷贝反转为免疫细胞激活信号;研究人员解释道,从历史上来看,尽管是癌症发生的标志,但这些缺失的基因拷贝却因为所编码蛋白的缺失而无法作为可行的新型疗法开发的治疗性靶点,而且目前并不能利用药物来对其进行靶向作用。然而免疫疗法以及利用嵌合抗原受体(CARs)激活通过工程学修饰的癌症杀伤性T细胞就会使得T细胞靶向作用LOH成为可能。
4.Blood:工程化开发的安全开关或能抑制CAR-T细胞免疫疗法治疗所产生的严重副作用!
doi:10.1182/blood.2021010784
近日,一项刊登在国际杂志Blood上的研究报告中,来自UNC Lineberger综合癌症研究中心等机构的科学家们通过研究成功利用一种实验性的安全开关降低了时有发生的疗法副作用的严重程度,这种安全开关能作为嵌合抗原受体T细胞疗法(CAR-T疗法)的一部分,而后者是一种新型的免疫疗法。这一研究进展是研究人员利用CAR-T疗法在治疗难治性急性B细胞白血病患者的临床试验中发现的,其证明了携带安全开关的CAR-T免疫疗法的扩大使用案例。
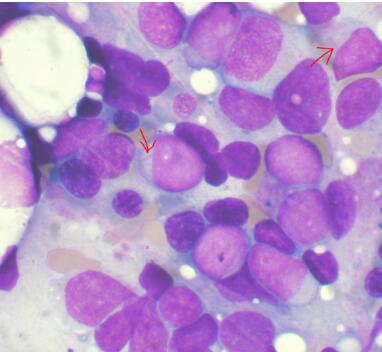
图片来源:Wikipedia。
在使用CAR-T疗法时,来自患者机体免疫系统的T细胞能被修饰来表达部分抗体结合癌细胞表面的蛋白,当输回患者体内后,修饰后的T细胞就能寻找并攻击患者机体全身的癌细胞,当利用这种疗法治疗时,白血病或淋巴瘤患者常常会经历疾病的完全缓解,但有时仍然会经历疗法的毒性作用,其或许是危及生命的,因为修饰后的T细胞会在患者体内诱发炎性反应或神经系统毒性作用。
5.Cytotherapy论文解读!靶向GXM多糖的CAR-T细胞疗法可控制隐球菌感染
doi:10.1016/j.jcyt.2020.11.002
一种基于细胞的创新癌症治疗方法被发现有希望控制由真菌引起的感染。在一项新的研究中,来自美国德克萨斯大学MD安德森癌症中心的研究人员报告称,使用经过编程识别隐球菌属真菌的嵌合抗原受体(CAR)T细胞(CAR-T)在体外和小鼠中都能有效地对抗感染。相关研究结果近期发表在Cytotherapy期刊上,论文标题为“Glucuronoxylomannan in the Cryptococcus species capsule as a target for Chimeric Antigen Receptor T-cell therapy”。
格特隐球菌(C. gattii)和新生隐球菌(C.neoformans)存在于有死亡有机物的土壤和被鸽子和其他鸟类的粪便污染的地方。它们会引起人类机体的系统性真菌病。它们可以感染肺部和中枢神经系统,引起脑膜炎。症状因感染部位不同而不同,有可能是致命的。人们通过吸入隐球菌进行传播。
6.BMJ子刊:剔除Cbl-b基因将CAR-T细胞变成精神焕发的实体瘤抗击战士
doi:10.1136/jitc-2020-001688
来自美国德克萨斯大学西南医学中心的研究人员领导的一项新研究表明,剔除单个基因可以将衰竭的称为CD8+ T细胞的抗癌免疫细胞重新变成精神焕发的战士,可以继续对抗恶性肿瘤。这一结果可能提供一种利用人体免疫系统攻击癌症的新方法。相关研究结果近期发表在Journal for Immunotherapy of Cancer期刊上,论文标题为“Deletion of Cbl-b inhibits CD8+ T-cell exhaustion and promotes CAR T-cell function”。
论文通讯作者、德克萨斯大学西南医学中心内科与免疫学副教授Venuprasad Poojary博士解释说,当CAR-T细胞进入实体瘤时,它们很快就会功能失调,失去抗癌能力。这种称为“衰竭”的状态伴随着它们表面上的PD1和Tim3等蛋白的增加,而且它们无法产生它们通常会产生的免疫诱导分子,如干扰素γ和肿瘤坏死因子。Poojary补充说,找到一种防止CAR-T细胞衰竭的方法已经成为癌症研究的重要目标。
为此,他和他的同事们搜罗了已发表的研究,比较了发挥作用的T细胞和衰竭的T细胞中的基因活性。他们很快就将目光锁定在了一个叫做Cbl-b的基因上,这个基因在衰竭的T细胞中更加活跃,或者说上调。
Poojary和他的同事们证实,在结肠癌小鼠模型的肿瘤浸润T细胞中,Cbl-b被激活。这些T细胞不仅失去了对抗肿瘤的能力,而且还出现了一组特征性的细胞表面蛋白,并且表达衰竭特征性的免疫分子。然而,当他们使用基因编辑工具CRISPR剔除这些细胞中的Cbl-b时,它们重新获得了抗癌能力,并失去了其他的衰竭特征。
7.NEJM论文解读!临床试验表明CAR-T细胞疗法在多发性骨髓瘤中产生深度的持续缓解
doi:10.1056/NEJMoa2024850
一项国际临床试验发现,在治疗多发性骨髓瘤方面的一项重大进展是,一种CAR-T细胞疗法使得先前在接受多种治疗后出现复发的患者获得了深度、持续的缓解。相关研究结果发表在2021年2月25日的NEJM期刊上,论文标题为“Idecabtagene Vicleucel in Relapsed and Refractory Multiple Myeloma”。
在这项临床研究中,来自美国、西班牙、法国、比利时、意大利、德国和加拿大的研究人员报告说,近75%的参与者对这种称为idecabtagene vicleucel(ide-cel,也称为bb2121)的CAR-T细胞疗法作出了反应,他们中的三分之一的人有完全缓解。这些研究人员表示,这种缓解反应的比率和持续时间,明显优于目前现有疗法对多次复发患者产生的缓解反应。
8.NEJM:大量非霍奇金淋巴瘤患者在接受CAR-T细胞治疗五年后仍然处于缓解状态
doi:10.1056/NEJMc2030164
在一项新的研究中,来自美国宾夕法尼亚州立大学的研究人员报道,在宾夕法尼亚大学佩雷尔曼医学院发起的一项临床试验中,大量的非霍奇金淋巴瘤(NHL)患者在接受嵌合抗原受体(CAR)T细胞(CAR-T)疗法(称为Kymriah)五年后仍然处于缓解状态。这些研究结果代表了迄今为止美国食品药物管理局(FDA)批准用于治疗复发性或难治性大B细胞淋巴瘤的CAR-T细胞疗法的最长随访发表数据。相关研究结果发表在2021年2月18日的NEJM期刊上,论文标题为“Five-Year Outcomes for Refractory B-Cell Lymphomas with CAR T-Cell Therapy”。
图片来源:Www.pixabay.com。
在24名弥漫性大B细胞淋巴瘤(DLBCL)(最常见的NHL形式)患者中,他们在标准治疗后癌症复发后接受了Kymriah,46%的患者获得了完全缓解,31%的患者在五年内实现了无进展生存。在14名接受Kymriah的复发或难治性滤泡性淋巴瘤(第二种最常见的NHL形式)患者中,71%的患者实现了完全缓解,43%的患者在五年内实现了无进展生存。
9.Blood:为何CAR-T细胞疗法会在某些淋巴瘤患者的治疗中失败?
doi:10.1182/blood.2020007445
嵌合抗原受体T细胞疗法(CAR-T细胞疗法)是治疗多种血液癌症疗法的重大图谱,比如急性淋巴细胞白血病和弥漫性大B细胞淋巴瘤;临床研究结果表明,患者治疗后两年的疾病总反应率超过80%,疾病持续反应率接近40%,然而免疫细胞疗法并不总是对每个患者都有效。来自Moffitt癌症研究中心的研究人员就一直在探索阐明为何相比其它患者而言,某些患者对CAR-T细胞疗法反应较好,以及应该怎么做才能够改善疗法的效率。日前一篇刊登在国际杂志Blood上的研究报告中,Moffitt癌症研究中心的科学家们就通过研究发现,免疫功能失调或会直接影响弥漫性大B细胞淋巴瘤患者接受CAR-T细胞疗法的反应和效率。
弥漫性大B细胞淋巴瘤是一种最常见的非霍奇金淋巴瘤,其是一种影响B淋巴细胞的恶性癌症,而B细胞则是机体中能帮助抵御感染的一类白细胞;YESCARTA (axicabtagene ciloleucel)就是一种被FDA批准用于治疗这类癌症的首个CAR-T细胞疗法;该疗法适用于顽固性或复发性疾病的患者,这意味着这些患者已经至少在两个以上的疗法中失败了。对于CAR-T细胞疗法而言,研究人员会通过一种单采过程收集患者机体自身的免疫细胞,随后在实验室中对这些细胞进行遗传修饰,添加嵌合抗原受体来帮助T细胞定位并杀灭患者机体中的肿瘤细胞。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


