新冠肺炎重大消息!罗氏/再生元抗体鸡尾酒REGEN-COV治疗非住院患者:住院/死亡风险降低70%!
来源:本站原创 2021-03-24 20:00
REGEN-COV是由2种单抗组成,既能治疗、又能预防COVID-19。

2021年03月24日/生物谷BIOON/--罗氏(Roche)与合作伙伴再生元(Regeneron)近日联合宣布,迄今为止评估一种COVID-19药物治疗受感染非住院患者(n=4567)的最大规模临床试验的结果为阳性。该试验在高危非住院COVID-19患者(门诊患者)中开展,评估了抗体鸡尾酒疗法REGEN-COV(casirivimab和imdevimab)的疗效和安全性。
结果显示,研究达到了主要终点:与安慰剂相比,REGEN-COV治疗将住院或死亡风险显著降低了70%(1200mg,静脉输注[IV])和71%(2400mg IV)。该研究中,REGEN-COV也达到了全部次要终点,包括将症状持续时间显著缩短4天。
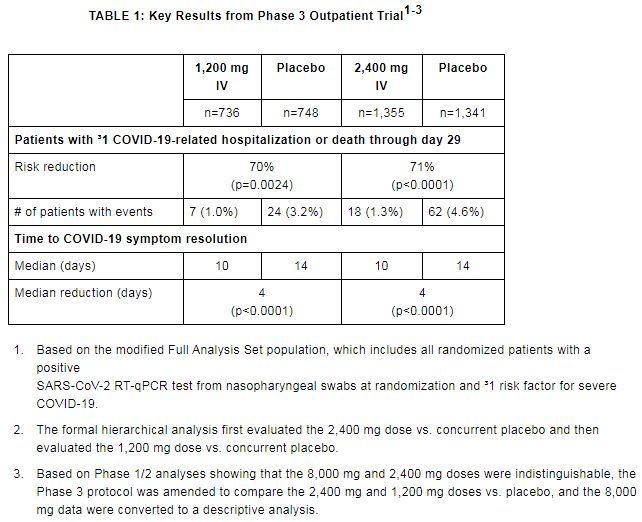
此外,一项伴随性的剂量范围2期试验表明,所有剂量(8000mg、2400mg、1200mg)在所有终点都有相似的疗效。此外即使在测试的最低剂量下(IV:300mg;皮下注射[SC]:600mg),在注射后的前7天中病毒载量也显著减少,与2400mg和1200mg IV相当。
最近,美国FDA更新了所有已授权的单克隆抗体疗法的美国紧急使用授权(US EUA)资料单(fact sheet),表明REGEN-COV是唯一一个对关键的新型变种保持效力的药物。再生元将立即与监管机构分享数据,并请求向EUA中添加较低的1200mg剂量。
该研究的调查员、新泽西州圣名医疗中心传染病主管Suraj Saggar表示:“这是对抗COVID-19的一个里程碑时刻,因为这项大型良好对照试验提供了确凿的结果,证明REGEN-COV可以显著降低门诊患者住院和死亡的风险。由于仍有非常多的人受到感染,以及最近的数据显示REGEN-COV能够解决新出现的变异,这些数据强调需要迅速采用REGEN-COV作为护理标准,为高危患者提供最佳机会,以减少住院或死亡等严重后果。”
该研究中,对直至第169天的所有可用患者数据进行了安全性评估,未发现新的安全信号。严重不良事件(SAE)主要与COVID-19有关,发生率1200mg组为1.1%、2400mg组为1.3%、安慰剂组为4.0%。1200mg组(n=827)有1例死亡,2400mg组(n=1849)有1例死亡,安慰剂组(n=1843)有5例死亡。
在此次分析中,所有患者至少有一个危险因素,包括肥胖(58%)、年龄50岁(51%)和心血管疾病,包括高血压(36%)。大约35%的患者是拉丁裔/西班牙裔,5%是黑人/非裔美国人,中位年龄为50岁(范围:18-96岁)。
再生元总裁兼首席科学官George D.Yancopoulos医学博士表示:“在美国,每天约有6万名新诊断的患者,有4万名患者因为COVID-19仍在医院。我们致力于与政府、医疗保健机构和其他机构合作,支持在适当的患者中迅速广泛采用REGEN-COV。我们将与监管机构讨论新数据,并要求将1200mg剂量迅速添加到美国紧急使用授权(EUA)中,以便使预期的REGEN-COV供应可用于治疗更多患者。这些3期研究数据也将构成完整的生物制剂许可申请(BLA)的基础。”

REGN-COV是由2种抗体(casirivimab和imdevimab)组成的一种鸡尾酒疗法,2种抗体分别针对SARS-CoV-2棘突蛋白受体结合区域的2个独立的、不重叠的位点,具有协同作用,可降低病毒变异逃逸的风险,并保护个体免受人群中已出现的棘突变体病毒的侵害。
REGN-COV开发用于治疗、预防COVID-19感染。2020年8月,罗氏宣布与再生元达成战略合作,开发、制造并向全球各地分发REGEN-COV。再生元负责美国的开发和销售,罗氏负责美国以外市场的开发和销售。REGN-COV有望为已经出现COVID-19症状的感染者提供一种急需的治疗选择,并且有潜力在已暴露于病毒的高风险人群中预防感染,从而减缓全球大流行的蔓延。
2020年11月,美国FDA授予REGEN-COV紧急使用授权(EUA),用于治疗最近确诊为轻度至中度COVID-19的高危人群,具体为:新型冠状病毒(SARS-CoV-2)直接检测法结果呈阳性、且有高风险发展为严重COVID-19和/或住院治疗、年龄≥12岁、体重≥40公斤的儿童和成人患者。目前的EUA中,REGEN-COV的静脉输注剂量为2400mg,输注时间可短至20分钟。
值得一提的是,REGEN-COV是2020年10月份美国前总统特朗普在治疗COVID-19时接受的3种药物中的一种,同时也是继2020年11月初礼来中和抗体bamlanivimab之后获得EUA的第二种抗体疗法。2020年11月9日,bamlanivimab被美国FDA授予EUA,用于治疗与REGEN-COV2相似的COVID-19患者群体。(生物谷Bioon.com)
原文出处:PHASE 3 TRIAL SHOWS REGEN-COV™ (CASIRIVIMAB WITH IMDEVIMAB) ANTIBODY COCKTAIL REDUCED HOSPITALIZATION OR DEATH BY 70% IN NON-HOSPITALIZED COVID-19 PATIENTS
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


