2020年10月Science期刊不得不看的亮点研究
来源:本站原创 2020-10-31 22:05
2020年10月31日讯/生物谷BIOON/---2020年10月份即将结束了,10月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Science:大多数人对SARS-CoV-2产生强劲的抗体反应,而且这种抗体反应至少在5个月内保持相对稳定doi:10.1126/science.abd7728在一项新的研究中,来自美国西
2020年10月31日讯/生物谷BIOON/---2020年10月份即将结束了,10月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:大多数人对SARS-CoV-2产生强劲的抗体反应,而且这种抗体反应至少在5个月内保持相对稳定
doi:10.1126/science.abd7728
在一项新的研究中,来自美国西奈山伊坎医学院的研究人员发现绝大多数感染轻度到中度COVID-19的人都会产生强大的抗体反应,这种抗体反应至少在5个月内保持相对稳定。此外,他们还发现这种抗体反应与人体中和(或者说杀灭)SARS-CoV-2(导致COVID-19疾病的冠状病毒)的能力相关。相关研究结果于2020年10月28日在线发表在Science期刊上,论文标题为“Robust neutralizing antibodies to SARS-CoV-2 infection persist for months”。
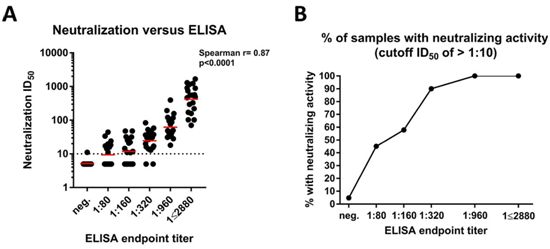
论文共同通讯作者、西奈山伊坎医学院疫苗学教授Florian Krammer博士说,“虽然有些报告说针对这种病毒的抗体很快就会消失,但是我们发现恰恰相反:90%以上轻度或中度患病的人都会产生足以中和这种病毒的抗体反应,而且这种抗体反应会维持多个月。发现针对SARS-CoV-2的抗体反应的稳健性,包括它的持久性和中和作用,对于让我们能够有效地监测社区的血清阳性率并确定保护我们免受再感染的抗体的持续时间和水平至关重要。这对有效的疫苗开发至关重要。”
2.Science:重磅!新研究重塑我们对肠道微生物组的理解
doi:10.1126/science.aay7367; doi:10.1126/science.abe7194
人类肠道是微生物的家园,它们的数量超过我们细胞数量的10倍。如今,在一项新的研究中,来自美国俄克拉荷马医学研究基金会等机构的研究人员获得的新发现重新定义了所谓的肠道微生物组是如何运作的,以及我们的身体如何与组成肠道微生物组的100万亿个细菌中的一些细菌共存。相关研究结果发表在2020年10月23日的Science期刊上,论文标题为“Proximal colon–derived O-glycosylated mucus encapsulates and modulates the microbiota”。
利用研究模型,俄克拉荷马医学研究基金会的Lijun Xia博士领导的一个研究团队发现肠道微生物组控制着一层特殊形式的富含糖分的粘液的产生,该粘液包裹粪便物质并随后者一起移动。他们发现粘液并不像以前认为的那样是静态的,而是作为粪便中的细菌和结肠中成千上万个免疫细胞之间的屏障发挥作用。若没有粘液,这整个系统就会失去平衡。
Xia说,“结肠不仅是一种消化器官,而且也是一种免疫器官。我们的肠道微生物组在出生的那一刻就开始产生,并在我们的一生中不断变化。它对我们体内获得性免疫系统的成长和成熟至关重要。当它没有得到很好的发展或护理时,它就不能发挥应有的作用,从而导致疾病的发生。”
3.Science:当感受到挤压时,细胞核会引导细胞逃离拥挤的空间
doi:10.1126/science.aba2644; doi:10.1126/science.abe3881
严重变形的威胁会引发一种快速的逃生反射,从而使得细胞从狭小的空间或拥挤的组织中移开并挤出。在一项新的研究中,来自巴塞罗那科技研究所、庞培法布拉大学和上奥地利应用科学大学的研究人员揭示了将细胞挤压到它的细胞核开始伸展的程度,会引发运动蛋白的激活,进而改变细胞的细胞骨架,使得它能够逃离拥挤的环境。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“The nucleus measures shape changes for cellular proprioception to control dynamic cell behavior”。
每个细胞都有一个细胞核,每个细胞核都有一层将染色体与细胞的其他部分分开的膜。在静止状态下,核膜是松弛的,就像一个松散的购物袋。如今,在这项新的研究中,这些研究人员发现,当核膜受到挤压时,它表面上的褶皱会自行熨平,这会引发一连串事件,改变细胞骨架,最终帮助细胞逃离拥挤的环境。
论文第一作者、巴塞罗那科技研究所的博士生Valeria Venturini说,“我们的研究代表了一种观念变革:细胞核本身并不只是一种静态的遗传物质容器,而是一种动态的传感器,可被细胞用来感知周围的环境。细胞核拉伸的强度可预测反应的强度,这就为这种单细胞水平上的'战斗或逃跑(fight or flight)'反射提供了新的启示。了解这种感知变形、测量这种变形并做出相应反应的能力,可能对理解癌症生长和稳态等过程具有重要意义。”
4.Science:细胞核就像一把尺子,可调整细胞对拥挤空间的反应
doi:10.1126/science.aba2894; doi:10.1126/science.abe3881
在一项新的研究中,为了测试细胞具有检测和应对环境引起的它们的形状发生变化的能力的假设,来自来自奥地利、英国、法国、瑞士、俄罗斯和美国的研究人员构建出人工微环境,用于模拟肿瘤细胞和免疫细胞在拥挤的组织中经历的情形。通过结合动态限制、力测量和活细胞成像,他们能够定量确定细胞在它们的形状受到精确控制的物理扰动时所作出的反应。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“The nucleus acts as a ruler tailoring cell responses to spatial constraints”。
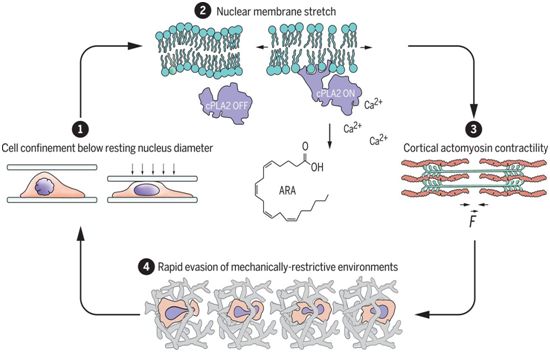
这些研究人员的研究结果显示,尽管细胞对压缩力具有惊人的抵抗能力,但是当它们在特定高度下变形时,它们会监测自身的形状,并产生积极的收缩反应。值得注意的是,他们发现,这是通过细胞监测它的最大内部区室---细胞核---的变形来实现的。他们确定细胞核为细胞提供了一个精确测量它的变形程度的方法。一旦细胞挤压超过了细胞核的尺寸,这就会引起边界核膜(bounding nuclear envelope)的展开和伸展。当核膜达到完全展开的状态时,收缩反应就开始了。核膜及其膜的机械状态的转变允许从内部膜储存中释放钙,并激活钙依赖性磷脂酶cPLA2。已知cPLA2作为核膜张力的分子传感器起作用,而且也是信号转导和代谢的关键调节因子。激活的cPLA2催化一种称为花生四烯酸(arachidonic acid)的Ω6脂肪酸的形成,而花生四烯酸除触发其他过程外,还能增强肌球蛋白II的三磷酸腺苷酶活性。这诱导肌球蛋白皮层(actomyosin cortex)的收缩性,产生推力来抵抗物理挤压,并在“逃避反射”机制中迅速将细胞挤出它所在的拥挤的微环境。
5.Science:颠覆常规!细胞利用脂滴抵御病毒和细菌感染机制
doi:10.1126/science.aay8085; doi:10.1126/science.abe7891
在一项新的研究中,来自西班牙多家研究机构的研究人员描述了一种新的免疫防御机制。这种机制是由能够吸引和清除入侵病原体的细胞器---脂滴(lipid droplet)---协调的。相关研究结果发表在2020年10月16日的Science期刊上 ,论文标题为“Mammalian lipid droplets are innate immune hubs integrating cell metabolism and host defense”。
脂滴是我们的细胞积累营养物的细胞器,这些营养物以脂肪的形式为细胞的功能发挥提供必要的能量。比如,脂滴为心脏的跳动、肝脏的代谢功能或肌肉的运动提供能量。论文共同通讯作者Albert Pol教授说,“脂滴就像我们细胞的储藏室,我们把以后要用的食物积累 在这里。这发生在所有真核细胞中,从酵母或昆虫到植物或哺乳动物。”
当病毒或细菌感染宿主细胞时,它们需要大量的营养物来增殖,并让它们达到脂滴。在这项新的研究中,这些研究人员发现,为了应对感染,脂滴将抗生素和抗病毒蛋白组装在一起而形成复合物,在这些复合物中,抗生素和抗病毒蛋白协同作用,对抗病原体并消灭它。 这是一种会在身体所有细胞中发挥作用的机制,而不仅仅是巨噬细胞等免疫系统细胞所特有的。在昆虫身上也观察到了这种防御策略,这说明了它在我们先天免疫进化过程中的重要性。
6.Science:新研究详细揭示人类正常心脏和衰竭心脏中的代谢组学特征
doi:10.1126/science.abc8861
在一项新的研究中,来自美国宾夕法尼亚大学、普林斯顿大学和费城儿童医院的研究人员提供了人类心脏使用燃料和营养物的详细情况。这项研究是同类研究中的第一次,它对数十名人类参与者的循环系统不同部位的血液进行同步采样,以记录流进和流出跳动的心脏的相关分子的水平。由此产生的数据揭示了正常心脏以及衰竭心脏中燃料使用的关键特征,从而为研究健康和患病的心脏建立了一个新的框架。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“Comprehensive quantification of fuel use by the failing and nonfailing human heart”。
论文通讯作者、宾夕法尼亚大学佩雷尔曼医学院心血管代谢项目主任Zoltan Arany博士说,“在这种细节水平上了解心脏如何处理燃料和营养物应当为未来开发治疗心力衰竭和相关疾病的方法提供信息。如今,我们清楚地了解了心脏如何为自己提供燃料,我们可以将目光放在设计改善心力衰竭患者的心脏代谢的方法上。”
7.Science:重大突破!蛋白Neuropilin-1促进新冠病毒进入和感染人体细胞
doi:10.1126/science.abd2985
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。众所周知,SARS-CoV-2是通过受体ACE2感染宿主细胞的。在一项新的研究中,来自德国神经退行性疾病研究中心、慕尼黑工业大学、哥廷根大学医学中心和芬兰赫尔辛基大学等研究机构的研究人员发现神经纤毛蛋白1(neuropilin-1, NRP1)是一种可以促进SARS-CoV-2进入细胞内部的因子。NRP1定位于呼吸道和嗅觉上皮,这可能是一个重要的战略定位,但却有助于SARS-CoV-2的感染和传播。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity”。论文通讯作者为慕尼黑工业大学的Mikael Simons和赫尔辛基大学的Giuseppe Balistreri。
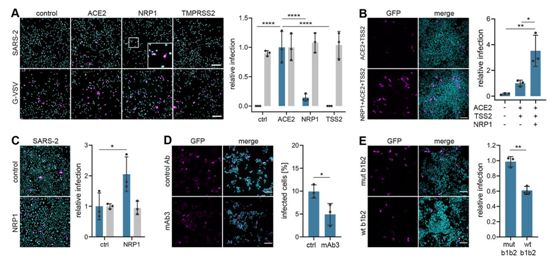
利用实验室培养的细胞、模拟SARS-CoV-2的人工病毒以及天然存在的病毒进行的实验表明,在ACE2存在的情况下,NRP1能够促进病毒感染。通过用抗体特异性阻断NRP1,这种病毒感染可被抑制。Simons解释说,“如果你把ACE2看作是进入细胞的一扇门,那么NRP1可能是引导这种病毒进入这扇门的一个因素。ACE2在大多数细胞中的表达水平很低。因此,这种病毒不容易找到进入细胞的门。诸如NRP1之类的其他因素可能是帮助这种病毒进入细胞的必要因素。”
8.Science:重大突破!蛋白Neuropilin-1是SARS-CoV-2感染的宿主因子
doi:10.1126/science.abd3072
在一项新的研究中,来自英国布里斯托大学和澳大利亚昆士兰大学等研究机构的研究人员取得一项重大突破:他们可能发现了SARS-CoV-2冠状病毒具有高度传染性并能在人体细胞中迅速传播的原因。这些发现描述了SARS-CoV-2感染人体细胞的能力是如何通过抑制剂阻断一种新发现的病毒与宿主相互作用来降低的,这有助人们开发出一种潜在的抗病毒治疗方法。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 is a host factor for SARS-CoV-2 infection”。与可引起普通感冒和轻度呼吸道症状的其他冠状病毒的不同的是,作为导致COVID-19疾病的病原体,SARS-CoV-2具有很强的传染性和传播性。在此之前,关于SARS-CoV-2为什么容易感染呼吸系统以外的大脑和心脏等器官的主要问题仍未得到解答。
在这项突破性的研究中,布里斯托大学生命科学学院的Peter Cullen教授、Yohei Yamauchi博士、Boris Simonetti博士和James Daly博士及其合作者们利用多种方法发现SARS-CoV-2能识别人体细胞表面上的一种名为神经纤毛蛋白1(neuropilin-1, NRP1)的蛋白,以促进病毒感染。
Yamauchi、Simonetti和Cullen解释道,“在研究SARS-CoV-2刺突蛋白的序列时,我们被一个小的氨基酸序列所震惊,这个序列似乎模仿了在人类蛋白中发现的与NRP1相互作用的蛋白序列。这使得使我们提出了一个简单的假设:SARS-CoV-2的刺突蛋白是否能与NRP1结合以帮助这种病毒感染人类细胞?令人兴奋的是,在应用一系列结构和生化方法时,我们能够确定SARS-CoV-2的刺突蛋白确实与NRP1结合。一旦我们确定这种刺突蛋白与NRP1结合,我们就能够证实这种相互作用可增强SARS-CoV-2对体外培养的人体细胞的入侵。重要的是,通过使用单克隆抗体(简称单抗)--实验室构建的类似于天然抗体的蛋白---或一种阻断这种相互作用的选择性药物,我们能够降低SARS-CoV-2感染人体细胞的能力。这凸显我们的发现在对抗COVID-19方面的潜在治疗价值。”
9.Science:重大进展!在体外重建HIV复制和整合过程,为开发靶向HIV衣壳的药物奠定基础
doi:10.1126/science.abc8420
在一项新的研究中,来自美国犹他大学医学院和弗吉尼亚大学的研究人员在试管中重现了导致获得性免疫缺陷综合征(AIDS,俗称艾滋病)的HIV(人类免疫缺陷病毒)感染的最初步骤,实现了几十年来的梦想。这样做使得人们能够近距离观察HIV,并能够确定这种病毒在人类宿主体内复制所需的基本成分。相关研究结果发表在2020年10月9日的Science期刊上,论文标题为“Reconstitution and visualization of HIV-1 capsid-dependent replication and integration in vitro”。
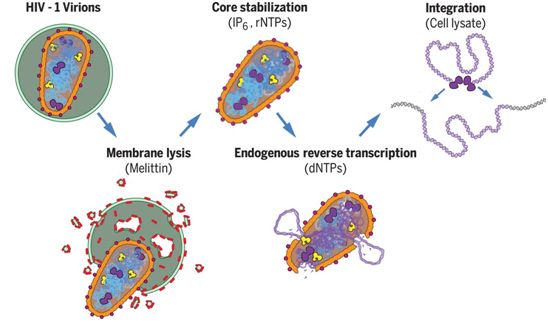
就HIV的所有危险性而言,这种病毒的外表却很简单。HIV类似于一个圆形的冰淇淋甜筒,它的外壳将它的遗传物质封装在里面。此前,人们一直认为,这个称为衣壳(capsid)的外壳的主要作用是保护它的珍贵货物(即前面提及的遗传物质)。但是,这项新的研究显示,HIV衣壳在感染过程中也发挥着积极作用。
在试管中进行感染的初始步骤,使得这些研究人员能够以以前不可能的方式精确地操纵HIV。他们发现,当他们使用遗传方法和生化方法破坏HIV衣壳的稳定性时,这种病毒无法有效复制它的遗传物质。这是首次直接证明HIV衣壳不仅仅是起着包装的作用,而且也是HIV感染过程本身的一个重要组成部分。
10.Science:重大突破!一类新型抑制剂可高效阻止神经变性,有望治疗一系列神经退行性疾病
doi:10.1126/science.aay3302; doi:10.1126/science.abe2791
在一项新的研究中,来自德国海德堡大学的研究人员发现了一种位于神经连接(即突触)处的通常会激活一种保护性遗传程序的特殊受体当位于突触外时如何导致神经细胞死亡。这种在神经退行性过程方面的重要发现使得他们对治疗药物产生了全新的认识。在对小鼠模型的实验中,他们发现了一类新的保护神经细胞的高效抑制剂。正如Hilmar Bading教授指出的那样,这类新型药物首次在对抗目前无法治疗的神经系统疾病方面开辟了前景。相关研究结果发表在2020年10月9日的Science期刊上,论文标题为“Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants”。
Bading教授和他的团队着重关注是这种称为N-甲基-D-天门冬氨酸(NMDA)受体的受体。这种受体是一种可被生化信使分子---神经递质谷氨酸---激活的离子通道蛋白。它允许钙流入细胞。钙信号在突触中启动可塑性过程,但也会传送到细胞核中,在那里激活一种保护性遗传程序。位于神经细胞连接处的可被谷氨酸激活的NMDA受体在大脑中具有关键功能,有助于学习和记忆过程以及神经保护。但是,这种受体也存在于突触外。这些位于突触外的NMDA受体构成了威胁,这是因为它们的激活会导致细胞死亡。然而,正常情况下,高效的细胞谷氨酸摄取系统可以确保这种受体不被激活,从而确保神经细胞不受损伤。
这种情况在疾病的存在下会发生巨大的变化。例如,如果在中风发作后,大脑的部分区域没有得到足够的氧气供应,循环中断就会使得这种谷氨酸摄取系统无效。突触外的谷氨酸水平增加,从而激活突触外的NMDA受体。其结果是神经细胞损伤和死亡,并伴随着脑功能受到限制。突触外谷氨酸水平增加不仅发生在大脑循环紊乱期间。Bading教授解释说,“有证据表明突触外NMDA受体的毒性特性在一些神经退行性疾病中起着核心作用。”根据这位科学家的说法,这尤其适用于阿尔茨海默病和肌萎缩侧索硬化症,其结果是肌肉无力、肌肉萎缩以及视网膜退化,甚至可能在病毒或寄生虫感染后出现大脑损伤。(生物谷 Bioon.com)
1.Science:大多数人对SARS-CoV-2产生强劲的抗体反应,而且这种抗体反应至少在5个月内保持相对稳定
doi:10.1126/science.abd7728
在一项新的研究中,来自美国西奈山伊坎医学院的研究人员发现绝大多数感染轻度到中度COVID-19的人都会产生强大的抗体反应,这种抗体反应至少在5个月内保持相对稳定。此外,他们还发现这种抗体反应与人体中和(或者说杀灭)SARS-CoV-2(导致COVID-19疾病的冠状病毒)的能力相关。相关研究结果于2020年10月28日在线发表在Science期刊上,论文标题为“Robust neutralizing antibodies to SARS-CoV-2 infection persist for months”。

血清样品中和活性与ELISA滴度有关。图片来自Science, 2020, doi:10.1126/science.abd7728。
2.Science:重磅!新研究重塑我们对肠道微生物组的理解
doi:10.1126/science.aay7367; doi:10.1126/science.abe7194
人类肠道是微生物的家园,它们的数量超过我们细胞数量的10倍。如今,在一项新的研究中,来自美国俄克拉荷马医学研究基金会等机构的研究人员获得的新发现重新定义了所谓的肠道微生物组是如何运作的,以及我们的身体如何与组成肠道微生物组的100万亿个细菌中的一些细菌共存。相关研究结果发表在2020年10月23日的Science期刊上,论文标题为“Proximal colon–derived O-glycosylated mucus encapsulates and modulates the microbiota”。
利用研究模型,俄克拉荷马医学研究基金会的Lijun Xia博士领导的一个研究团队发现肠道微生物组控制着一层特殊形式的富含糖分的粘液的产生,该粘液包裹粪便物质并随后者一起移动。他们发现粘液并不像以前认为的那样是静态的,而是作为粪便中的细菌和结肠中成千上万个免疫细胞之间的屏障发挥作用。若没有粘液,这整个系统就会失去平衡。
Xia说,“结肠不仅是一种消化器官,而且也是一种免疫器官。我们的肠道微生物组在出生的那一刻就开始产生,并在我们的一生中不断变化。它对我们体内获得性免疫系统的成长和成熟至关重要。当它没有得到很好的发展或护理时,它就不能发挥应有的作用,从而导致疾病的发生。”
3.Science:当感受到挤压时,细胞核会引导细胞逃离拥挤的空间
doi:10.1126/science.aba2644; doi:10.1126/science.abe3881
严重变形的威胁会引发一种快速的逃生反射,从而使得细胞从狭小的空间或拥挤的组织中移开并挤出。在一项新的研究中,来自巴塞罗那科技研究所、庞培法布拉大学和上奥地利应用科学大学的研究人员揭示了将细胞挤压到它的细胞核开始伸展的程度,会引发运动蛋白的激活,进而改变细胞的细胞骨架,使得它能够逃离拥挤的环境。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“The nucleus measures shape changes for cellular proprioception to control dynamic cell behavior”。
每个细胞都有一个细胞核,每个细胞核都有一层将染色体与细胞的其他部分分开的膜。在静止状态下,核膜是松弛的,就像一个松散的购物袋。如今,在这项新的研究中,这些研究人员发现,当核膜受到挤压时,它表面上的褶皱会自行熨平,这会引发一连串事件,改变细胞骨架,最终帮助细胞逃离拥挤的环境。
论文第一作者、巴塞罗那科技研究所的博士生Valeria Venturini说,“我们的研究代表了一种观念变革:细胞核本身并不只是一种静态的遗传物质容器,而是一种动态的传感器,可被细胞用来感知周围的环境。细胞核拉伸的强度可预测反应的强度,这就为这种单细胞水平上的'战斗或逃跑(fight or flight)'反射提供了新的启示。了解这种感知变形、测量这种变形并做出相应反应的能力,可能对理解癌症生长和稳态等过程具有重要意义。”
4.Science:细胞核就像一把尺子,可调整细胞对拥挤空间的反应
doi:10.1126/science.aba2894; doi:10.1126/science.abe3881
在一项新的研究中,为了测试细胞具有检测和应对环境引起的它们的形状发生变化的能力的假设,来自来自奥地利、英国、法国、瑞士、俄罗斯和美国的研究人员构建出人工微环境,用于模拟肿瘤细胞和免疫细胞在拥挤的组织中经历的情形。通过结合动态限制、力测量和活细胞成像,他们能够定量确定细胞在它们的形状受到精确控制的物理扰动时所作出的反应。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“The nucleus acts as a ruler tailoring cell responses to spatial constraints”。

图片来自Science, 2020, doi:10.1126/science.aba2894。
这些研究人员的研究结果显示,尽管细胞对压缩力具有惊人的抵抗能力,但是当它们在特定高度下变形时,它们会监测自身的形状,并产生积极的收缩反应。值得注意的是,他们发现,这是通过细胞监测它的最大内部区室---细胞核---的变形来实现的。他们确定细胞核为细胞提供了一个精确测量它的变形程度的方法。一旦细胞挤压超过了细胞核的尺寸,这就会引起边界核膜(bounding nuclear envelope)的展开和伸展。当核膜达到完全展开的状态时,收缩反应就开始了。核膜及其膜的机械状态的转变允许从内部膜储存中释放钙,并激活钙依赖性磷脂酶cPLA2。已知cPLA2作为核膜张力的分子传感器起作用,而且也是信号转导和代谢的关键调节因子。激活的cPLA2催化一种称为花生四烯酸(arachidonic acid)的Ω6脂肪酸的形成,而花生四烯酸除触发其他过程外,还能增强肌球蛋白II的三磷酸腺苷酶活性。这诱导肌球蛋白皮层(actomyosin cortex)的收缩性,产生推力来抵抗物理挤压,并在“逃避反射”机制中迅速将细胞挤出它所在的拥挤的微环境。
5.Science:颠覆常规!细胞利用脂滴抵御病毒和细菌感染机制
doi:10.1126/science.aay8085; doi:10.1126/science.abe7891
在一项新的研究中,来自西班牙多家研究机构的研究人员描述了一种新的免疫防御机制。这种机制是由能够吸引和清除入侵病原体的细胞器---脂滴(lipid droplet)---协调的。相关研究结果发表在2020年10月16日的Science期刊上 ,论文标题为“Mammalian lipid droplets are innate immune hubs integrating cell metabolism and host defense”。
脂滴是我们的细胞积累营养物的细胞器,这些营养物以脂肪的形式为细胞的功能发挥提供必要的能量。比如,脂滴为心脏的跳动、肝脏的代谢功能或肌肉的运动提供能量。论文共同通讯作者Albert Pol教授说,“脂滴就像我们细胞的储藏室,我们把以后要用的食物积累 在这里。这发生在所有真核细胞中,从酵母或昆虫到植物或哺乳动物。”
当病毒或细菌感染宿主细胞时,它们需要大量的营养物来增殖,并让它们达到脂滴。在这项新的研究中,这些研究人员发现,为了应对感染,脂滴将抗生素和抗病毒蛋白组装在一起而形成复合物,在这些复合物中,抗生素和抗病毒蛋白协同作用,对抗病原体并消灭它。 这是一种会在身体所有细胞中发挥作用的机制,而不仅仅是巨噬细胞等免疫系统细胞所特有的。在昆虫身上也观察到了这种防御策略,这说明了它在我们先天免疫进化过程中的重要性。
6.Science:新研究详细揭示人类正常心脏和衰竭心脏中的代谢组学特征
doi:10.1126/science.abc8861
在一项新的研究中,来自美国宾夕法尼亚大学、普林斯顿大学和费城儿童医院的研究人员提供了人类心脏使用燃料和营养物的详细情况。这项研究是同类研究中的第一次,它对数十名人类参与者的循环系统不同部位的血液进行同步采样,以记录流进和流出跳动的心脏的相关分子的水平。由此产生的数据揭示了正常心脏以及衰竭心脏中燃料使用的关键特征,从而为研究健康和患病的心脏建立了一个新的框架。相关研究结果发表在2020年10月16日的Science期刊上,论文标题为“Comprehensive quantification of fuel use by the failing and nonfailing human heart”。
论文通讯作者、宾夕法尼亚大学佩雷尔曼医学院心血管代谢项目主任Zoltan Arany博士说,“在这种细节水平上了解心脏如何处理燃料和营养物应当为未来开发治疗心力衰竭和相关疾病的方法提供信息。如今,我们清楚地了解了心脏如何为自己提供燃料,我们可以将目光放在设计改善心力衰竭患者的心脏代谢的方法上。”
7.Science:重大突破!蛋白Neuropilin-1促进新冠病毒进入和感染人体细胞
doi:10.1126/science.abd2985
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。众所周知,SARS-CoV-2是通过受体ACE2感染宿主细胞的。在一项新的研究中,来自德国神经退行性疾病研究中心、慕尼黑工业大学、哥廷根大学医学中心和芬兰赫尔辛基大学等研究机构的研究人员发现神经纤毛蛋白1(neuropilin-1, NRP1)是一种可以促进SARS-CoV-2进入细胞内部的因子。NRP1定位于呼吸道和嗅觉上皮,这可能是一个重要的战略定位,但却有助于SARS-CoV-2的感染和传播。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity”。论文通讯作者为慕尼黑工业大学的Mikael Simons和赫尔辛基大学的Giuseppe Balistreri。

NRP1促进SARS-CoV-2病毒假颗粒进入细胞。图片来自Science, 2020, doi:10.1126/science.abd2985。
利用实验室培养的细胞、模拟SARS-CoV-2的人工病毒以及天然存在的病毒进行的实验表明,在ACE2存在的情况下,NRP1能够促进病毒感染。通过用抗体特异性阻断NRP1,这种病毒感染可被抑制。Simons解释说,“如果你把ACE2看作是进入细胞的一扇门,那么NRP1可能是引导这种病毒进入这扇门的一个因素。ACE2在大多数细胞中的表达水平很低。因此,这种病毒不容易找到进入细胞的门。诸如NRP1之类的其他因素可能是帮助这种病毒进入细胞的必要因素。”
8.Science:重大突破!蛋白Neuropilin-1是SARS-CoV-2感染的宿主因子
doi:10.1126/science.abd3072
在一项新的研究中,来自英国布里斯托大学和澳大利亚昆士兰大学等研究机构的研究人员取得一项重大突破:他们可能发现了SARS-CoV-2冠状病毒具有高度传染性并能在人体细胞中迅速传播的原因。这些发现描述了SARS-CoV-2感染人体细胞的能力是如何通过抑制剂阻断一种新发现的病毒与宿主相互作用来降低的,这有助人们开发出一种潜在的抗病毒治疗方法。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 is a host factor for SARS-CoV-2 infection”。与可引起普通感冒和轻度呼吸道症状的其他冠状病毒的不同的是,作为导致COVID-19疾病的病原体,SARS-CoV-2具有很强的传染性和传播性。在此之前,关于SARS-CoV-2为什么容易感染呼吸系统以外的大脑和心脏等器官的主要问题仍未得到解答。
在这项突破性的研究中,布里斯托大学生命科学学院的Peter Cullen教授、Yohei Yamauchi博士、Boris Simonetti博士和James Daly博士及其合作者们利用多种方法发现SARS-CoV-2能识别人体细胞表面上的一种名为神经纤毛蛋白1(neuropilin-1, NRP1)的蛋白,以促进病毒感染。
Yamauchi、Simonetti和Cullen解释道,“在研究SARS-CoV-2刺突蛋白的序列时,我们被一个小的氨基酸序列所震惊,这个序列似乎模仿了在人类蛋白中发现的与NRP1相互作用的蛋白序列。这使得使我们提出了一个简单的假设:SARS-CoV-2的刺突蛋白是否能与NRP1结合以帮助这种病毒感染人类细胞?令人兴奋的是,在应用一系列结构和生化方法时,我们能够确定SARS-CoV-2的刺突蛋白确实与NRP1结合。一旦我们确定这种刺突蛋白与NRP1结合,我们就能够证实这种相互作用可增强SARS-CoV-2对体外培养的人体细胞的入侵。重要的是,通过使用单克隆抗体(简称单抗)--实验室构建的类似于天然抗体的蛋白---或一种阻断这种相互作用的选择性药物,我们能够降低SARS-CoV-2感染人体细胞的能力。这凸显我们的发现在对抗COVID-19方面的潜在治疗价值。”
9.Science:重大进展!在体外重建HIV复制和整合过程,为开发靶向HIV衣壳的药物奠定基础
doi:10.1126/science.abc8420
在一项新的研究中,来自美国犹他大学医学院和弗吉尼亚大学的研究人员在试管中重现了导致获得性免疫缺陷综合征(AIDS,俗称艾滋病)的HIV(人类免疫缺陷病毒)感染的最初步骤,实现了几十年来的梦想。这样做使得人们能够近距离观察HIV,并能够确定这种病毒在人类宿主体内复制所需的基本成分。相关研究结果发表在2020年10月9日的Science期刊上,论文标题为“Reconstitution and visualization of HIV-1 capsid-dependent replication and integration in vitro”。

在体外重建和可视化观察HIV-1衣壳依赖性的复制和整合。图片来自Science, 2020, doi:10.1126/science.abc8420。
就HIV的所有危险性而言,这种病毒的外表却很简单。HIV类似于一个圆形的冰淇淋甜筒,它的外壳将它的遗传物质封装在里面。此前,人们一直认为,这个称为衣壳(capsid)的外壳的主要作用是保护它的珍贵货物(即前面提及的遗传物质)。但是,这项新的研究显示,HIV衣壳在感染过程中也发挥着积极作用。
在试管中进行感染的初始步骤,使得这些研究人员能够以以前不可能的方式精确地操纵HIV。他们发现,当他们使用遗传方法和生化方法破坏HIV衣壳的稳定性时,这种病毒无法有效复制它的遗传物质。这是首次直接证明HIV衣壳不仅仅是起着包装的作用,而且也是HIV感染过程本身的一个重要组成部分。
10.Science:重大突破!一类新型抑制剂可高效阻止神经变性,有望治疗一系列神经退行性疾病
doi:10.1126/science.aay3302; doi:10.1126/science.abe2791
在一项新的研究中,来自德国海德堡大学的研究人员发现了一种位于神经连接(即突触)处的通常会激活一种保护性遗传程序的特殊受体当位于突触外时如何导致神经细胞死亡。这种在神经退行性过程方面的重要发现使得他们对治疗药物产生了全新的认识。在对小鼠模型的实验中,他们发现了一类新的保护神经细胞的高效抑制剂。正如Hilmar Bading教授指出的那样,这类新型药物首次在对抗目前无法治疗的神经系统疾病方面开辟了前景。相关研究结果发表在2020年10月9日的Science期刊上,论文标题为“Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants”。
Bading教授和他的团队着重关注是这种称为N-甲基-D-天门冬氨酸(NMDA)受体的受体。这种受体是一种可被生化信使分子---神经递质谷氨酸---激活的离子通道蛋白。它允许钙流入细胞。钙信号在突触中启动可塑性过程,但也会传送到细胞核中,在那里激活一种保护性遗传程序。位于神经细胞连接处的可被谷氨酸激活的NMDA受体在大脑中具有关键功能,有助于学习和记忆过程以及神经保护。但是,这种受体也存在于突触外。这些位于突触外的NMDA受体构成了威胁,这是因为它们的激活会导致细胞死亡。然而,正常情况下,高效的细胞谷氨酸摄取系统可以确保这种受体不被激活,从而确保神经细胞不受损伤。
这种情况在疾病的存在下会发生巨大的变化。例如,如果在中风发作后,大脑的部分区域没有得到足够的氧气供应,循环中断就会使得这种谷氨酸摄取系统无效。突触外的谷氨酸水平增加,从而激活突触外的NMDA受体。其结果是神经细胞损伤和死亡,并伴随着脑功能受到限制。突触外谷氨酸水平增加不仅发生在大脑循环紊乱期间。Bading教授解释说,“有证据表明突触外NMDA受体的毒性特性在一些神经退行性疾病中起着核心作用。”根据这位科学家的说法,这尤其适用于阿尔茨海默病和肌萎缩侧索硬化症,其结果是肌肉无力、肌肉萎缩以及视网膜退化,甚至可能在病毒或寄生虫感染后出现大脑损伤。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


