2019年11月HIV研究亮点进展
来源:本站原创 2019-11-27 23:59
2019年11月27日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,
2019年11月27日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,导致免疫系统瘫痪,从而致使各种疾病在人体内蔓延,最终导致艾滋病。由于HIV的变异极其迅速,难以生产特异性疫苗,至今无有效治疗方法,对人类健康造成极大威胁。
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的11月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Science子刊:诱导太多Th1细胞产生会破坏HIV疫苗的效力
doi:10.1126/scitranslmed.aav1800
如果HIV疫苗引起错误的免疫反应,则这种疫苗接种可能适得其反。如今,在一项新的研究中,来自美国埃默里大学等研究机构的研究人员从利用与HIV病毒存在紧密亲缘关系的SIV病毒开展的几项非人灵长类动物研究中收集到证据表明构建太多的软靶标(soft target)会削弱旨在提供预防病毒感染的疫苗接种。HIV靶向协助身体产生抗病毒免疫反应的辅助性T细胞(Th细胞)并在它们当中复制。他们发现至关重要的是,针对HIV的疫苗不能为这种病毒建立更多的安全避风港。相关研究结果发表在2019年11月20日的Science Translational Medicine期刊上,论文标题为“Strong TH1-biased CD4 T cell responses are associated with diminished SIV vaccine efficacy”。
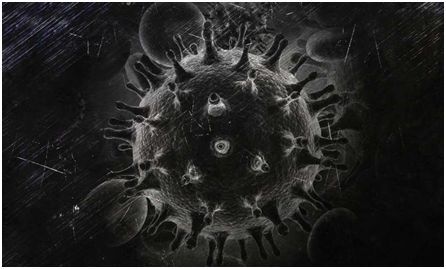
当疫苗接种产生太多特定类型的I型辅助性T细胞(Th1细胞)时,就会出现问题。这些细胞迁移到粘膜组织,比如直肠、子宫颈和阴道,在大多数感染中,HIV/SIV首先就从粘膜组织进入人体。
这些Th1细胞好比是应对僵尸攻击的第一批反应者。它们最初对抗HIV病毒,但随后被这种病毒接管。论文通讯作者、埃默里大学耶克斯国家灵长类动物研究中心研究员Rama Rao Amara博士说,人们需要的是Tfh细胞,它们停留在淋巴结中,并协助免疫系统产生针对这种病毒的抗体。他说,“我们并不是说Th1细胞是坏的。但是,如果你有太多的Th1细胞,它们会使得疫苗无法产生有效的保护。”
2.Science子刊:临床试验表明抗原竞争会破坏HIV疫苗的效力
doi:10.1126/scitranslmed.aaw1673
许多HIV疫苗旨在产生强大的T细胞反应。T细胞反应与未感染者感染HIV的风险下降和HIV感染者控制病毒复制有关。HIV抗原Gag特异性T细胞主要与感染后控制相关,而HIV抗原Env抗原是保护性抗体的作用靶标。 因此,HIV疫苗设计中通常包含这两种抗原。但是,包含多种抗原可能会引起抗原竞争,从而降低疫苗的潜在效力。
在一项新的临床研究中,来自美国、巴西、秘鲁和瑞士的研究人员给研究参与者仅接种HIV 抗原Gag/Pol,或者同时接种HIV 抗原Gag/Pol和Env,以便观察抗原竞争是否会干扰CD4 T细胞反应。他们发现当同时接种Gag/Pol和Env时,检测到的针对Gag/Pol的CD4 T细胞反应较低,这表明在疫苗中包含多种抗原可能会阻止最大的T细胞反应。相关研究结果发表在2019年11月20日的Science Translational Medicine期刊上,论文标题为“Antigenic competition in CD4+ T cell responses in a randomized, multicenter, double-blind clinical HIV vaccine trial”。
具体而言,这项称为HVTN 084的临床研究,是一项随机、多中心、双盲1期临床试验,旨在研究Gag/Pol疫苗中添加Env是否会降低Gag/Pol特异性T细胞反应的幅度或广度。五十名志愿者每人肌肉内注射一次1×1010颗粒单位(PU)的rAd5 Gag/Pol和EnvA/B/C(按照3:1:1:1比例混合在一起)或5×109颗粒单位的rAd5 Gag/Pol。在未接种Env的疫苗接种组中,疫苗接种后4周通过细胞因子表达衡量的CD4+ T细胞反应显著高于接种Env的疫苗接种组,不过这两个疫苗接种组之间的CD8+ T细胞反应没有显著差异。他们进一步揭示与Gag/Pol和Env共免疫接种相比,在不存在Env的情况下,Gag/Pol特异性T细胞反应的广度更大。向Gag/Pol疫苗中添加Env抗原导致针对Gag/Pol的CD4+ T细胞反应率和幅度降低,以及抗原表位的宽度也下降了,这就证实了抗原竞争的存在。
3.Science:重磅!突破性的HIV疫苗设计策略崭露头角
doi:10.1126/science.aax4380
在一项新的研究中,来自美国斯克里普斯研究所等研究机构的研究人员成功地对一种先进的HIV疫苗策略进行了原理验证,这种方法也可能有效地保护人们免受其他致命性传染病的侵害。相关研究结果近期发表在Science期刊上,论文标题为“A generalized HIV vaccine design strategy for priming of broadly neutralizing antibody responses”。
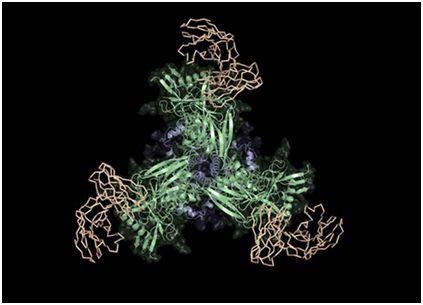
这种新的疫苗策略集中在刺激免疫系统以产生针对HIV的广泛中和抗体(bnAb)。这些特殊的抗体能够结合到HIV病毒表面上重要的但难以接近的区域,而且这些区域在不同HIV毒株之间的差异并不大,因此它们可以中和许多不同的快速突变的HIV毒株。产生此类抗体的疫苗可以挽救数百万人的生命和节省数十亿美元,并最终可能有助于消除艾滋病这一重大的公共卫生问题。基于一种称为“生殖系靶向(germline targeting)”的概念,这种新的策略可能阻止在全球传播的数百万种不同的病毒毒株。迄今为止,实现这一目标还很困难。从未发现有任何候选HIV疫苗能在人体内诱导保护性的bnAb反应。
Schief及其同事们先前在一种特殊情况下展示了一种生殖系靶向策略:bnAb以一种不寻常的方式捕获HIV。这种新方法功能更强大,这是因为它适用于通过一种更为常见的机制捕获靶标的抗体。此外,这项研究中进行的分析表明这种方法也可能适用于制备针对许多其他难治病原体的疫苗,比如流感病毒、登革热病毒、寨卡病毒、丙型肝炎病毒和疟原虫。为了证实这种策略的可行性,Schief和论文共同第一作者、Schief实验室高级科学家Jon Steichen博士首先选择了一种已知的称为BG18的HIV bnAb作为测试案例。通过对BG18与HIV病毒上的靶标结合在一起时的结构研究,这些研究人员鉴定出这种抗体的HIV捕获能力的关键特征。接下来,他们搜索了一个庞大的人类抗体基因数据库,以便寻找产生的抗体与BG18的关键特征天然相同的B细胞。他们随后使用一种复杂的策略来选择和进化一组可能潜在地激活多种BG18样B细胞(BG18-like B cell)的病毒模拟蛋白。这些蛋白最终将作为“免疫原”刺激接受疫苗接种的人体中的BG18样B细胞。对来自HIV阴性人类捐赠者的血液样本进行的测试证实这些研究人员设计出的免疫原与正常循环的具有所需的BG18样特征的B细胞良好地结合。
4.Cell Rep:疟疾领域新发现有助于HIV的治疗
doi:10.1016/j.celrep.2019.10.087
根据最近一项研究,来自澳大利亚研究人员发现免疫系统对疟疾感染作出的反应可能有助于开发针对丙型肝炎,艾滋病毒和狼疮的新型治疗方法。研究者们通过实验室模型发现,由疟疾感染引起的强烈炎症信号激活了特定分子,这些分子触发了抵抗疾病的高效抗体的产生。相关结果发表在《Cell Reports》杂志上。
Hansen博士和她的团队在过去的十年中一直在探索宿主免疫系统如何应对疟疾感染。“在我们以前的论文中,我们证明了炎症信号激活了阻止辅助性T细胞发育的分子,这意味着B细胞没有获得制造抗体的必要指令。当我们开始这项研究时,我们期望看到炎症也对B细胞产生了负面影响。事实上,我们发现情况恰恰相反。炎症信号传给B细胞进而提高了抗体的质量。”
Hansen博士说,她希望这一发现将在疟疾之外发挥作用。她说:“我认为这项发现提供了治疗慢性病毒感染和自身免疫性疾病的机会。我们已经确定了驱动免疫系统产生强效抗体的分子'开关',以及影响其功能的炎症信号。针对该分子或同一途径中的其他分子,可以提供治疗这些疾病的精密手段”。
在包括疟疾和病毒感染(如HIV和慢性丙型肝炎)在内的慢性感染中,产生非常高质量的有效抗体对于清除感染至关重要。另一方面,能够产生针对自身抗原(人体自身的蛋白质和组织)的抗体的B细胞则是导致自身免疫性疾病,例如狼疮的根本原因。
5.Menopause:女性HIV感染者具有增加的过早绝经风险
doi:10.1097/GME.0000000000001423
由于医学的进步,HIV阳性的女性如今具有更长的预期寿命,但这让她们面临许多中年健康问题,比如绝经(menopause, 也译作更年期)。一项新研究表明,感染HIV的女性更可能在平均48岁时进入绝经,比一般人群年轻3岁。相关研究结果近期发表在Menopause期刊上,论文标题为“Prevalence and correlates of early-onset menopause among women living with HIV in Canada”。
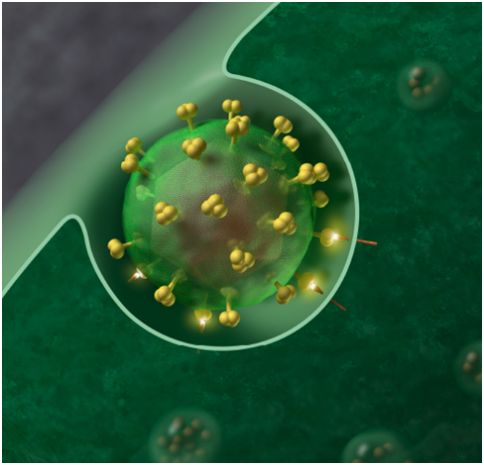
加拿大和美国女性的绝经平均年龄在50至52岁之间。先前的研究已表明感染HIV的女性出现绝经提前(early menopause, 年龄在40岁和45岁之间)和早绝经(premature menopause, 也称为原发性卵巢功能不足,年龄在小于40岁)的风险增加。但是,来自加拿大的这项研究是已知的第一项确定HIV患者平均绝经年龄、绝经提前(40岁和45岁之间)发生率、早绝经(小于40岁)发生率以及其他影响绝经年龄的相关因素的研究。
这些研究人员证实感染HIV的女性绝经年龄更小,更具体地说48岁,比未感染的女性早3年。这个感染HIV的女性群体还具有更高的绝经提前发生率和早绝经发生率。此外,较低的教育水平和丙型肝炎病毒合并感染也会影响绝经提前风险,其他可能的修正因素包括婚姻状况和出生地区。
6.J Virol:病毒特性或能预测HIV抗体疗法的疗效
doi:10.1128/JVI.01604-19
当前的HIV疗法能够高效减缓患者体内病毒的进展且副作用较小,日常的抗逆转录病毒疗法(ART)使用了HIV药物的组合来对患者进行治疗,然而由于很多原因,一部分HIV-1患者并不能接受ART来进行治疗;即便目前研究人员正在开发一种包括基于抗体疗法在内可选择的治疗手段,但其仍然很难预测哪些患者适合这些昂贵疗法的治疗。
近日,一项刊登在国际杂志Journal of Virology上的研究报告中,来自波士顿医学中心的科学家们通过研究发现,利用特殊病毒的特性或能帮助预测基于抗体的HIV-1疗法的治疗效力。医学博士Manish Sagar表示,利用测序的方法对HIV-1病毒特性进行分析,或能预测特殊抗体疗法的治疗效果,已经鉴定出的病毒特性或许也能用来确定患者未来是否能因特殊抗体疗法而获益,这就能够有效减少患者治疗的时间和成本。
抗体疗法能够结合保护HIV-1免于宿主免疫系统反应的包膜蛋白,这些包膜蛋白拥有广泛的DNA序列变异,其能提供病毒的信息以及疗法是否能有效给患者带来帮助,但研究者很难仅通过了解包膜的序列来预测基于抗体的疗法是否有效,因此通过在患者开始接受HIV-1治疗之前就能获得序列信息,从而确定其体内的病毒是否对疗法敏感。这项研究中,研究人员鉴别出了HIV-1包膜序列的基序特性并能预测特殊抗体疗法给患者带来的治疗潜力。
7.JCI:新型DNA技术用于靶向输送抗HIV药物
doi:10.1172/JCI132779
近日,Wistar研究所的科学家利用基于合成DNA的技术来促进小动物和大动物模型中产生HIV广谱性中和抗体,为简单有效的下一代HIV预防和治疗方法提供了概念验证。这些结果在线发表在《Journal of Clinical Investigation》杂志上。
尽管抗逆转录病毒疗法在治疗HIV感染方面取得了非凡的进步,但仍需要新的预防和治疗方法以根除HIV感染。研究人员从受感染的个体中分离出许多非常有效的单克隆抗体,这些抗体可以中和各种各样的HIV毒株。这样的单克隆抗体可以作为被动免疫疗法生产和施用,并且代表了目前在早期临床研究中有希望的方法。
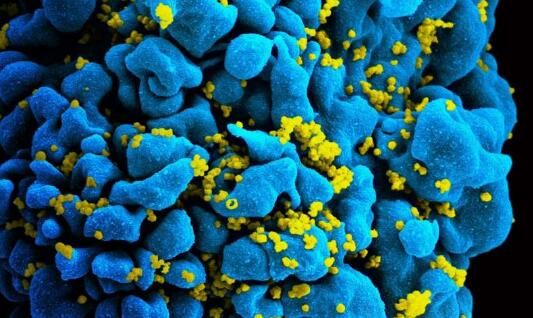
首席研究员,执行副总裁兼董事David B. Weiner博士说:“我们开发了DMAb平台,以允许通过合成DNA直接体内产生抗体,而合成DNA的目的是向人体提供制造所需抗体的指导。根据我们的早期数据,我们认为该平台作为HIV抗体递送的新策略值得进一步研究。”
Weiner和合作者设计了一个由16个DMAb组成的小组,将先前表征的广泛中和抗体重新合成为DMAb。使用Cellectra自适应电穿孔法通过注射导入小鼠体内并进行了研究。研究人员观察到快速DMAb表达和血液中长达数月的稳定水平。此外,与相应的重组抗体相比,体内产生的DMAbs具有很强的中和能力。由于HIV病毒能够突变以逃避单一抗体的免疫力,因此测试了多达四个不同DMAb的组合作为克服耐药性的策略。组合产生的抗体的体内总水平与单独给药的相同抗体的水平之和相当,表明该方法具有灵活性,适用于多种抗体的联合治疗。重要的是,数据支持这种组合比单一抗体可以阻止更多的HIV病毒。
接下来,研究人员在一项非人类灵长类动物试验性研究中探索了HIV-1 DMAb的递送,该研究与向临床转化更为相关。研究结果表明,注入一或两种组合的DMAb后,三天就可以在体内检测到表达,到14天时显示出峰值活性。重要的是,来自上述动物的血清具有很高的抗病毒活性。
8.JAIDS:重磅!自2000年以来科学家们首次发现新型HIV毒株
doi:10.1097/QAI.0000000000002246
近日,一项刊登在国际杂志Journal of Acquired Immune Deficiency Syndromes上的研究报告中,来自雅培公司等机构的科学家们通过研究宣布,自2000年以来他们发现了全球首个HIV病毒新亚型。研究者Rodgers表示,我们一直在寻找病毒,很多人可能并没有意识到HIV有不止一种毒株,如今研究者正在对鉴别出的所有HIV毒株进行测试来了解其不同的毒株类型。
这种新发现的HIV毒株为HIV-1 M群、L亚型,于20世纪80年代首次收集自刚果民主共和国,但仅有两份样本能通过基因测序来进行检测,研究者需要第三个样本才能够确定病毒的形式,2001年,他们收集了一份非常相似的样本,但该样本并不能进行完全测序,当然了,研究者也无法合成病毒,而样本数量也太少了。
如今,在测序技术的帮助下,研究者证实,L亚型毒株属于HIV病毒M群的突变体,而M群病毒是AIDS流行的罪魁祸首;尽管研究人员并不清楚这种新型亚型毒株如何影响机体,但他们推测,这种病毒与其它M群毒株的行为方式大致相同。这项研究非常重要,其对于开发新型HIV疗法具有重要意义。
9.JCI:三种抗体介导的免疫反应增加与HIV传播风险下降有关
doi:10.1172/JCI126391
与感染风险下降相关的免疫反应称为保护相关因素(correlates of protection, CoP)。测量疫苗诱导的抗体和细胞介导的免疫反应的临床试验有助于确定针对HIV的保护相关因素,这对于评估一种有前景的HIV候选疫苗的疗效是必要的。
在来自受到美国国家过敏与传染病研究所(NIAID)资助的HIV疫苗试验网络(HIV Vaccine Trials Network, HVTN)的资深作者Georgia Tomaras、Peter Gilbert和论文第一作者Scott Neidich、Youyi Fong和Shuying Li的领导下,一项新的初步临床研究证实三种抗体介导的免疫反应---抗体介导的Fcγ受体(FcγR)招募、抗体依赖的细胞吞噬作用(ADCP)和抗Env IgG3--的增加与HIV传播减少有关。相关研究结果近期发表在Journal of Clinical Investigation期刊上,论文标题为“Antibody Fc effector functions and IgG3 associate with decreased HIV-1 risk”。
值得注意的是,针对这些抗体反应而言,ADCP和IgG3是与HIV传播减少相关的最强相关因素。然而,FcγRIIa参与是受到HIV感染的疫苗接种者中病毒载量下降的唯一相关因素。ADCP、IgG3和FcR参与是新提出的保护相关因素,可在全球正在进行的HVTN 702、HVTN 705和HVTN 706大规模HIV疫苗功效临床试验完成后加以验证。
10.Mol Ther:相似机制!HIV药物能够有效治疗寨卡病毒感染
doi:10.1016/j.ymthe.2019.10.006
众所周知,开发能够适应不同病毒复制机制的药物将极大地提高不同类型传染病的治疗手段。在一项新的工作中,坦普尔大学医学院的研究人员表明,利用现有药物来治疗其它类型病毒性疾病实际上是可能的。
坦普尔的研究人员在《Molecular Therapy》杂志上发表的一项新研究发现,用于治疗HIV的药物同时也可以抑制Zika病毒感染。在细胞和动物模型中,他们表明这种名为rilpivirine的药物通过靶向HIV和Zika病毒复制所依赖的酶来抑制Zika病毒感染。实际上,这些酶存在于Zika病毒以及其它密切相关的病毒中,包括登革热,黄热,西尼罗河热和丙型肝炎等等。
“ HIV和Zika病毒是不同类型的RNA病毒,”文章作者,神经病毒学中心主任以及LKSOM综合神经艾滋病中心主任博士Kamel Khalili博士解释道:“我们发现rilpivirine通过结合RNA病毒家族共有的RNA聚合酶来阻断Zika病毒复制,因此,我们开辟了使用相同策略潜在地治疗多种RNA病毒感染的途径。”
11.Gut:HIV药物利匹韦林或能有效改善机体肝纤维化症状
doi:10.1136/gutjnl-2019-318372
近日,一项刊登在国际杂志Gut上题为“Rilpivirine attenuates liver fibrosis through selective STAT1-mediated apoptosis in hepatic stellate cells”的研究报告中,来自西班牙瓦伦西亚大学等机构的科学家们通过研究发现,一种用于治疗HIV的抗逆转录病毒药物—利匹韦林(Rilpivirine)或对慢性肝脏疾病具有有益效应,相关研究结果或有望帮助开发治疗肝脏疾病的新型疗法。
文章中,研究者表示,当对不同的肝脏损伤临床前模型进行研究后他们发现,用于治疗HIV感染的药物利匹韦林或能有效降低模型机体中的肝脏纤维化程度。目前研究人员需要寻找能够有效治疗肝纤维化患者的选择性疗法,这些疗法能作用于星状细胞的失活并促进肝脏组织再生。(生物谷 Bioon.com)
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的11月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Science子刊:诱导太多Th1细胞产生会破坏HIV疫苗的效力
doi:10.1126/scitranslmed.aav1800
如果HIV疫苗引起错误的免疫反应,则这种疫苗接种可能适得其反。如今,在一项新的研究中,来自美国埃默里大学等研究机构的研究人员从利用与HIV病毒存在紧密亲缘关系的SIV病毒开展的几项非人灵长类动物研究中收集到证据表明构建太多的软靶标(soft target)会削弱旨在提供预防病毒感染的疫苗接种。HIV靶向协助身体产生抗病毒免疫反应的辅助性T细胞(Th细胞)并在它们当中复制。他们发现至关重要的是,针对HIV的疫苗不能为这种病毒建立更多的安全避风港。相关研究结果发表在2019年11月20日的Science Translational Medicine期刊上,论文标题为“Strong TH1-biased CD4 T cell responses are associated with diminished SIV vaccine efficacy”。

图片来自CC0 Public Domain。
当疫苗接种产生太多特定类型的I型辅助性T细胞(Th1细胞)时,就会出现问题。这些细胞迁移到粘膜组织,比如直肠、子宫颈和阴道,在大多数感染中,HIV/SIV首先就从粘膜组织进入人体。
这些Th1细胞好比是应对僵尸攻击的第一批反应者。它们最初对抗HIV病毒,但随后被这种病毒接管。论文通讯作者、埃默里大学耶克斯国家灵长类动物研究中心研究员Rama Rao Amara博士说,人们需要的是Tfh细胞,它们停留在淋巴结中,并协助免疫系统产生针对这种病毒的抗体。他说,“我们并不是说Th1细胞是坏的。但是,如果你有太多的Th1细胞,它们会使得疫苗无法产生有效的保护。”
2.Science子刊:临床试验表明抗原竞争会破坏HIV疫苗的效力
doi:10.1126/scitranslmed.aaw1673
许多HIV疫苗旨在产生强大的T细胞反应。T细胞反应与未感染者感染HIV的风险下降和HIV感染者控制病毒复制有关。HIV抗原Gag特异性T细胞主要与感染后控制相关,而HIV抗原Env抗原是保护性抗体的作用靶标。 因此,HIV疫苗设计中通常包含这两种抗原。但是,包含多种抗原可能会引起抗原竞争,从而降低疫苗的潜在效力。
在一项新的临床研究中,来自美国、巴西、秘鲁和瑞士的研究人员给研究参与者仅接种HIV 抗原Gag/Pol,或者同时接种HIV 抗原Gag/Pol和Env,以便观察抗原竞争是否会干扰CD4 T细胞反应。他们发现当同时接种Gag/Pol和Env时,检测到的针对Gag/Pol的CD4 T细胞反应较低,这表明在疫苗中包含多种抗原可能会阻止最大的T细胞反应。相关研究结果发表在2019年11月20日的Science Translational Medicine期刊上,论文标题为“Antigenic competition in CD4+ T cell responses in a randomized, multicenter, double-blind clinical HIV vaccine trial”。
具体而言,这项称为HVTN 084的临床研究,是一项随机、多中心、双盲1期临床试验,旨在研究Gag/Pol疫苗中添加Env是否会降低Gag/Pol特异性T细胞反应的幅度或广度。五十名志愿者每人肌肉内注射一次1×1010颗粒单位(PU)的rAd5 Gag/Pol和EnvA/B/C(按照3:1:1:1比例混合在一起)或5×109颗粒单位的rAd5 Gag/Pol。在未接种Env的疫苗接种组中,疫苗接种后4周通过细胞因子表达衡量的CD4+ T细胞反应显著高于接种Env的疫苗接种组,不过这两个疫苗接种组之间的CD8+ T细胞反应没有显著差异。他们进一步揭示与Gag/Pol和Env共免疫接种相比,在不存在Env的情况下,Gag/Pol特异性T细胞反应的广度更大。向Gag/Pol疫苗中添加Env抗原导致针对Gag/Pol的CD4+ T细胞反应率和幅度降低,以及抗原表位的宽度也下降了,这就证实了抗原竞争的存在。
3.Science:重磅!突破性的HIV疫苗设计策略崭露头角
doi:10.1126/science.aax4380
在一项新的研究中,来自美国斯克里普斯研究所等研究机构的研究人员成功地对一种先进的HIV疫苗策略进行了原理验证,这种方法也可能有效地保护人们免受其他致命性传染病的侵害。相关研究结果近期发表在Science期刊上,论文标题为“A generalized HIV vaccine design strategy for priming of broadly neutralizing antibody responses”。

斯克里普斯研究所的科学家们是设计和测试一种新候选疫苗(绿色和蓝色)的研究团队的一部分,这种候选疫苗与HIV广泛中和抗体的前体(棕褐色)结合,有望成为HIV多阶段疫苗的第一阶段。图片来自Schief实验室。
这种新的疫苗策略集中在刺激免疫系统以产生针对HIV的广泛中和抗体(bnAb)。这些特殊的抗体能够结合到HIV病毒表面上重要的但难以接近的区域,而且这些区域在不同HIV毒株之间的差异并不大,因此它们可以中和许多不同的快速突变的HIV毒株。产生此类抗体的疫苗可以挽救数百万人的生命和节省数十亿美元,并最终可能有助于消除艾滋病这一重大的公共卫生问题。基于一种称为“生殖系靶向(germline targeting)”的概念,这种新的策略可能阻止在全球传播的数百万种不同的病毒毒株。迄今为止,实现这一目标还很困难。从未发现有任何候选HIV疫苗能在人体内诱导保护性的bnAb反应。
Schief及其同事们先前在一种特殊情况下展示了一种生殖系靶向策略:bnAb以一种不寻常的方式捕获HIV。这种新方法功能更强大,这是因为它适用于通过一种更为常见的机制捕获靶标的抗体。此外,这项研究中进行的分析表明这种方法也可能适用于制备针对许多其他难治病原体的疫苗,比如流感病毒、登革热病毒、寨卡病毒、丙型肝炎病毒和疟原虫。为了证实这种策略的可行性,Schief和论文共同第一作者、Schief实验室高级科学家Jon Steichen博士首先选择了一种已知的称为BG18的HIV bnAb作为测试案例。通过对BG18与HIV病毒上的靶标结合在一起时的结构研究,这些研究人员鉴定出这种抗体的HIV捕获能力的关键特征。接下来,他们搜索了一个庞大的人类抗体基因数据库,以便寻找产生的抗体与BG18的关键特征天然相同的B细胞。他们随后使用一种复杂的策略来选择和进化一组可能潜在地激活多种BG18样B细胞(BG18-like B cell)的病毒模拟蛋白。这些蛋白最终将作为“免疫原”刺激接受疫苗接种的人体中的BG18样B细胞。对来自HIV阴性人类捐赠者的血液样本进行的测试证实这些研究人员设计出的免疫原与正常循环的具有所需的BG18样特征的B细胞良好地结合。
4.Cell Rep:疟疾领域新发现有助于HIV的治疗
doi:10.1016/j.celrep.2019.10.087
根据最近一项研究,来自澳大利亚研究人员发现免疫系统对疟疾感染作出的反应可能有助于开发针对丙型肝炎,艾滋病毒和狼疮的新型治疗方法。研究者们通过实验室模型发现,由疟疾感染引起的强烈炎症信号激活了特定分子,这些分子触发了抵抗疾病的高效抗体的产生。相关结果发表在《Cell Reports》杂志上。
Hansen博士和她的团队在过去的十年中一直在探索宿主免疫系统如何应对疟疾感染。“在我们以前的论文中,我们证明了炎症信号激活了阻止辅助性T细胞发育的分子,这意味着B细胞没有获得制造抗体的必要指令。当我们开始这项研究时,我们期望看到炎症也对B细胞产生了负面影响。事实上,我们发现情况恰恰相反。炎症信号传给B细胞进而提高了抗体的质量。”
Hansen博士说,她希望这一发现将在疟疾之外发挥作用。她说:“我认为这项发现提供了治疗慢性病毒感染和自身免疫性疾病的机会。我们已经确定了驱动免疫系统产生强效抗体的分子'开关',以及影响其功能的炎症信号。针对该分子或同一途径中的其他分子,可以提供治疗这些疾病的精密手段”。
在包括疟疾和病毒感染(如HIV和慢性丙型肝炎)在内的慢性感染中,产生非常高质量的有效抗体对于清除感染至关重要。另一方面,能够产生针对自身抗原(人体自身的蛋白质和组织)的抗体的B细胞则是导致自身免疫性疾病,例如狼疮的根本原因。
5.Menopause:女性HIV感染者具有增加的过早绝经风险
doi:10.1097/GME.0000000000001423
由于医学的进步,HIV阳性的女性如今具有更长的预期寿命,但这让她们面临许多中年健康问题,比如绝经(menopause, 也译作更年期)。一项新研究表明,感染HIV的女性更可能在平均48岁时进入绝经,比一般人群年轻3岁。相关研究结果近期发表在Menopause期刊上,论文标题为“Prevalence and correlates of early-onset menopause among women living with HIV in Canada”。

HIV-1病毒,图片来自 J Roberto Trujillo/Wikipedia。
加拿大和美国女性的绝经平均年龄在50至52岁之间。先前的研究已表明感染HIV的女性出现绝经提前(early menopause, 年龄在40岁和45岁之间)和早绝经(premature menopause, 也称为原发性卵巢功能不足,年龄在小于40岁)的风险增加。但是,来自加拿大的这项研究是已知的第一项确定HIV患者平均绝经年龄、绝经提前(40岁和45岁之间)发生率、早绝经(小于40岁)发生率以及其他影响绝经年龄的相关因素的研究。
这些研究人员证实感染HIV的女性绝经年龄更小,更具体地说48岁,比未感染的女性早3年。这个感染HIV的女性群体还具有更高的绝经提前发生率和早绝经发生率。此外,较低的教育水平和丙型肝炎病毒合并感染也会影响绝经提前风险,其他可能的修正因素包括婚姻状况和出生地区。
6.J Virol:病毒特性或能预测HIV抗体疗法的疗效
doi:10.1128/JVI.01604-19
当前的HIV疗法能够高效减缓患者体内病毒的进展且副作用较小,日常的抗逆转录病毒疗法(ART)使用了HIV药物的组合来对患者进行治疗,然而由于很多原因,一部分HIV-1患者并不能接受ART来进行治疗;即便目前研究人员正在开发一种包括基于抗体疗法在内可选择的治疗手段,但其仍然很难预测哪些患者适合这些昂贵疗法的治疗。
近日,一项刊登在国际杂志Journal of Virology上的研究报告中,来自波士顿医学中心的科学家们通过研究发现,利用特殊病毒的特性或能帮助预测基于抗体的HIV-1疗法的治疗效力。医学博士Manish Sagar表示,利用测序的方法对HIV-1病毒特性进行分析,或能预测特殊抗体疗法的治疗效果,已经鉴定出的病毒特性或许也能用来确定患者未来是否能因特殊抗体疗法而获益,这就能够有效减少患者治疗的时间和成本。
抗体疗法能够结合保护HIV-1免于宿主免疫系统反应的包膜蛋白,这些包膜蛋白拥有广泛的DNA序列变异,其能提供病毒的信息以及疗法是否能有效给患者带来帮助,但研究者很难仅通过了解包膜的序列来预测基于抗体的疗法是否有效,因此通过在患者开始接受HIV-1治疗之前就能获得序列信息,从而确定其体内的病毒是否对疗法敏感。这项研究中,研究人员鉴别出了HIV-1包膜序列的基序特性并能预测特殊抗体疗法给患者带来的治疗潜力。
7.JCI:新型DNA技术用于靶向输送抗HIV药物
doi:10.1172/JCI132779
近日,Wistar研究所的科学家利用基于合成DNA的技术来促进小动物和大动物模型中产生HIV广谱性中和抗体,为简单有效的下一代HIV预防和治疗方法提供了概念验证。这些结果在线发表在《Journal of Clinical Investigation》杂志上。
尽管抗逆转录病毒疗法在治疗HIV感染方面取得了非凡的进步,但仍需要新的预防和治疗方法以根除HIV感染。研究人员从受感染的个体中分离出许多非常有效的单克隆抗体,这些抗体可以中和各种各样的HIV毒株。这样的单克隆抗体可以作为被动免疫疗法生产和施用,并且代表了目前在早期临床研究中有希望的方法。

图片来源:NIAID。
首席研究员,执行副总裁兼董事David B. Weiner博士说:“我们开发了DMAb平台,以允许通过合成DNA直接体内产生抗体,而合成DNA的目的是向人体提供制造所需抗体的指导。根据我们的早期数据,我们认为该平台作为HIV抗体递送的新策略值得进一步研究。”
Weiner和合作者设计了一个由16个DMAb组成的小组,将先前表征的广泛中和抗体重新合成为DMAb。使用Cellectra自适应电穿孔法通过注射导入小鼠体内并进行了研究。研究人员观察到快速DMAb表达和血液中长达数月的稳定水平。此外,与相应的重组抗体相比,体内产生的DMAbs具有很强的中和能力。由于HIV病毒能够突变以逃避单一抗体的免疫力,因此测试了多达四个不同DMAb的组合作为克服耐药性的策略。组合产生的抗体的体内总水平与单独给药的相同抗体的水平之和相当,表明该方法具有灵活性,适用于多种抗体的联合治疗。重要的是,数据支持这种组合比单一抗体可以阻止更多的HIV病毒。
接下来,研究人员在一项非人类灵长类动物试验性研究中探索了HIV-1 DMAb的递送,该研究与向临床转化更为相关。研究结果表明,注入一或两种组合的DMAb后,三天就可以在体内检测到表达,到14天时显示出峰值活性。重要的是,来自上述动物的血清具有很高的抗病毒活性。
8.JAIDS:重磅!自2000年以来科学家们首次发现新型HIV毒株
doi:10.1097/QAI.0000000000002246
近日,一项刊登在国际杂志Journal of Acquired Immune Deficiency Syndromes上的研究报告中,来自雅培公司等机构的科学家们通过研究宣布,自2000年以来他们发现了全球首个HIV病毒新亚型。研究者Rodgers表示,我们一直在寻找病毒,很多人可能并没有意识到HIV有不止一种毒株,如今研究者正在对鉴别出的所有HIV毒株进行测试来了解其不同的毒株类型。
这种新发现的HIV毒株为HIV-1 M群、L亚型,于20世纪80年代首次收集自刚果民主共和国,但仅有两份样本能通过基因测序来进行检测,研究者需要第三个样本才能够确定病毒的形式,2001年,他们收集了一份非常相似的样本,但该样本并不能进行完全测序,当然了,研究者也无法合成病毒,而样本数量也太少了。
如今,在测序技术的帮助下,研究者证实,L亚型毒株属于HIV病毒M群的突变体,而M群病毒是AIDS流行的罪魁祸首;尽管研究人员并不清楚这种新型亚型毒株如何影响机体,但他们推测,这种病毒与其它M群毒株的行为方式大致相同。这项研究非常重要,其对于开发新型HIV疗法具有重要意义。
9.JCI:三种抗体介导的免疫反应增加与HIV传播风险下降有关
doi:10.1172/JCI126391
与感染风险下降相关的免疫反应称为保护相关因素(correlates of protection, CoP)。测量疫苗诱导的抗体和细胞介导的免疫反应的临床试验有助于确定针对HIV的保护相关因素,这对于评估一种有前景的HIV候选疫苗的疗效是必要的。
在来自受到美国国家过敏与传染病研究所(NIAID)资助的HIV疫苗试验网络(HIV Vaccine Trials Network, HVTN)的资深作者Georgia Tomaras、Peter Gilbert和论文第一作者Scott Neidich、Youyi Fong和Shuying Li的领导下,一项新的初步临床研究证实三种抗体介导的免疫反应---抗体介导的Fcγ受体(FcγR)招募、抗体依赖的细胞吞噬作用(ADCP)和抗Env IgG3--的增加与HIV传播减少有关。相关研究结果近期发表在Journal of Clinical Investigation期刊上,论文标题为“Antibody Fc effector functions and IgG3 associate with decreased HIV-1 risk”。

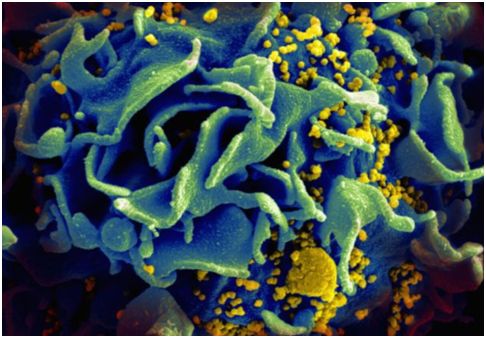
关于受HIV感染的T细胞的扫描电镜图,图片来自NIAID。
值得注意的是,针对这些抗体反应而言,ADCP和IgG3是与HIV传播减少相关的最强相关因素。然而,FcγRIIa参与是受到HIV感染的疫苗接种者中病毒载量下降的唯一相关因素。ADCP、IgG3和FcR参与是新提出的保护相关因素,可在全球正在进行的HVTN 702、HVTN 705和HVTN 706大规模HIV疫苗功效临床试验完成后加以验证。
10.Mol Ther:相似机制!HIV药物能够有效治疗寨卡病毒感染
doi:10.1016/j.ymthe.2019.10.006
众所周知,开发能够适应不同病毒复制机制的药物将极大地提高不同类型传染病的治疗手段。在一项新的工作中,坦普尔大学医学院的研究人员表明,利用现有药物来治疗其它类型病毒性疾病实际上是可能的。
坦普尔的研究人员在《Molecular Therapy》杂志上发表的一项新研究发现,用于治疗HIV的药物同时也可以抑制Zika病毒感染。在细胞和动物模型中,他们表明这种名为rilpivirine的药物通过靶向HIV和Zika病毒复制所依赖的酶来抑制Zika病毒感染。实际上,这些酶存在于Zika病毒以及其它密切相关的病毒中,包括登革热,黄热,西尼罗河热和丙型肝炎等等。
“ HIV和Zika病毒是不同类型的RNA病毒,”文章作者,神经病毒学中心主任以及LKSOM综合神经艾滋病中心主任博士Kamel Khalili博士解释道:“我们发现rilpivirine通过结合RNA病毒家族共有的RNA聚合酶来阻断Zika病毒复制,因此,我们开辟了使用相同策略潜在地治疗多种RNA病毒感染的途径。”
11.Gut:HIV药物利匹韦林或能有效改善机体肝纤维化症状
doi:10.1136/gutjnl-2019-318372
近日,一项刊登在国际杂志Gut上题为“Rilpivirine attenuates liver fibrosis through selective STAT1-mediated apoptosis in hepatic stellate cells”的研究报告中,来自西班牙瓦伦西亚大学等机构的科学家们通过研究发现,一种用于治疗HIV的抗逆转录病毒药物—利匹韦林(Rilpivirine)或对慢性肝脏疾病具有有益效应,相关研究结果或有望帮助开发治疗肝脏疾病的新型疗法。
文章中,研究者表示,当对不同的肝脏损伤临床前模型进行研究后他们发现,用于治疗HIV感染的药物利匹韦林或能有效降低模型机体中的肝脏纤维化程度。目前研究人员需要寻找能够有效治疗肝纤维化患者的选择性疗法,这些疗法能作用于星状细胞的失活并促进肝脏组织再生。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


