Science:重磅!突破性的HIV疫苗设计策略崭露头角
来源:本站原创 2019-11-11 11:46
2019年11月11日讯/生物谷BIOON/---在一项新的研究中,来自美国斯克里普斯研究所等研究机构的研究人员成功地对一种先进的HIV疫苗策略进行了原理验证,这种方法也可能有效地保护人们免受其他致命性传染病的侵害。相关研究结果近期发表在Science期刊上,论文标题为“A generalized HIV vaccine design strategy for priming of broadly
2019年11月11日讯/生物谷BIOON/---在一项新的研究中,来自美国斯克里普斯研究所等研究机构的研究人员成功地对一种先进的HIV疫苗策略进行了原理验证,这种方法也可能有效地保护人们免受其他致命性传染病的侵害。相关研究结果近期发表在Science期刊上,论文标题为“A generalized HIV vaccine design strategy for priming of broadly neutralizing antibody responses”。
这种新的疫苗策略集中在刺激免疫系统以产生针对HIV的广泛中和抗体(bnAb)。这些特殊的抗体能够结合到HIV病毒表面上重要的但难以接近的区域,而且这些区域在不同HIV毒株之间的差异并不大,因此它们可以中和许多不同的快速突变的HIV毒株。
产生此类抗体的疫苗可以挽救数百万人的生命和节省数十亿美元,并最终可能有助于消除艾滋病这一重大的公共卫生问题。基于一种称为“生殖系靶向(germline targeting)”的概念,这种新的策略可能阻止在全球传播的数百万种不同的病毒毒株。迄今为止,实现这一目标还很困难。从未发现有任何候选HIV疫苗能在人体内诱导保护性的bnAb反应。
论文共同通讯作者、斯克里普斯研究所免疫学与微生物学系教授William Schief博士说,“我认为我们需要一种生殖系靶向策略来开发一种有效的抗HIV疫苗,而且这种相同类型的策略可能有助于制备抵抗许多其他难治的病原体的疫苗。在这里,通过多个实验室之间的大力合作,我们证实了一种通用的生殖系靶向策略的可行性。”
这项研究吸引了来自不同背景和专业领域的科学家:Schief;论文共同通讯作者、麻省总医院拉根研究所首席科学官Facundo Batista博士;论文共同通讯作者、拉霍亚免疫学研究所疫苗发现部门教授Shane Crotty博士。Batista说:“这是一个雄心勃勃的项目,需要采取多学科的方法,只有依靠合作才能成功。”
这种生殖系靶向方法旨在通过刺激正确的产生抗体的细胞来促进所需的bnAb产生。抗体是由称为B细胞的免疫细胞产生的,这些免疫细胞最初处于一种“初始(na?ve)”或“生殖系”状态。
大量生殖系B细胞在血液和其他组织中循环。在病毒感染中或者在接种模拟感染病毒的疫苗后,一些生殖系B细胞将至少微弱地结合到位于病毒表面的结构上。这将刺激这些细胞开始长达数周的成熟过程,在这个过程中,抗体不断提高它们与病毒表面结合的能力,从而最终能够中和病毒。
针对HIV疫苗的生殖系靶向策略旨在刺激少数B细胞,使得它们能够成熟为产生bnAb的细胞。这些研究人员猜测其他制备诱导bnAb产生的HIV疫苗的尝试失败了,这是因为它们没有刺激足够数量的“bnAb前体”生殖系B细胞。
Schief及其同事们先前在一种特殊情况下展示了一种生殖系靶向策略:bnAb以一种不寻常的方式捕获HIV。这种新方法功能更强大,这是因为它适用于通过一种更为常见的机制捕获靶标的抗体。此外,这项研究中进行的分析表明这种方法也可能适用于制备针对许多其他难治病原体的疫苗,比如流感病毒、登革热病毒、寨卡病毒、丙型肝炎病毒和疟原虫。
为了证实这种策略的可行性,Schief和论文共同第一作者、Schief实验室高级科学家Jon Steichen博士首先选择了一种已知的称为BG18的HIV bnAb作为测试案例。通过对BG18与HIV病毒上的靶标结合在一起时的结构研究,这些研究人员鉴定出这种抗体的HIV捕获能力的关键特征。
接下来,他们搜索了一个庞大的人类抗体基因数据库,以便寻找产生的抗体与BG18的关键特征天然相同的B细胞。他们随后使用一种复杂的策略来选择和进化一组可能潜在地激活多种BG18样B细胞(BG18-like B cell)的病毒模拟蛋白。这些蛋白最终将作为“免疫原”刺激接受疫苗接种的人体中的BG18样B细胞。
Steichen说,“鉴于B细胞库的组成因人而异,并且随着时间的推移,在同一个人体内也存在差异,因此我们认为需要靶向这些B细胞中的多个以上才有合理的机会在任何给定的疫苗接种者中激活它们中的一个。”
在拉荷亚免疫学研究所的Shane Crotty实验室中,对来自HIV阴性人类捐赠者的血液样本进行的测试证实这些研究人员设计出的免疫原与正常循环的具有所需的BG18样特征的B细胞良好地结合。
论文共同第一作者、Crotty实验室高级科学家Colin Havenar-Daughton博士说:“其中的一些B细胞正是我们所寻找的细胞类型。”在斯克里普斯研究所Andrew Ward博士的实验室里进行的低温电镜分析表明这些B细胞产生的抗体在原子水平上模拟了BG18的结构。
麻省总医院拉根研究所Facundo Batista实验室在经过基因改造后携带BG18前体B细胞的小鼠中开展了实验,他们的实验表明这些免疫原可以激活这些B细胞,从而诱导强效的抗体反应。
论文共同第一作者、Batista实验室博士后研究员Ying-Cing Lin博士说,“我们培育出携带罕见BG18前体和高水平竞争性B细胞的小鼠模型,从而模拟了在人体免疫接种过程中遇到的生理状况。我们发现这些设计出的免疫原刺激BG18前体产生强烈而又特异性的免疫反应,而且所产生的这些抗体显示出它们正在朝正确方向成熟的迹象。”
这些研究结果提示着这些研究人员设计出的免疫原可以在旨在诱导BG18和密切相关的bnAb产生的多阶段疫苗的初次接种阶段发挥作用。他们如今计划为随后的疫苗阶段开发免疫原,以“指导”针对bnAb的抗体反应。他们设想了一种最终的HIV疫苗,它结合了上述几种努力,从而诱发多种类型的bnAb来对抗HIV。(生物谷 Bioon.com)
参考资料:
1.Jon M. Steichen et al. A generalized HIV vaccine design strategy for priming of broadly neutralizing antibody responses. Science, 2019, doi:10.1126/science.aax4380.
2.Groundbreaking HIV vaccine design strategy shows promise in proof-of-principle tests
https://www.scripps.edu/news-and-events/press-room/2019/20191031-schief-HIV.html

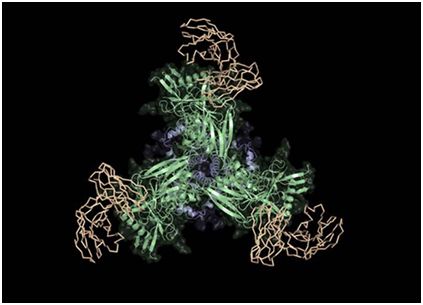
斯克里普斯研究所的科学家们是设计和测试一种新候选疫苗(绿色和蓝色)的研究团队的一部分,这种候选疫苗与HIV广泛中和抗体的前体(棕褐色)结合,有望成为HIV多阶段疫苗的第一阶段。图片来自Schief实验室。
这种新的疫苗策略集中在刺激免疫系统以产生针对HIV的广泛中和抗体(bnAb)。这些特殊的抗体能够结合到HIV病毒表面上重要的但难以接近的区域,而且这些区域在不同HIV毒株之间的差异并不大,因此它们可以中和许多不同的快速突变的HIV毒株。
产生此类抗体的疫苗可以挽救数百万人的生命和节省数十亿美元,并最终可能有助于消除艾滋病这一重大的公共卫生问题。基于一种称为“生殖系靶向(germline targeting)”的概念,这种新的策略可能阻止在全球传播的数百万种不同的病毒毒株。迄今为止,实现这一目标还很困难。从未发现有任何候选HIV疫苗能在人体内诱导保护性的bnAb反应。
论文共同通讯作者、斯克里普斯研究所免疫学与微生物学系教授William Schief博士说,“我认为我们需要一种生殖系靶向策略来开发一种有效的抗HIV疫苗,而且这种相同类型的策略可能有助于制备抵抗许多其他难治的病原体的疫苗。在这里,通过多个实验室之间的大力合作,我们证实了一种通用的生殖系靶向策略的可行性。”
这项研究吸引了来自不同背景和专业领域的科学家:Schief;论文共同通讯作者、麻省总医院拉根研究所首席科学官Facundo Batista博士;论文共同通讯作者、拉霍亚免疫学研究所疫苗发现部门教授Shane Crotty博士。Batista说:“这是一个雄心勃勃的项目,需要采取多学科的方法,只有依靠合作才能成功。”
这种生殖系靶向方法旨在通过刺激正确的产生抗体的细胞来促进所需的bnAb产生。抗体是由称为B细胞的免疫细胞产生的,这些免疫细胞最初处于一种“初始(na?ve)”或“生殖系”状态。
大量生殖系B细胞在血液和其他组织中循环。在病毒感染中或者在接种模拟感染病毒的疫苗后,一些生殖系B细胞将至少微弱地结合到位于病毒表面的结构上。这将刺激这些细胞开始长达数周的成熟过程,在这个过程中,抗体不断提高它们与病毒表面结合的能力,从而最终能够中和病毒。
针对HIV疫苗的生殖系靶向策略旨在刺激少数B细胞,使得它们能够成熟为产生bnAb的细胞。这些研究人员猜测其他制备诱导bnAb产生的HIV疫苗的尝试失败了,这是因为它们没有刺激足够数量的“bnAb前体”生殖系B细胞。
Schief及其同事们先前在一种特殊情况下展示了一种生殖系靶向策略:bnAb以一种不寻常的方式捕获HIV。这种新方法功能更强大,这是因为它适用于通过一种更为常见的机制捕获靶标的抗体。此外,这项研究中进行的分析表明这种方法也可能适用于制备针对许多其他难治病原体的疫苗,比如流感病毒、登革热病毒、寨卡病毒、丙型肝炎病毒和疟原虫。
为了证实这种策略的可行性,Schief和论文共同第一作者、Schief实验室高级科学家Jon Steichen博士首先选择了一种已知的称为BG18的HIV bnAb作为测试案例。通过对BG18与HIV病毒上的靶标结合在一起时的结构研究,这些研究人员鉴定出这种抗体的HIV捕获能力的关键特征。
接下来,他们搜索了一个庞大的人类抗体基因数据库,以便寻找产生的抗体与BG18的关键特征天然相同的B细胞。他们随后使用一种复杂的策略来选择和进化一组可能潜在地激活多种BG18样B细胞(BG18-like B cell)的病毒模拟蛋白。这些蛋白最终将作为“免疫原”刺激接受疫苗接种的人体中的BG18样B细胞。
Steichen说,“鉴于B细胞库的组成因人而异,并且随着时间的推移,在同一个人体内也存在差异,因此我们认为需要靶向这些B细胞中的多个以上才有合理的机会在任何给定的疫苗接种者中激活它们中的一个。”
在拉荷亚免疫学研究所的Shane Crotty实验室中,对来自HIV阴性人类捐赠者的血液样本进行的测试证实这些研究人员设计出的免疫原与正常循环的具有所需的BG18样特征的B细胞良好地结合。
论文共同第一作者、Crotty实验室高级科学家Colin Havenar-Daughton博士说:“其中的一些B细胞正是我们所寻找的细胞类型。”在斯克里普斯研究所Andrew Ward博士的实验室里进行的低温电镜分析表明这些B细胞产生的抗体在原子水平上模拟了BG18的结构。
麻省总医院拉根研究所Facundo Batista实验室在经过基因改造后携带BG18前体B细胞的小鼠中开展了实验,他们的实验表明这些免疫原可以激活这些B细胞,从而诱导强效的抗体反应。
论文共同第一作者、Batista实验室博士后研究员Ying-Cing Lin博士说,“我们培育出携带罕见BG18前体和高水平竞争性B细胞的小鼠模型,从而模拟了在人体免疫接种过程中遇到的生理状况。我们发现这些设计出的免疫原刺激BG18前体产生强烈而又特异性的免疫反应,而且所产生的这些抗体显示出它们正在朝正确方向成熟的迹象。”
这些研究结果提示着这些研究人员设计出的免疫原可以在旨在诱导BG18和密切相关的bnAb产生的多阶段疫苗的初次接种阶段发挥作用。他们如今计划为随后的疫苗阶段开发免疫原,以“指导”针对bnAb的抗体反应。他们设想了一种最终的HIV疫苗,它结合了上述几种努力,从而诱发多种类型的bnAb来对抗HIV。(生物谷 Bioon.com)
参考资料:
1.Jon M. Steichen et al. A generalized HIV vaccine design strategy for priming of broadly neutralizing antibody responses. Science, 2019, doi:10.1126/science.aax4380.
2.Groundbreaking HIV vaccine design strategy shows promise in proof-of-principle tests
https://www.scripps.edu/news-and-events/press-room/2019/20191031-schief-HIV.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


