全球BCMA靶向疗法!GSK抗体药物偶联物belantamab mafodotin获美国FDA委员会全票通过!
来源:本站原创 2020-07-15 20:33
目前,该药正在接受美国FDA优先审查和欧盟EMA加速评估。

2020年07月15日讯 /生物谷BIOON/ --葛兰素史克(GSK)近日宣布,美国食品和药物管理局(FDA)肿瘤药物咨询委员会(ODAC)以12-0的投票结果,支持belantamab mafodotin(GSK2857916)的临床益处大于其风险:该药是一种靶向B细胞成熟抗原(BCMA)的抗体药物偶联物(ADC),作为一种单药疗法,用于治疗先前已接受过至少4种疗法(包括一种免疫调节剂、一种蛋白酶体抑制剂、一种抗CD38抗体)的复发或难治性多发性骨髓瘤(MM)患者。该委员会的2名成员未能参加最后表决。
值得注意的是,在召开ODAC会议之前,FDA内部审查员对belantamab mafodotin与眼睛相关的不良事件表达了关注。FDA在做出最终审查决定时,将会考虑ODAC的建议,尽管其建议并不具有约束力。
目前,belantamab mafodotin正在接受美国FDA的优先审查和欧盟EMA的加速评估。如果获得批准,该药将成为上市的第一个BCMA靶向疗法。在2017年,belantamab mafodotin获得美国FDA授予突破性药物资格(BTD)以及欧盟EMA授予优先药物资格(PRIME),该药也是第一个被授予BTD和PRIME的BCMA靶向制剂。这些资格认定旨在促进在重大未满足医疗需求领域具有临床前景的在研药物的开发。
葛兰素史克高级副总裁兼肿瘤学研发主管Axel Hoos博士说:“我们很高兴委员会认识到belantamab mafodotin有潜力帮助复发或难治性多发性骨髓瘤患者,这是一种治疗方法有限的不可治愈性疾病。我们期待着与FDA合作完成对该药生物制品许可申请的审查。”
ODAC全票支持的建议,基于DREAMM临床试验项目的数据,包括关键性的DREAMM-2研究。这是一项随机、开放标签、双臂II期研究,共入组了196例既往过度治疗的(heavily pretreated)R/R MM患者,这些患者尽管接受当前的标准治疗但病情恶化、既往接受的治疗方案中位数为7种、对免疫调节药物和蛋白酶体抑制剂难治、并对抗CD38抗体难治和/或不耐受。研究中,患者被随机分为两组,接受每三周一次2.5mg/kg或3.4mg/kg剂量belantamab mafodotin治疗。该研究的6个月初步结果于2019年12月发表于《柳叶刀肿瘤学》,并作为美欧监管申请文件的基础。
今年5月底,GSK在2020年美国临床肿瘤学会年会(ASCO)虚拟会议上公布了该研究的13个月随访数据,结果显示:belantamab mafodotin(2.5mg/kg,每3周一次[Q3W])单药治疗的中位缓解持续时间(DoR)为11个月(95%CI:4.2-未达到)、中位总生存期(OS)为14.9个月(95%CI:9.9-未达到)。ORR数据与6个月数据(ORR=32%)一致。在这些患者中,大多数(58%)患者病情取得了非常好的部分缓解或更好缓解(≥VGPR),包括2例严格的完全缓解(sCR)和5例完全缓解(CR)。获得临床受益的患者比例为36%(95%CI:26.6-46.5)。
长期随访中,没有发现新的安全信号。在接受2.5mg/kg剂量的患者中,最常见的3级或更高级别的不良事件(发生在10%以上的患者中)是角膜病变/微囊藻样上皮改变(MEC;46%)、血小板减少(22%)、贫血(21%)、淋巴细胞计数下降(13%)和中性粒细胞减少(11%)。第一例角膜病变(MEC)的特征是眼部检查所见的角膜上皮细胞的变化,可出现或不出现症状。在数据截止时,2.5 mg/kg剂量组中77%的患者得到了解决,迄今为止还没有永久性视力丧失的报告。
对于接受当前可用的治疗方法但疾病仍在进展的R/R MM患者,治疗选择非常有限,预后也很差。来自DREAMM-2研究的最新结果进一步证明了belantamab mafodotin的潜力。如果获得批准,belantamab mafodotin将为这些患者提供一个重要的新治疗选择,帮助解决重大未满足医疗需求。
belantamab mafodotin作用机制(图片来源文献:DOI:https://doi.org/10.1016/S1470-2045(19)30788-0)
DREAMM临床开发项目共包括10项临床研究(DREAMM-1至DREAMM-10),正在评估belantamab mafodotin作为单药疗法以及用于组合疗法一线、二线及多线治疗MM的疗效和安全性。之前公布的来自首个人体临床研究DREAMM-1的更新数据显示,在BCMA阳性R/R MM患者中,belantamab mafodotin治疗的总缓解率(ORR)达到了60%。
在ASCO年会上,GSK还公布了DREAMM-6研究的数据。该研究在接受一种或多种疗法难治或治疗后病情复发的R/R MM患者中开展,调查了belantamab mafodotin(2.5mg/kg,每3周一次[Q3W])联合硼替佐米/地塞米松(BorDex)的疗效和安全性。
初步结果显示,belantamab mafodotin联合BorDex(B-Vd)治疗的总缓解率(ORR)达到了78%(n=14/18;95%CI:52.4-93.6),50%为非常好的部分缓解(VGPR)、28%为部分缓解(PR)。获得临床受益(最小缓解或更好)的患者比例为83%(95%CI:58.6-96.4)。中位治疗18.2周时,中位DoR尚未达到。3级或以上不良事件包括角膜病变(MEC;56%)和血小板减少(61%)。无4级MEC病例。这些初步结果,证实了belantamab mafodotin联合治疗在多发性骨髓瘤早期患者中的潜力

BCMA为靶点的在研MM免疫疗法(来源文献—PMID:31277554)
多发性骨髓瘤(MM)是仅次于非霍奇金淋巴瘤的第二大常见血液学恶性肿瘤。近年来,尽管在化疗、蛋白酶体抑制剂、免疫调节剂沙利度胺衍生物和CD38靶向抗体方面取得了很大的进展,但几乎所有患者最终仍会复发。因此,对新治疗方案存在着迫切需求。MM市场2017年接近140亿美元,预计2027年将达到近290亿美元。
BCMA是一种极其重要的B细胞生物标志物,广泛存在于MM细胞表面,近年来已成为MM和其他血液系统恶性肿瘤的一个非常热门的免疫治疗靶点。目前,针对BCMA开发的免疫疗法超过20种,主要分为3类:嵌合抗原受体T细胞疗法(CAR-T,新基/蓝鸟生物、诺华为代表)、双特异性抗体(BsAb,安进为代表)、抗体药物偶联物(ADC,葛兰素史克为代表)。
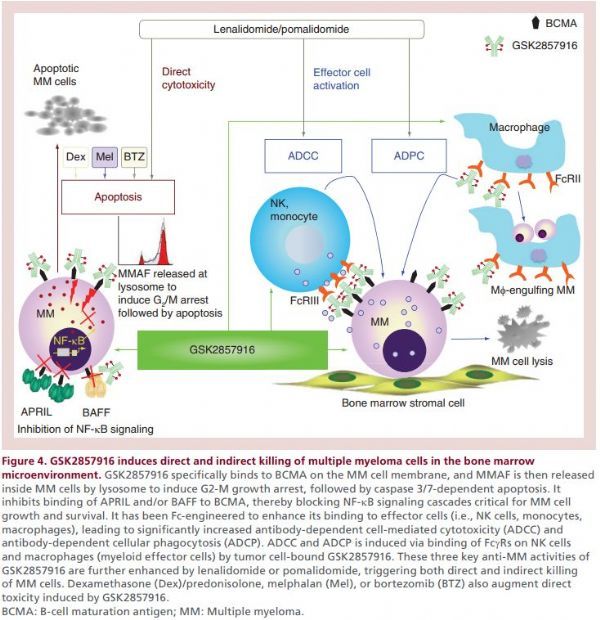
belantamab mafodotin是一种新型人源化Fc-改造过的抗BCMA单抗与细胞毒制剂MMAF(monomethyl auristatin-F)通过一种非裂解链接子(药物链接技术从西雅图遗传学取得授权)偶联而成的ADC药物。belantamab mafodotin通过抗BCMA单抗靶向结合MM细胞表面的BCMA,之后迅速被MM细胞内化,在溶酶体中降解并在MM细胞内释放出非渗透性的MMAF发挥作用。MMAF是一种有丝分裂抑制剂,为抗微管蛋白化合物,能通过阻断微管聚合抑制细胞分裂,可使肿瘤细胞停止于G/M期并诱导caspase-3依赖的细胞凋亡。此外,belantamab mafodotin还能诱导NK细胞介导的ADCC(抗体依赖性细胞介导的细胞毒性作用),同时诱导巨噬细胞介导ADCP(抗体依赖性细胞介导的吞噬作用)。
belantamab mafodotin通过多种细胞毒作用机制选择性作用于MM细胞,有望为该类癌症提供有极具潜力的下一代免疫治疗选择。目前,belantamab mafodotin正处于临床开发,用于R/R MM和其他表达BCMA的晚期血液系统恶性肿瘤患者的治疗。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->