偏头痛急性治疗新药!艾尔建口服CGRP受体拮抗剂ubrogepant将于本月获得美国FDA批准!
来源:本站原创 2019-12-07 11:34
2019年12月07日讯 /生物谷BIOON/ --艾尔建(Allergan)近日宣布,评估ubrogepant用于成人偏头痛急性治疗III期临床研究ACHIEVE I(UBR-MD-01)的阳性结果已发表于12月5日出版的《新英格兰医学杂志》(NEJM)。研究数据进一步证实,在偏头痛急性治疗方面,与安慰剂组相比,2种剂量(50mg和100mg)ubroge

2019年12月07日讯 /生物谷BIOON/ --艾尔建(Allergan)近日宣布,评估ubrogepant用于成人偏头痛急性治疗III期临床研究ACHIEVE I(UBR-MD-01)的阳性结果已发表于12月5日出版的《新英格兰医学杂志》(NEJM)。研究数据进一步证实,在偏头痛急性治疗方面,与安慰剂组相比,2种剂量(50mg和100mg)ubrogepant治疗的患者在给药后2小时达到无疼痛、无偏头痛相关最烦人症状的患者比例显著更高。
目前,ubrogepant用于成人偏头痛急性治疗的新药申请(NDA)正在接受美国FDA的审查,该机构将在今年12月份做出审查决定。如果获得批准,ubrogepant将成为用于偏头痛(有或无先兆)急性治疗的第一种口服降钙素基因相关肽(CGRP)受体拮抗剂。
ACHIEVE I是一项多中心、双盲、平行组III期研究,评估了ubrogepant(50mg和100mg)与安慰剂相比,用于中度或重度头痛疼痛强度单次偏头痛发作急性治疗的疗效、安全性和耐受性。该研究中,共计1672例有偏头痛病史(有或无先兆)的成人患者(18-75岁)被随机(1:1:1)分配接受安慰剂、ubrogepant 50mg、ubrogepant 100mg治疗。研究的共同主要疗效参数是初始剂量后2小时的疼痛消除(无疼痛)和初始剂量后2小时无最烦人的偏头痛相关症状。最烦人的偏头痛相关症状可能包括畏光、声音恐惧或恶心,由受试者在偏头痛发作时选择。次要疗效终点还评估了ubrogrepant在一系列结果测量中的临床益处,包括2小时疼痛缓解、2-24小时持续疼痛缓解和2-24小时持续疼痛消除(无疼痛)等。在首次和可选的第二次给药后48小时以及在任何一次给药后30天内收集和评估不良事件。
结果显示,在2个共同主要终点方面,与安慰剂组相比,2种剂量(50mg和100mg)ubrogepant治疗组在初始给药后2小时实现疼痛消除(无疼痛)的患者比例显著更高且数据具有统计学意义(安慰剂组为11.8%,50mg组为19.2%,100mg组为21.2%)、在初始给药后2小时实现无最烦人偏头痛相关症状的患者比例更高且数据具有统计学意义(安慰剂组为27.8%,50mg组为38.6%,100mg组为37.7%)。
此外,在给药后2小时疼痛缓解的次要终点方面,2种剂量ubrogepant治疗组与安慰剂组相比均显示出显著改善(安慰剂组49.1%,50mg组60.7%,100mg组61.4%)。疼痛缓解定义为在初次给药后2小时头痛严重程度由中度至重度降低至轻度或无疼痛。这一次要终点与FDA以前批准的偏头痛药物(如曲坦类药物)的主要终点最为相似。此外,在2-24小时持续疼痛缓解方面,2种剂量ubrogepant在统计学上均优于安慰剂(安慰剂组20.8%,50mg组36.3%,100mg组38.0%)。
该研究中,50mg和100mg剂量的ubrogepant都具有良好的耐受性,不良事件特征与安慰剂相似。无严重不良反应,最常见的不良反应是恶心,安慰剂组为1.6%,50mg组为1.7%,100mg组为4.1%。所有治疗出现的不良事件发生率也与安慰剂相似(安慰剂组为12.8%,50mg组为9.4%,100mg组为16.3%)。
目前,在偏头痛急性治疗方面,曲坦类药物(triptan)使用最为普遍,占处方的70%。然而,偏头痛患者中,有67%患者报告称,当偏头痛发作时会延迟或避免服用处方药,通常是因为他们在治疗过程中遇到的不良事件。此外,偏头痛患者中大约20%存在多个心血管(CV)风险因素,而曲坦类药物具有收缩血管作用,该类药物可能不适合那些具有CV风险因素的偏头痛患者。在服用曲坦类药物的患者中,多达30%患者可能应答不足或可能会出现副作用。
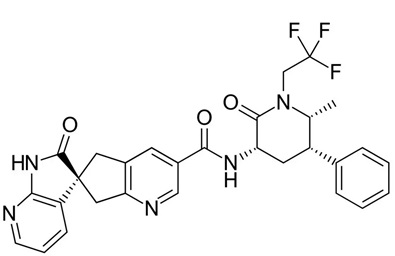
ubrogepant的分子结构式(图片来源:Wikipedia)
在美国,ubrogepant的新药申请(NDA)基于成功完成的4项临床研究——2项关键III期研究(ACHIEVE I,ACHIEVE II)以及2项额外的安全性研究(UBR-MD-04,3110-105-002),这些研究证明了ubrogepant在广泛患者群体(包括对曲坦类药物反应不足的患者,对曲坦类药物禁忌的患者,伴中度至重度心血管风险特征的患者)中对偏头痛的急性治疗的有效性、安全性和耐受性。
ubrogepant是一种新型、高效、口服降钙素基因相关肽(CGRP)受体拮抗剂,目前开发用于急性偏头痛的治疗。CGRP及其受体在与偏头痛病理生理学相关的神经系统区域表达。CGRP受体拮抗作用是偏头痛急性治疗的一种新的作用机制,与现有的曲坦类(血清素1B / 1D激动剂)和阿片类药物的作用机制明显不同。目前,CGRP受体已成为偏头痛药物研发的热门靶点。
截至目前,已有3款靶向CGRP受体的单抗类偏头痛预防性治疗药物上市,分别为:诺华/安进Aimovig(erenumab-aooe)、梯瓦Ajovy(fremanezumab-vfrm)、礼来Emgality(galcanezumab-gnlm)。用药方面,Aimovig和Emgality均每月一次皮下注射,Ajovy则可每月一次或每3个月一次皮下注射,用药方面更具便利性,将为患者提供一种差异化的治疗选择。此外,Alder公司单抗药物eptinezumab(3月静脉输注1次)也于今年2月下旬在美国提交上市申请。另有一些公司正在开发口服CGRP抑制剂,除了艾尔建的ubrogepant和atogepant之外,还包括Biohaven公司的rimegepant。
今年10月,礼来公司产品Reyvow(lasmiditan)获得美国FDA批准,用于成人伴或不伴先兆症状偏头痛的急性治疗。此次批准意义重大,因为Reyvow代表着20多年来FDA批准的首个新一类的急性偏头痛治疗药物。该药活性药物成分为lasmiditan是一种口服、中枢神经系统渗透性、选择性、5-羟色胺1F(5-HT1F)激动剂,在结构上和机制上不同于目前已获批的偏头痛药物,而且不存在血管收缩活性。值得一提的是,lasmiditan是“地坦(-ditan)”类药物中第一个也是唯一一个被批准用于成人偏头痛急性治疗的药物分子。此次批准,代表着20多年来急性偏头痛治疗的首个重大创新。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


