CRM:中国医学科学院肿瘤医院吴晨/林东昕团队发现食管癌对化疗耐药的新机制
来源:网络 2024-05-24 09:26
吴晨、林东昕团队此次找到了食管癌化疗耐药的新机制,证明S100A8可以作为无创预测食管癌化疗反应的生物标志物,靶向S100A8-CD147通路或是克服食管癌化疗耐药性的新策略。
晚期食管癌的首选治疗为化疗,可却长期陷于耐药性的瓶颈之中。近日,一篇发表在Cell Reports Medicine期刊上的论文提出[1],食管癌细胞能够引诱肿瘤相关成纤维细胞(CAFs)为自己打造防护服,逃避死亡。
中国医学科学院肿瘤医院的吴晨、林东昕团队首次揭示,食管鳞状细胞癌(ESCC)细胞能够通过释放S100A8蛋白诱导CAFs转变为肿瘤相关肌成纤维细胞(myCAFs),myCAFs继而激活肿瘤细胞的抗凋亡信号通路,导致化疗耐药。
抑制S100A8介导的关键信号通路,可以提高食管癌小鼠的化疗敏感性。此外还证明,患者外周血中的S100A8水平可以作为预测化疗反应的生物标志物。

论文首页截图
在肿瘤微环境中,恶性细胞与多种非恶性细胞共存,包括肿瘤相关成纤维细胞(CAFs)、内皮细胞、肿瘤浸润淋巴细胞等。其中,CAFs具有异质性,在不同的刺激下可能会偏向形成肿瘤相关肌成纤维细胞(myCAFs)、炎症型成纤维细胞(iCAFs)或抗原呈递型成纤维细胞(apCAFs),以促进癌症进展和侵袭[2]。不过,彻底清除CAFs也会促使肿瘤侵袭,因此最为安全有效的办法是将其劝服,从促癌状态转变回来。
此次,为揭秘食管癌化疗耐药性之谜,吴晨、林东昕团队利用20名食管鳞状细胞癌(ESCC)患者的肿瘤样本,建立了患者衍生异种移植(PDX)小鼠模型。当肿瘤移植物达到150mm³大小时,小鼠开始接受三个周期的5-FU/CDDP化疗或安慰剂治疗。
经过对比分析肿瘤生长情况、细胞转录组特征、细胞外基质(ECM)组成,研究团队找到了化疗耐药的食管癌小鼠的与众不同之处:myCAFs在肿瘤组织中富集,并且发生由myCAFs介导的ECM重塑和胶原蛋白异常沉积。
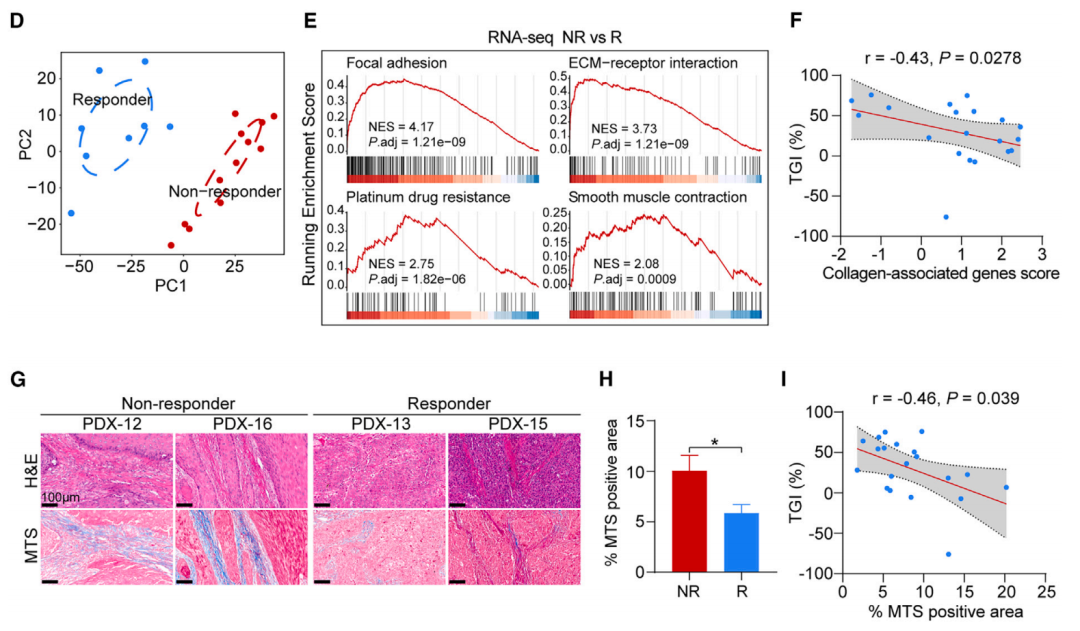
myCAFs在化疗无响应小鼠肿瘤中富集,且胶原蛋白异常沉积
越来越多的证据表明,肿瘤细胞可以通过分泌细胞因子引诱CAF转化为多种促癌表型,为自己所用。于是研究团队将目光转向食管癌小鼠的肿瘤细胞。
结果显示,化疗耐药的食管癌小鼠肿瘤细胞中S100A8蛋白表达显著上调。S100A8是属于S100蛋白家族的钙结合蛋白,通常与S100A9蛋白形成异源二聚体,通过与细胞外受体TLR4、RAGE、CD147等结合发挥作用。
在排除肿瘤细胞分泌的S100A8是以自分泌的方式来影响肿瘤生长后,研究团队评估S100A8对CAFs的作用。他们发现,在食管癌PDX小鼠模型中,S100A8敲低表达能够增加化疗敏感性,即使没有接受化疗也会导致小鼠肿瘤细胞生长减缓,且小鼠肿瘤微环境中的胶原蛋白沉积和CAFs活性化程度降低,血管内皮细胞数量没有改变。
接下来的研究揭示,ESCC肿瘤细胞如何使用S100A8引诱CAFs协助自己完成这场逃生表演。
ESCC肿瘤细胞分泌的S100A8通过与CAFs表面的CD147受体结合,启动细胞内RhoA-ROCK-MLC2-MRTF-A信号通路,推动CAFs从静态转变为具有高度活性的myCAFs。数量增加、活性提高的myCAFs在肿瘤微环境中促进ECM的重塑和胶原蛋白的沉积,已有研究表明这会形成阻碍药物输送和免疫细胞浸润的物理屏障[3,4];另一方面,研究团队此次发现,myCAFs能够激活ESCC肿瘤细胞的FAK/SRC/ERK抗凋亡通路,增强ESCC的化疗耐药性。
食管癌PDX小鼠实验结果显示,使用特异性抑制剂AC-73对S100A8-CD147通路进行阻断,能够阻碍myCAFs的激活并削弱其对肿瘤细胞的保护作用,且AC-73治疗对体重影响忽略不计。与单独化疗相比,AC-73与化疗的组合显著抑制肿瘤生长。

AC-37增加化疗敏感性
为确定S100A8的临床意义,研究团队收集152名接受过新辅助化疗的ESCC患者的外周血样本。结果显示,对化疗无响应的患者S100A8血液水平显著高于对化疗有响应的患者。在调整年龄、性别、组织学分级、TNM分期和治疗周期等多因素后,仍显示S100A8/S100A9血液水平高与化疗耐药紧密相关(OR 2.21;95%CI 1.09-4.48;p=0.029),这表明S100A8/S100A9水平可作为评估患者化疗反应的独立风险因素。
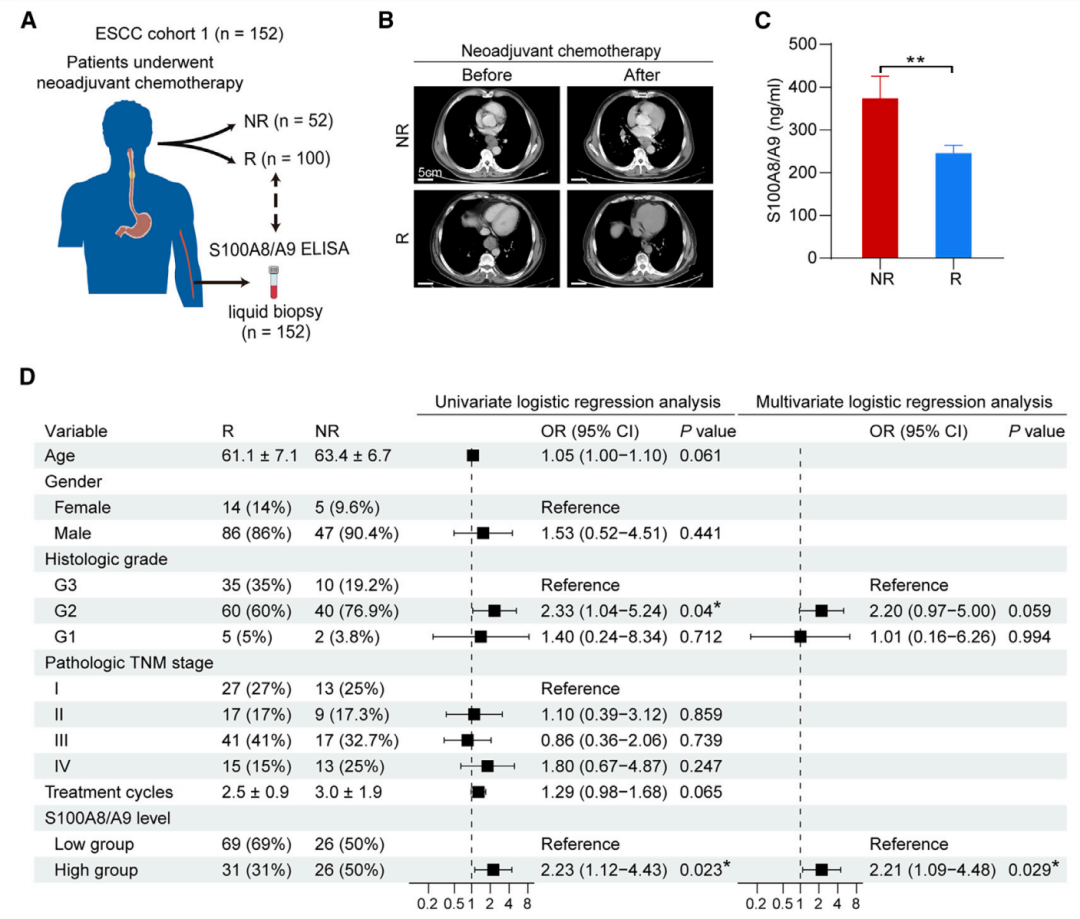
S100A8/S100A9水平可作为评估患者化疗反应的独立风险因素
另外一组包括21名ESCC患者的小型队列分析结果显示,S100A8/S100A9高表达与生存时间短相关(p=0.04;p=0.02)。
研究团队还使用癌症基因组图谱(TCGA)数据进行统计分析,发现在宫颈癌、肝癌、膀胱癌、胰腺癌、头颈癌、胶质母细胞瘤和肾透明细胞癌中,S100A8/S100A9水平与接受化疗的患者总生存期显著负相关。
这些结果表明,不仅是ESCC,S100A8血液水平有望成为跨癌种的化疗预后生物标志物,未来需要更大规模的前瞻性临床研究进行验证。
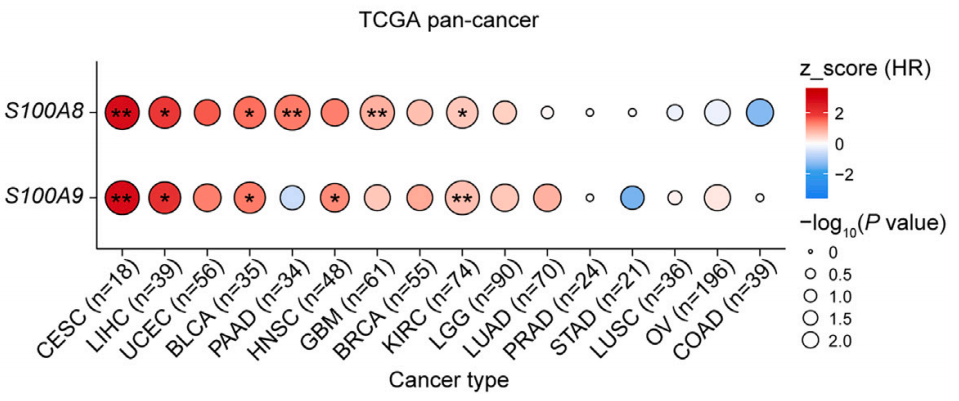
S100A8血液水平有望成为跨癌种的化疗预后生物标志物
总之,吴晨、林东昕团队此次找到了食管癌化疗耐药的新机制,证明S100A8可以作为无创预测食管癌化疗反应的生物标志物,靶向S100A8-CD147通路或是克服食管癌化疗耐药性的新策略。
参考文献:
[1]https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00268-4
[2]Kalluri, R. (2016). The biology and function of fibroblasts in cancer. Nat.
Rev. Cancer 16, 582–598. https://doi.org/10.1038/nrc.2016.73.
[3]Shi, Y., Du, L., Lin, L., and Wang, Y. (2017). Tumour-associated mesenchymal stem/stromal cells: emerging therapeutic targets. Nat. Rev. Drug
Discov. 16, 35–52. https://doi.org/10.1038/nrd.2016.193.
[4]Sleeboom, J.J.F., van Tienderen, G.S., Schenke-Layland, K., van der
Laan, L.J.W., Khalil, A.A., and Verstegen, M.M.A. (2024). The extracellular
matrix as hallmark of cancer and metastasis: From biomechanics to therapeutic targets. Sci. Transl. Med. 16, eadg3840. https://doi.org/10.1126/
scitranslmed.adg3840.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


