胃食管腺癌(GEA)新药!HER2双特异性抗体zanidatamab一线治疗HER2阳性GEA:总缓解率68.2%!
来源:本站原创 2021-09-14 01:35
2018年11月,百济神州签订4亿美元协议,获得zanidatamab在亚洲(除日本外)、澳大利亚、新西兰的独家权利。
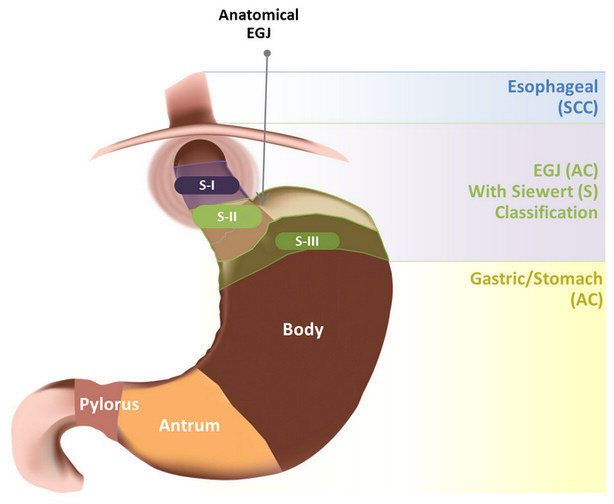
胃食管癌分类(图片来源于文献PMID-23998446)
2021年09月13日讯 /生物谷BIOON/ --百济神州合作伙伴Zymeworks是一家临床阶段的生物制药公司,致力于开发多功能生物疗法。近日,Zymeworks公司公布了一份摘要,重点介绍了zanidatamab一线治疗表达HER2的胃食管腺癌(GEA)患者的新临床数据,这是一款靶向HER2的双特异性抗体。
截至2021年3月18日的摘要亮点包括:30例患者接受了zanidatamab联合标准护理化疗(mFOLFOX6、或CAPOX、或FP)治疗,14例患者仍在进行治疗。22例HER2阳性可评估缓解的患者中,经确认的客观缓解率(cORR)为68.2%、疾病控制率(DCR)为90.9%。与治疗相关的不良事件通常与之前关于zanidatamab和/或化疗方案的报告一致,大多数报告的严重程度为1级或2级。
zanidatamab是一种双特异性抗体,基于Zymeworks公司Azymetric™平台开发,可以同时结合HER2的2个非重叠表位,称为双互补位结合(biparatopic binding)。这种独特的设计导致了多种作用机制,包括双重HER2信号阻断、细胞表面HER2蛋白结合和去除的增加,以及导致抗肿瘤活性增强的强效效应器功能。
目前,Zymeworks公司正在全球范围内进行多项1期、2期和关键临床试验,以开发zanidatamab,作为表达HER2的实体瘤患者的靶向治疗选择。
之前,美国FDA已授予zanidatamab突破性疗法认定(BTD),用于治疗既往治疗过的HER2基因扩增性胆管癌(BTC)患者。此外,FDA还授予了zanidatamab 2个快速通道资格(BTD),一个是单药治疗难治性BTC,另一个是联合标准护理化疗一线治疗胃食管腺癌(GEA)。这些资格认定,意味着zanidatamab有资格获得加速批准、优先审查和滚动审查,以及FDA关于有效药物开发计划的强化指导。
此外,美国FDA还授予了zanidatamab治疗胆管癌、胃癌和卵巢癌的孤儿药资格(ODD)。在欧盟,欧洲药品管理局(EMA)也授予了zanidatamab治疗胆管癌和胃癌的ODD。
值得一提的是,2018年11月,百济神州以高达4000万美元的首付款以及至多3.9亿美元的里程碑付款,获得了zanidatamab和另一款在研药物ZW49在亚洲(除日本外)、澳大利亚和新西兰的独家开发和商业化权利,其中ZW49是一款双特异性抗体偶联药物(ADC)。目前,zanidatamab在中国国内已被批准开展一线、二线治疗胆管癌的临床试验。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



