2025年2月Cell期刊精华
来源:生物谷原创 2025-02-28 11:33
2025年2月份即将结束,2月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:模拟低氧呼吸效果的药物HypoxyStat有望治疗一系列线粒体疾病
doi:10.1016/j.cell.2025.01.029
对于普通人来说,生活在氧气比海平面少的高海拔地区可以带来健康益处,比如降低心脏病发病率和提高耐力等等。但对于那些天生患有遗传性线粒体疾病的人来说,他们很少能活过童年,像山顶上的低氧空气可能他们而言是救命的,有可能延长他们的寿命并消除他们的症状。
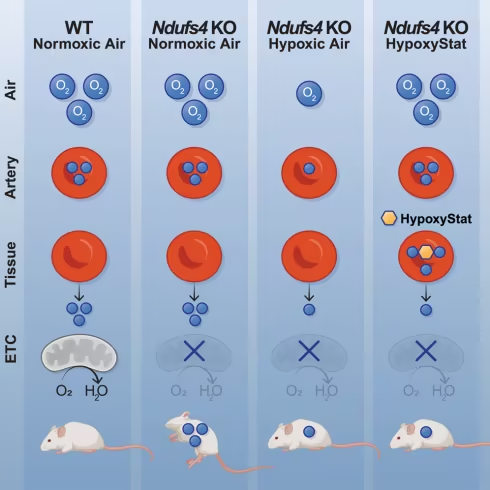
如今,在一项标题为“HypoxyStat, a small-molecule form of hypoxia therapy that increases oxygen-hemoglobin affinity”的研究中,格莱斯顿研究所的科学家们开发出一种模拟低氧呼吸效果的药物:HypoxyStat。在患有一种称为莱氏综合征(Leigh Syndrome)的最常见儿童线粒体疾病的小鼠模型中,即使在疾病的晚期给药,这种药物也能将它们的寿命延长三倍以上,并逆转脑损伤和肌肉无力。
HypoxyStat是一种重新利用的化合物,最初是为镰状细胞贫血的无关适应症而设计的。研究人员发现,这种药物使血红蛋白更紧密地结合氧气,并降低了输送到组织的氧气量。他们让患有莱氏综合征的小鼠在生命早期每天服用HypoxyStat。因此,这些小鼠不再出现脑部病变,不再表现出肌肉无力或协调性丧失,它们的寿命是原来的三倍多。值得注意的是,即使小鼠在长大后已出现了主要症状(包括广泛的脑损伤、行为受损和慢性低温)才开始服用这种药物,这种药物也产生类似的效果。它逆转了这些小鼠的大脑、肌肉和行为症状。
2.Cell:10年谜团终破解!新研究揭示乙肝病毒在肝细胞中建立感染机制,为彻底消除乙肝奠定良好基础
doi:10.1016/j.cell.2025.01.033
乙型肝炎(简称乙肝)是由乙型肝炎病毒(HBV)感染肝脏引发的疾病,它在全球范围内影响了近5%的人口。这种病毒不仅会对肝细胞造成长期损害,还是肝癌的主要诱因之一。根据世界卫生组织(WHO)的数据,全球有超过2.5亿人患有慢性HBV感染,而该病毒每年导致超过100万人死亡,使其成为仅次于艾滋病的全球第二大致命感染病。
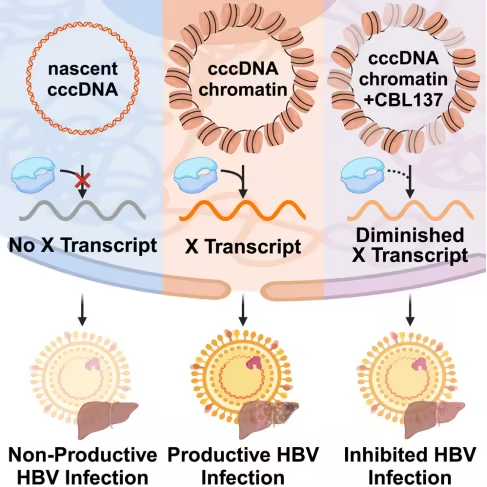
多年来,科学家们一直试图解开一个谜题:HBV是如何在肝细胞中建立感染的?如今,由纪念斯隆-凯特琳癌症中心(MSK)、威尔康奈尔医学院和洛克菲勒大学的研究团队领导的一项新研究取得了突破性进展。他们发现了一个HBV的潜在弱点,并利用一种名为CBL137的化合物成功阻断了HBV感染肝细胞的能力。这一成果为开发新的治疗方法奠定了基础,相关研究结果已于2025年2月20日发表在Cell期刊上,论文标题为“A nucleosome switch primes Hepatitis B Virus infection”。
该研究的核心是HBV的一个关键基因——X基因。这个基因编码一种名为X蛋白的物质,它对病毒在宿主细胞中建立感染和表达自身基因至关重要。然而,X基因本身也存在一个关键问题:它需要一种特殊的DNA-组蛋白复合物——核小体,来启动其功能。核小体通常被认为是基因表达的“刹车”,但在HBV感染中,它却起到了相反的作用。研究发现,核小体的存在对于HBV基因的转录和X蛋白的生成是必需的。这一发现打破了传统观念,即核小体总是抑制基因表达的假设。
基于这一发现,研究团队测试了多种已知会影响染色质结构的小分子化合物,最终发现CBL137能够有效阻断X蛋白的生成。这种化合物在极低浓度下就能发挥作用,且仅对HBV产生影响,而不伤害人体细胞。这表明CBL137具有高度的特异性,能够精准地攻击病毒而不损害宿主细胞。
doi:10.1016/j.cell.2025.01.018
在一项新的研究中,来自哥伦比亚大学的研究人员在小鼠大脑中发现了专门的神经元,这些神经元可命令这些动物停止进食。相关研究结果于2025年2月5日在线发表在Cell期刊上,论文标题为“Brainstem Neuropeptidergic Neurons Link a Neurohumoral Axis to Satiation”。
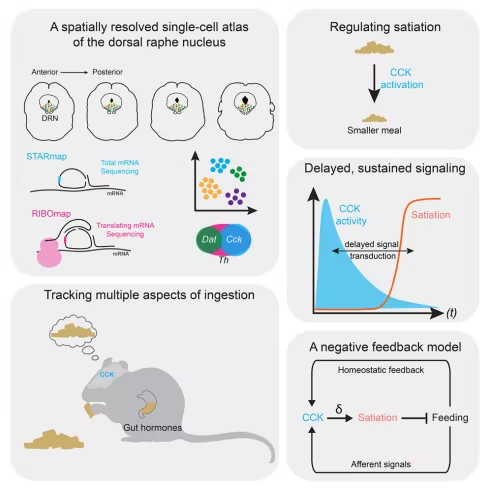
论文通讯作者、哥伦比亚大学瓦格洛斯内科外科学院内科医生Alexander Nectow说,“这些神经元不同于任何其他参与调节饱腹感的神经元。大脑中的其他神经元通常仅限于感知放入我们嘴里的食物,或食物如何填充肠道,或从食物中获得的营养。我们发现的神经元很特别,因为它们似乎整合了所有这些不同的信息等等。”
为了了解这些神经元是如何影响进食的,Nectow及其团队对它们进行了改造,使其可以由用光开启和关闭。
当这些神经元被光激活时,小鼠吃的食物要少得多。这种激活的强度决定了这些动物停止进食的速度。Chowdhury 说,“有趣的是,这些神经元不仅发出立即停止的信号;它们还帮助小鼠逐渐放慢进食速度。”
4.Cell:新研究揭示DNA错配修复基因在亨廷顿病中起着重要作用
doi:10.1016/j.cell.2025.01.031
在一项新的研究中,来自加州大学洛杉矶分校的研究人员在小鼠模型中发现,与修复错配DNA相关的基因在引发亨廷顿病(Huntington's disease, HD)中最脆弱的神经元损伤以及引发下游病理和运动损伤方面至关重要,这为疾病机制和开发治疗方法的潜在新方法提供了线索。
相关研究结果于2025年2月11日在线发表在Cell期刊上,论文标题为“Distinct mismatch-repair complex genes set neuronal CAG-repeat expansion rate to drive selective pathogenesis in HD mice”。
论文通讯作者、加州大学洛杉矶分校精神病学与生物行为科学卫生系教授X.William Yang博士说,“我们证实作为HD患者修饰因子的相同DNA错配修复基因只能在小鼠模型中最脆弱的神经元中驱动快节奏的疾病过程,导致一系列疾病表型。”
值得注意的是,缺乏一个错配修复基因子集的HD小鼠,尤其是Msh3和Pms1基因,校正了该小鼠模型中绝大多数的基因表达缺陷。此外,它们部分或完全阻止了整个大脑中的突变亨廷顿蛋白聚集体病理学特性。
除了分子和病理学益处外,这项研究还表明,靶向Msh3可以改善运动缺陷和步态缺陷,提高神经元突触蛋白水平,减少胶质细胞过度反应。
5.Cell:中德科学家联手揭示雄激素的新作用机制,有望开发出更好的肌肉增强药物
doi:10.1016/j.cell.2025.01.006
在一项新的研究中,来自莱比锡大学和山东大学的研究人员发现了一种对肌肉和骨骼功能至关重要的雄激素所使用的新机制。这一发现可能会导致开发副作用更少的新药物,用于加强不活动患者肌肉等应用。相关研究结果发表在Cell期刊上,论文标题为“Identification, structure, and agonist design of an androgen membrane receptor”。

雄激素是控制男性性特征发育的激素。最强大的雄激素是5α-二氢睾酮(5α-dihydrotestosterone, 5α-DHT)。除此之外,它对骨骼和肌肉功能以及青春期男性第二性征的发育至关重要。作为骨骼和肌肉形成的驱动因素,5α-DHT可以增加骨矿物质密度,促进骨骼肌生长,从而增强肌肉力量。
在这项研究中,这些作者能够证实一种称为GPR133的粘附G蛋白偶联受体被雄激素类固醇激素5α-DHT激活。
新型激动剂AP503激活GPR133可增加肌肉力量,而不会引发在服用雄激素时观察到的特定负面影响。例如,增加和延长对睾酮的暴露可以促进前列腺癌的产生,雄激素给药仅两周后小鼠前列腺的组织变化就证明了这一点。尚未观察到AP503会引发这种副作用。
此外,这项新的研究使用结构生物学方法来阐明5α-DHT、AP503和GPR133之间相互作用的分子基础。这将允许这种激动剂被专门优化并进一步开发成新的治疗药物。这可能会导致开发出副作用较低的新型肌肉增强药物。
doi:10.1016/j.cell.2025.01.025
在一项突破性的临床前研究中,来自威尔康奈尔医学院、纪念斯隆-凯特琳癌症中心和加州大学圣地亚哥分校的科学家们发现,癌症患者体内的血凝块(也称为血栓)形成并非像过去认为的那样源于其他器官,而是对来自肺部的信号作出的反应。这一发现颠覆了传统观念,揭示了血栓形成的新机制。
相关研究结果于2025年2月11日在线发表在Cell期刊上,论文标题为“Extracellular vesicles from the lung pro-thrombotic niche drive cancer-associated thrombosis and metastasis via integrin beta 2”。

论文第一作者Serena Lucotti博士分享了一个令人震惊的数据:“我们回顾了尸检研究,发现高达60%的癌症患者死于血栓,而非癌症本身。这非常令人遗憾,因为我们有预防血栓的药物,但它们可能导致出血风险,所以我们不能随意给所有患者使用。更糟糕的是,我们目前无法准确预测哪些患者会从这些药物中受益。”
为了进一步探索这一现象,研究团队在小鼠和人体组织中进行了实验。他们发现,不同类型的肿瘤会释放不同量的趋化因子CXCL13。例如,乳腺癌和黑色素瘤释放的CXCL13较少,但如果这些肿瘤扩散到肺部,它们会“就地取材”,通过局部影响肺部的巨噬细胞来触发血栓形成。相比之下,胰腺癌则像“CXCL13工厂”,将大量CXCL13分泌到血液中,远程激活肺部的巨噬细胞,无需靠近肺部即可引发血栓。
更有趣的是,研究团队还发现了一种潜在的“解药”。他们开发了一种抗体,可以阻断巨噬细胞释放的小囊泡与血小板的结合。接受这种抗体治疗的小鼠不仅血栓减少,癌症转移也显著降低。Lucotti博士兴奋地表示:“这非常重要,因为目前针对转移性癌症的治疗手段非常有限。我们正在开发一种人类抗体,希望能为患者带来新的希望。”
此外,研究团队还发现,整合素β2(一种粘附分子)可能成为预测血栓风险的生物标志物。通过分析癌症患者的血液样本,他们能够根据整合素β2的水平准确区分血栓风险的高低。这一发现为未来的个性化治疗提供了重要线索。
7.Cell:科学家在肺癌中发现一种能促进癌细胞代谢的特殊酶类,有望帮助开发新型个体化疗法
doi:10.1016/j.cell.2025.01.024
肺癌是一种尤其具有挑战性的癌症类型,其经常在没有任何警告的情况下出人意料地猛烈发作,同时也会以一种不可预测的方式来逃避疗法的攻击。尽管科学家们已经深入揭示了肺癌发生的基本生物学机制,但这种疾病的一些分子机制仍然令人难以捉摸。
近日,一篇发表在国际杂志Cell上题为“GUK1 activation is a metabolic liability in lung cancer”的研究报告中,来自哈佛医学院等机构的科学家们通过研究在理解一些肺癌的基因缺陷如何改变癌细胞代谢从而加剧疾病进展上取得了重要研究成果。
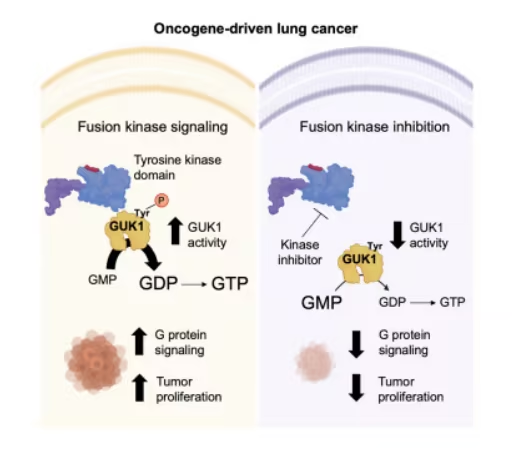
通过对小鼠模型和人类癌细胞进行研究,研究人员在携带ALK基因改变的肺癌中发现了一种名为GUK1的特殊代谢酶,实验结果表明,GUK1在促进肿瘤细胞代谢并帮其生长方面扮演着关键角色。相关研究结果为揭示肺癌代谢机制提供了更为清晰的图谱,研究者表示,这项研究为开发靶向作用GUK1从而遏制癌症生长的新型疗法奠定了一定的基础,研究者Jaime Schneider表示,他们经常治疗肺癌患者,而且经常目睹这种疾病的侵袭性和持久性。他们在诊所看到的很大一部分患者在接受当前可用疗法的一段时间内表现很好,但最终疾病还是会复发。
肺癌是美国乃至全球范围内癌症相关死亡的主要原因,而且不吸烟人群和轻度吸烟人群肺癌病例目前正在增加,其背后的原因研究人员并不清楚。研究者Schneider治疗的病人中很多人都为这项研究捐献了肿瘤样本,这就能鼓励研究人员更深入地理解肺癌发生的分子机制,如今研究人员需要跳出思维定式更好地理解肺癌的疾病生物学特性并识别出新型疗法靶点。
doi:10.1016/j.cell.2024.12.034
在一项新的研究中,来自科克大学等研究机构的研究人员发现,受非工业化社会饮食习惯启发而新开发的饮食可以显著降低多种慢性疾病的风险,并计划与公众分享食谱。相关研究结果近期发表在Cell期刊上,论文标题为“Cardiometabolic benefits of a non-industrialized-type diet are linked to gut microbiome modulation”。
在这篇论文中,在一项人类干预实验中,一种模拟非工业化社区饮食习惯的新开发饮食导致了代谢和免疫的显著改善。在短短三周内,这一饮食促进减肥、坏胆固醇降低17%、血糖降低6%和C反应蛋白(炎症和心脏病的标志物)减少14%。
这些改善与参与者肠道微生物组的有益变化有关,其中肠道微生物组是数万亿细菌的家园,这些细菌在人类的健康中起着至关重要的作用,影响消化、免疫和新陈代谢。
这项研究表明,这种名为“NiMe(Non-industrialized Microbiome Restore, 非工业化微生物组恢复)”的新饮食增强了罗伊氏乳杆菌在肠道中的短期持久性。
NiMe饮食具有非工业化饮食的关键特征:(1)以植物为主,但不是素食主义者:主要由蔬菜、豆类和其他全植物性食物组成,以及每天一小份动物蛋白(鲑鱼、鸡肉或猪肉);(2)没有乳制品、牛肉或小麦:被排除在外只是因为它们不是巴布亚新几内亚农村人消费的传统食物的一部分;(3)含糖量和饱和脂肪含量高的加工食品所在比例很低;(4)富含纤维,纤维含量为每1000卡路里22克,超过了目前的饮食建议。
doi:10.1016/j.cell.2024.11.029
在一项新的研究中,霍华德-休斯医学研究所珍妮莉亚研究园高级小组组长Lippincott Schwartz及其团队发现一个类似于负责传播使肌肉收缩的分子信号的亚细胞结构网络也负责在大脑中传播可能有助于学习和记忆的信号。相关研究结果近期发表在Cell期刊上,论文标题为“Periodic ER-plasma membrane junctions support long-range Ca2+ signal integration in dendrites”。
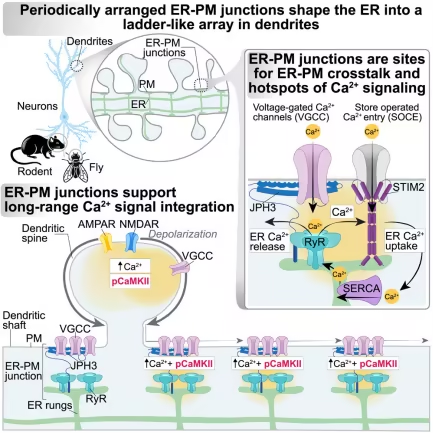
Lippincott-Schwartz团队首先研究了身体中唯一已知具有类似梯形的内质网结构的其他区域:肌肉组织。在肌肉细胞中,内质网和质膜(细胞的外膜)在周期性的接触部位相遇,这种排列由一种称为亲联蛋白(junctophilin)分子控制。
通过高分辨率成像,该团队发现树突还含有一种控制内质网和质膜之间接触位点的亲联蛋白。此外,他们发现,控制肌肉细胞接触部位钙释放的相同分子机制也存在于树突接触位点,其中在肌肉细胞接触位点,释放的钙驱动肌肉收缩,而在树突接触位点,释放的钙调节神经元信号传导。
由于这些线索,该团队有一种预感,这种存在于树突接触位点的分子机制对于传递细胞用于交流的钙信号也一定很重要。他们猜测树突上的接触位点可能就像电报机上的中继器:接收、放大和远距离传播信号。在神经元中,这可能解释树突特定位点接收到的信号是如何传递到数百微米外的细胞体(cell body)的。
10.Cell:我国科学家揭示成年哺乳动物大脑中内源性NMDA受体的组装和结构
doi:10.1016/j.cell.2025.01.004
在一项新的研究中,由中国科学院脑科学与智能技术卓越创新中心研究员竺淑佳(Zhu Shujia)和中国科学院上海药物研究所研究员李扬(Li Yang)博士领导的一个研究小组剖析了成年哺乳动物大脑皮层和海马体中内源性N-甲基-D-天冬氨酸受体(endogenous N-methyl-D-aspartate receptor, eNMDAR)的组装和结构。相关研究结果近期发表在Cell期刊上,论文标题为“Assembly and architecture of endogenous NMDA receptors in adult cerebral cortex and hippocampus”。
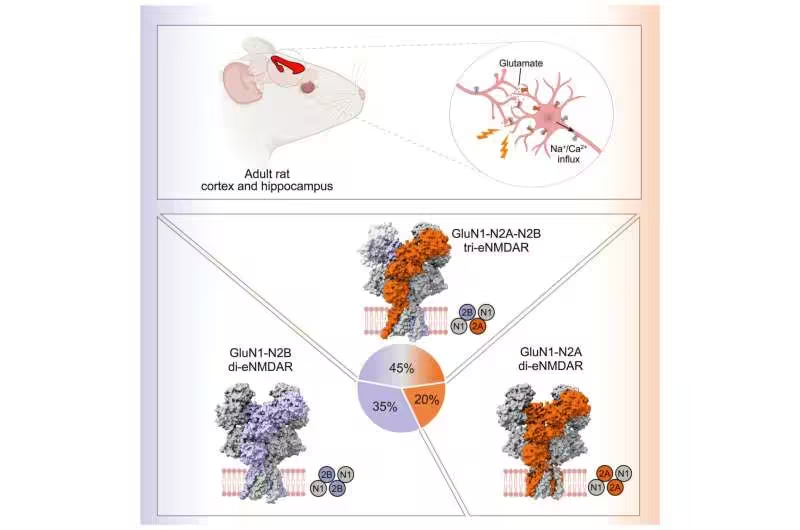
在这项研究中,这些作者首先使用用亲和标签标记的高亲和力抗体从成年野生型大鼠的大脑组织中富集eNMDAR。在低温电镜数据处理过程中,他们利用一种基于卷积网络的模型将eNMDAR从异质的内源性蛋白池中分离出来。通过结合生化和算法纯化技术,他们最终以接近原子分辨率解析了介导大脑生理突触可塑性的天然eNMDAR。
他们确定了三种主要的eNMDAR亚型:GluN1-N2A-N2B三异源聚体、GluN1-N2B和GluN1-N2A二异源聚体,它们分别占皮层和海马体NMDA受体的45%、35%和20%。
GluN1-N2A-N2B三异源四聚体突出了GluN2A和GluN2B亚基在体内的功能整合。它的结构显示出独特的组装和不对称的架构。
在GluN1-N2A-N2B三异源聚体和GluN1-N2B二异源聚体之间的GluN2B亚基中发现了构象变化。不同受体亚型GluN2B亚基的这些结构差异为eNMDAR的功能多样性提供了见解。
这些发现揭示了eNMDAR精确调节成年哺乳动物体内兴奋性突触传递和突触可塑性的分子基础。值得注意的是,eNMDAR的亚基组成在不同的发育阶段和大脑区域发生了变化。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


