Cell重磅!AI赋能常规病理切片,成功解锁1.4万例肿瘤微环境的隐藏密码
来源:生物谷原创 2026-01-02 09:19
GigaTIME多模态AI框架可从常规苏木精-伊红切片生成虚拟多光谱免疫荧光图像,构建涵盖24种癌症的大规模患者队列,揭示1234个蛋白-生物标志物关联,为肿瘤免疫微环境研究与精准治疗提供全新路径。
在医院病理科,苏木精-伊红染色切片是每个癌症患者的“基础档案”。这张看似普通的切片,不仅记录着组织形态,更藏着肿瘤免疫微环境的关键信息。可惜长期以来,这些信息难以被充分挖掘。肿瘤免疫微环境直接影响癌症进展和免疫治疗效果,而能精准解析这一复杂环境的多光谱免疫荧光技术,却因成本高昂、流程繁琐导致数据极度稀缺,让大规模临床研究屡屡受限。
近日,Cell发表的一项突破性研究成功让这些常规切片“说话”,为突破这一研究瓶颈带来了革命性解决方案。
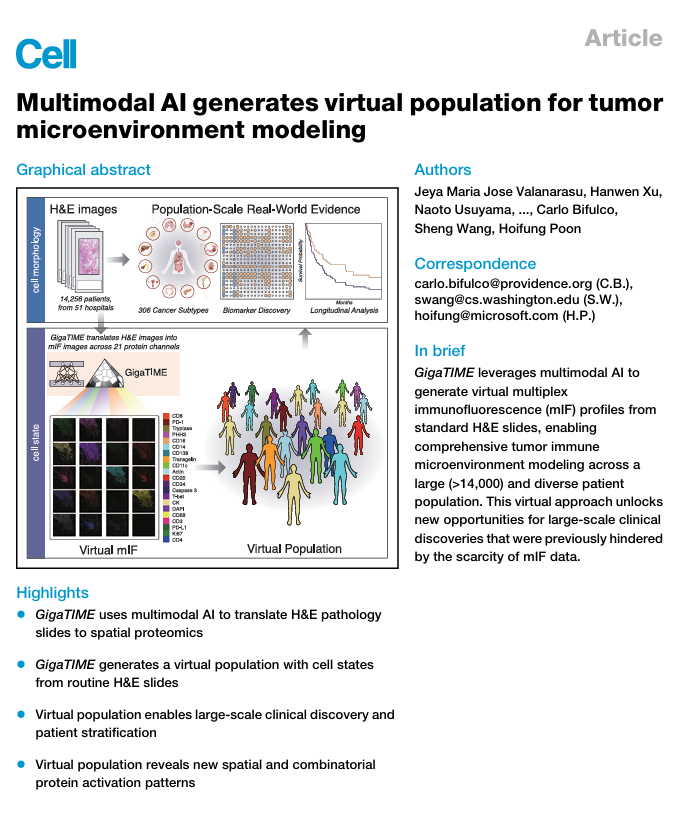
GigaTIME多模态AI框架的核心,是通过AI捕捉苏木精-伊红图像与多光谱免疫荧光图像的内在关联,直接从常规切片生成虚拟多光谱免疫荧光图像。研究团队以4000万个细胞的配对数据为训练基础,覆盖21种关键肿瘤免疫微环境蛋白,包括免疫检查点分子PD-1、PD-L1,免疫细胞标志物CD3、CD8、CD20等,采用NestedUNet架构构建模型。该模型应用于美国普罗维登斯健康系统51家医院、1000余家诊所的14256名患者数据,成功生成299376张虚拟多光谱免疫荧光切片,涵盖24种癌症类型和306种亚型,构建出目前规模最大、多样性最丰富的虚拟多光谱免疫荧光患者队列。
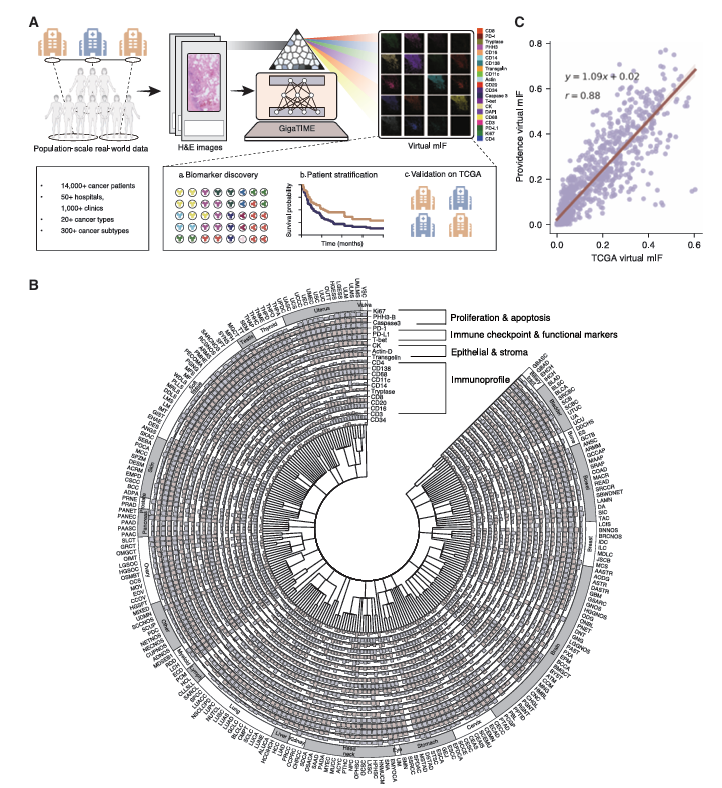
图1:GigaTIME支持大规模肿瘤免疫微环境分析
在性能验证中,GigaTIME展现出优异的跨模态转化能力。在像素、细胞和切片三个层面,其转化效果均显著优于传统图像翻译模型CycleGAN。核标志物DAPI的Dice相似度达到0.72,远高于平均激活基线的0.12;细胞水平的Pearson相关系数达0.59,而CycleGAN仅为0.03;切片水平的Spearman相关系数最高可达0.98,充分证明虚拟多光谱免疫荧光与真实多光谱免疫荧光的高度一致性。更值得关注的是,该模型在未经过训练的乳腺癌、脑癌组织中仍保持稳定性能,展现出强大的泛化能力。
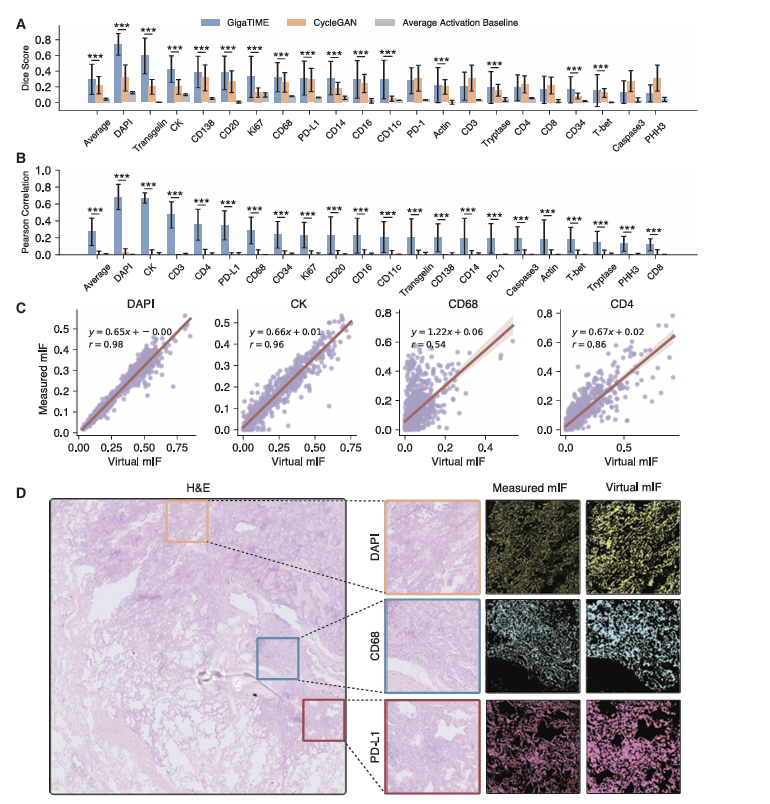
图2:GigaTIME实现从苏木精-伊红到多光谱免疫荧光图像的转化
基于这一虚拟队列,研究团队开展了大规模临床发现,共鉴定出1234个具有统计学意义的蛋白-生物标志物关联,覆盖泛癌、癌种和亚型三个层面。泛癌水平上,高肿瘤突变负荷和微卫星不稳定性高与CD138、CD20等免疫标志物的激活显著相关,KMT2D突变与免疫浸润增强相关,而KRAS突变则表现出免疫排斥表型。临床常用的PD-L1生物标志物与虚拟PD-L1通道激活高度一致,同时研究还发现其与增殖标志物Ki-67呈负相关。癌种特异性层面,脑癌中T-bet与TP53突变、肠癌中转移状态与PD-L1激活的独特关联,均为首次在大规模队列中得到证实。
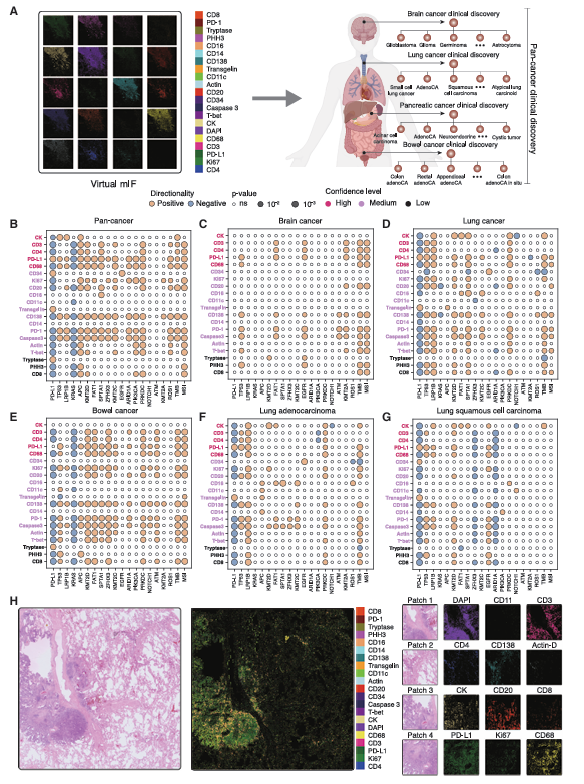
图3:GigaTIME在泛癌、癌种及亚型水平鉴定新型肿瘤免疫微环境蛋白与生物标志物关联
该虚拟队列还为患者分层提供了有力工具。GigaTIME整合21种蛋白的虚拟激活信号形成复合特征,在泛癌和肺癌、脑癌等特定癌种中,能有效将患者分为不同生存风险组,预测效果优于单一蛋白标志物。例如在肺癌中,复合特征的生存分层log-rank p值达2.8e-07,显著优于CD3、CD8等单个免疫标志物。
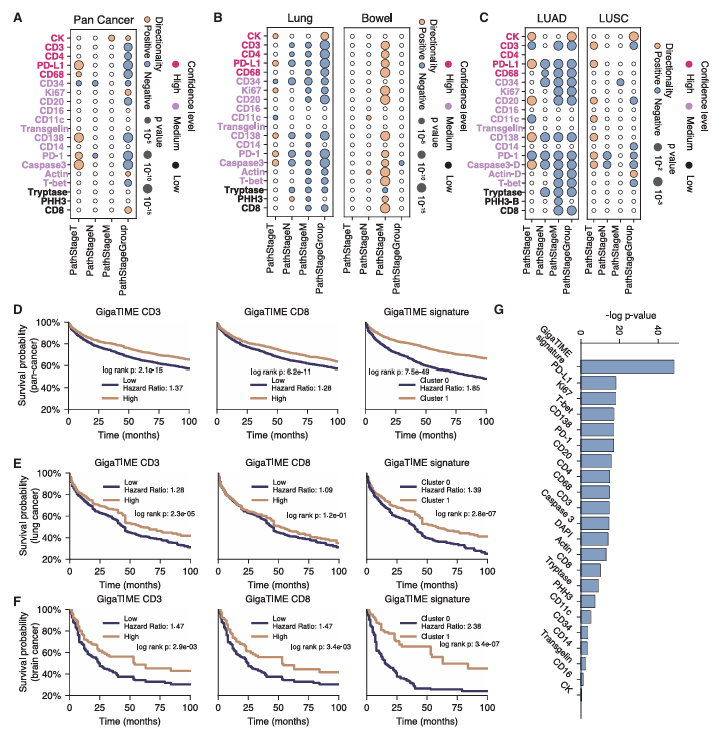
图4:GigaTIME支持病理分期和生存组的有效患者分层
为验证结果可靠性,研究团队将GigaTIME应用于癌症基因组图谱(TCGA)的10200个肿瘤样本,生成独立虚拟队列。两个队列的虚拟蛋白激活信号Spearman相关系数达0.88,且有80个蛋白-生物标志物关联在两组中均显著富集,充分证明GigaTIME结果的稳健性。同时,普罗维登斯队列还发现了33%更多的显著关联,凸显了真实世界大样本数据的临床价值。
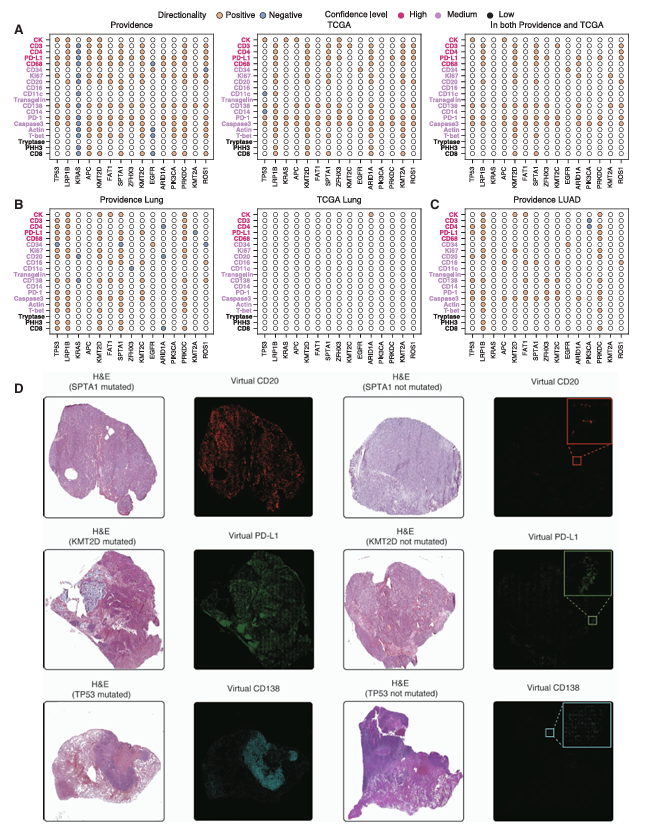
图5:基于TCGA虚拟队列的独立验证
此外,GigaTIME还解锁了新的分析维度。通过熵、信噪比、清晰度等空间指标分析,研究发现这些指标捕捉蛋白-生物标志物关联的能力优于传统激活密度指标。而CD138与CD68、PD-L1与caspase 3等蛋白组合分析,揭示了抗体介导的肿瘤杀伤、免疫逃逸与细胞凋亡互作等新型生物学机制,为药物靶点开发提供了新思路。
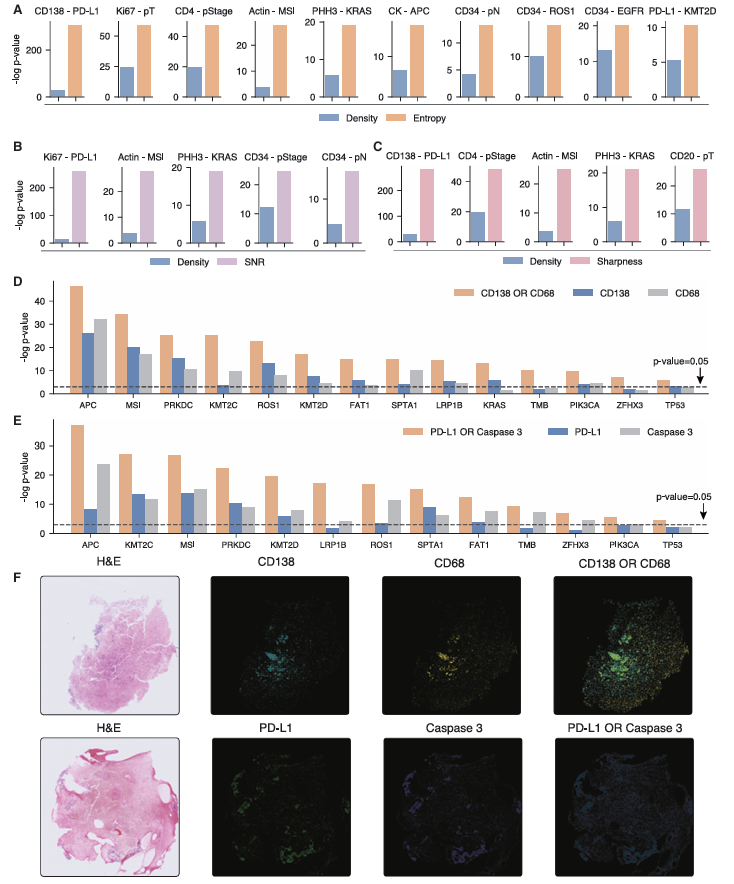
图6:GigaTIME揭示有趣的虚拟多光谱免疫荧光空间和组合模式
作为一项突破性技术革新,GigaTIME成功打破多光谱免疫荧光数据稀缺的限制,将海量常规苏木精-伊红切片转化为富含肿瘤免疫微环境信息的宝贵资源。它不仅实现了大规模、多维度的肿瘤免疫微环境分析,更为临床生物标志物发现、患者分层和精准免疫治疗提供了高效工具。随着模型的公开和推广,未来有望纳入更多癌种、更多蛋白标志物,构建更全面的肿瘤免疫微环境图谱,推动肿瘤精准医疗进入大数据驱动的全新阶段,让更多常规病理资料发挥更大临床价值,惠及广大癌症患者。(生物谷Bioon.com)
参考文献:
Valanarasu JMJ, Xu H, Usuyama N, et al. Multimodal AI generates virtual population for tumor microenvironment modeling. Cell. Published online December 9, 2025. doi:10.1016/j.cell.2025.11.016
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


