Nature子刊:马骏/刘卓炜/梁晓雨/孙万阳团队揭示肿瘤再生细胞耐受铁死亡的机制
来源:生物世界 2024-05-10 13:39
研究者通过细胞死亡检测和铁死亡相关氧化磷脂检测发现,相较于普通肿瘤细胞,肿瘤再生细胞可通过降低铁死亡敏感性来抵抗放放疗。
近年来的研究发现,肿瘤细胞对铁死亡耐受是肿瘤发生治疗抵抗的重要途径之一。铁死亡是一种铁依赖的、以膜磷脂多不饱和脂肪酸链过氧化为核心的细胞死亡方式。然而,肿瘤干细胞是否通过耐受铁死亡来介导放疗抵抗尚不清楚。
既往研究表明,在SH-SY5Y神经母细胞瘤分化模型中,具有更高干性的前体细胞比分化的子代细胞更耐受铁死亡。同样地,与心肌细胞相比,心肌细胞前体的铁死亡敏感性也更低。然而,高表达CD44或发生上皮-间充质转化(EMT)的肿瘤细胞更容易发生铁死亡。因此,进一步明确肿瘤干细胞对铁死亡的敏感性,找到诱导肿瘤干细胞铁死亡的方式,可能是解除肿瘤治疗抵抗的重要突破口。
2024年5月8日,中山大学肿瘤防治中心马骏院士课题组、刘卓炜教授课题组与暨南大学药学院何蓉蓉教授课题组孙万阳副研究员等合作,在 Nature Chemical Biology 期刊在线发表了题为:Tumor-repopulating cells evade ferroptosis via PCK2-dependent phospholipid remodeling 的研究论文。
该研究揭示了肿瘤再生细胞通过重塑膜磷脂耐受铁死亡进而抵抗肿瘤放化疗的机制,揭示了线粒体及线粒体代谢酶PCK2在调控肿瘤细胞ACSL4相关磷脂重塑中的关键作用。

该研究首先通过3D纤维软胶培养模型筛选和富集了具有干性特征的肿瘤再生细胞。研究者通过细胞死亡检测和铁死亡相关氧化磷脂检测发现,相较于普通肿瘤细胞,肿瘤再生细胞可通过降低铁死亡敏感性来抵抗放放疗。
研究团队进一步探究肿瘤再生细胞耐受铁死亡的机制。通过筛选调控铁死亡敏感性的关键分子,他们发现ACSL4介导的磷脂重塑是肿瘤再生细胞耐受铁死亡的关键。通过磷酸化质谱、体外酶活检测、脂质组学分析、氧化磷脂组学分析和分子动力学模拟,研究证实了ACSL4 T679位点磷酸化对ACSL4酶活性及细胞内磷脂重塑非常关键。
接下来,研究团队探究介导ACSL4 T679磷酸化及酶活增强的关键激酶。通过定量蛋白质谱、免疫荧光、细胞组分分离、免疫电镜、免疫共沉淀、体外激酶实验和脂质组学分析,他们明确了线粒体代谢激酶PCK2可磷酸化并激活ACSL4,以驱动铁死亡相关的磷脂重塑。此外,通过siRNA筛选、RNA-seq检测、泛素实验等方法鉴定出转录因子STAT3可通过转录E3泛素连接酶HERC6在调节肿瘤再生细胞中PCK2的下调中发挥关键作用。
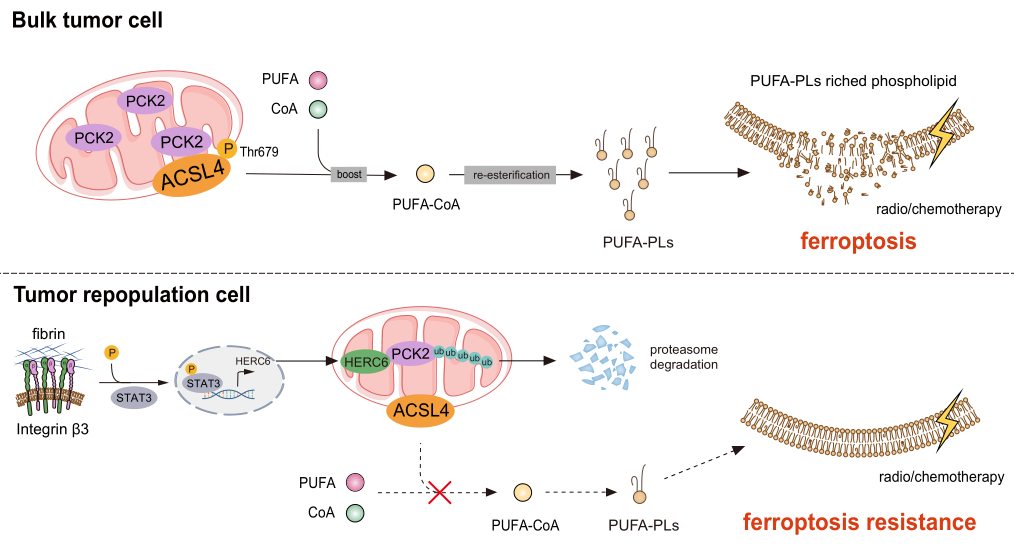
定位于线粒体的代谢酶PCK2可磷酸化ACSL4并促进肿瘤细胞发生ACSL4相关磷脂重塑。肿瘤再生细胞通过促进PCK2泛素化降解使膜磷脂处于铁死亡耐受状态。
中山大学肿瘤防治中心刘卓炜教授、梁晓雨副研究员、马骏院士及暨南大学药学院孙万阳副研究员为论文共同通讯作者。中山大学肿瘤防治中心博士生李哲、徐智敏、陈伟鹏及主任医师杜晓京为论文共同第一作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


