Cell:重大进展!新研究揭示重复150次以上的CAG重复扩增驱动亨廷顿病产生的新机制
来源:生物谷原创 2025-01-20 10:22
这项新的研究表明这种遗传性的基因突变本身不会伤害脑细胞。相反,这种突变在几十年内是无害的,但会慢慢变成一种剧毒的形式,然后迅速杀死脑细胞。
在一项新的研究中,来自布罗德研究所、哈佛医学院和麦克莱恩医院的研究人员发现了已知导致亨廷顿病(Huntington's disease)的遗传性基因突变导致脑细胞死亡的机制。这一发现改变了人们对这种致命的神经退行性疾病的理解,并提出了延缓甚至预防它的潜在方法。
相关研究结果于2025年1月16日在线发表在Cell期刊上,论文标题为“Long somatic DNA-repeat expansion drives neurodegeneration in Huntington’s disease”。

30年来,科学家们已经知道亨廷顿病是由亨廷顿蛋白(HTT)基因突变引起的,但他们不知道这种突变是如何导致脑细胞死亡的。
这项新的研究表明这种遗传性的基因突变本身不会伤害脑细胞。相反,这种突变在几十年内是无害的,但会慢慢变成一种剧毒的形式,然后迅速杀死脑细胞。
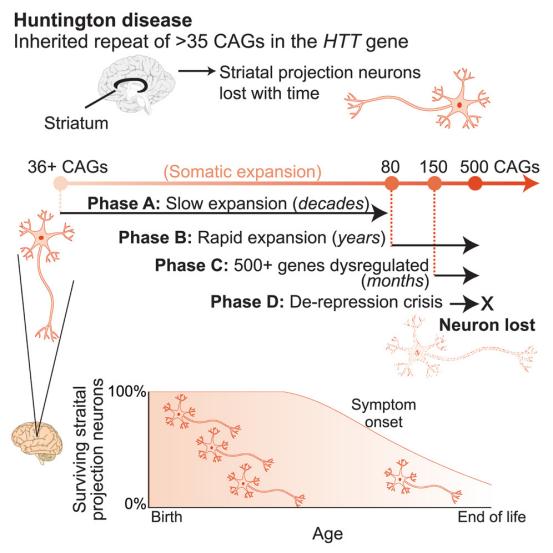
这种基因突变涉及HTT基因中的一段DNA序列,在这段序列中,长三个碱基的DNA序列“CAG”重复至少40次,而不是没有这种疾病的人遗传的15-35次重复。这些作者发现,具有40个或更多CAG重复的DNA片段会生长到数百个重复的长度。
这种类型的“体细胞扩增(somatic expansion)”只发生在后来死于亨廷顿病的特定类型的脑细胞中。只有当脑细胞的DNA扩增达到CAG重复的阈值数量——大约150个时,脑细胞才会生病然后死亡。许多此类细胞的累计死亡会导致亨廷顿病的症状。
这项研究为为什么旨在降低HTT蛋白表达的候选亨廷顿病药物在临床试验中表现不佳提供了一个潜在的解释:在任何给定时间,只有少量脑细胞具有这种蛋白的毒性版本,因此这些治疗方法可能对大多数脑细胞没有治疗效果。
这项研究还提升了一种不同的治疗策略:停止或减缓HTT基因中CAG重复扩增可能会推迟大量脑细胞的毒性,从而延缓甚至预防这种疾病的发生。
论文共同通讯作者Steve McCarroll说,“这些实验改变了我们对亨廷顿病如何发展的看法。这是一种非常不同的思考突变如何导致疾病的方式,我们认为它将适用于亨廷顿病以外的DNA重复序列疾病。”
论文共同通讯作者Sabina Berretta说,“我们研究工作的重点是减轻疾病造成的痛苦。这项研究及其开展的工作可能会产生影响,并在短期内对缓解痛苦产生重大影响。”
未解决的问题
亨廷顿病会杀死一个名为纹状体投射神经元(striatal projection neuron)的细胞群体,这些细胞位于纹状体中,即大脑深处负责运动、许多认知功能和动机的结构。
当大量这些细胞死亡时,患者的手臂、腿部和面部会出现不自主的运动,许多患者还会出现认知问题。这些症状通常始于中年,然后在10到20年内发展为更严重的认知问题和移动或吞咽困难。
1993年,科学家们发现这种疾病是由HTT基因中CAG的扩增引起的。大多数人继承了具有15至35个连续CAG的基因版本,从未患上亨廷顿病,但那些继承了具有40个或更多连续CAG版本的人几乎总是在以后的生活中患上这种疾病。
CAG重复的次数越多,一个人在症状首次出现时往往越年轻。CAG重复序列的覆盖范围也被证明会随着时间的推移而扩大,导致不同组织中的长度不同。
但是,潜在的生物学问题一直悬而未决:这种HTT突变是如何有毒的?为什么HTT蛋白——几乎存在于身体的每个细胞中——只会杀死一些脑细胞,而不会杀死其他脑细胞?为什么天生携带这种突变并终生表达这种蛋白的患者,在几十年的明显健康状况良好后,只有在中年才会出现症状?
CAG重复扩增
为了回答这些问题,这些作者建立在McCarroll 实验室十年前开发的一种名为液滴单细胞RNA测序(droplet single-cell RNA-sequencing, Drop-seq)的技术之上,该技术使得人们能够分析数千个单细胞中的基因表达。
为了了解CAG重复长度的直接生物学效应,他们调整了单细胞RNA测序,以帮助他们不仅确定基因表达和单细胞的身份,还确定每个细胞内DNA重复片段的长度。
论文共同第一作者Seva Kashin说,“众所周知,这些CAG重复在神经元中会扩增。但是,获取特定细胞并测量CAG长度和转录谱的能力——这是一个非常重要的基础,可以进行非常强大的分析。”
这些作者研究了53名亨廷顿病患者和50名未患上这种疾病的人捐赠的脑组织,这些组织由HBTRC收集和保存。他们分析了50多万个细胞,发现患有这种疾病的人的大多数脑细胞类型具有与他们遗传的基本相同的CAG重复。但是一类称为纹状体投射神经元的脑细胞——在这种疾病中死亡的主要纹状体细胞——极大地扩增了它们的CAG重复片段。
之前对人类大脑组织的大多数研究都集中在少于100次重复的CAG重复片段,但是这项新的研究表明一些神经元有多达800个CAG,证实了格拉斯哥大学Peggy Shelbourne在20年前取得的发现。
最令人惊讶的是,这些作者发现,这种DNA重复片段从40个CAG扩展到150个CAG对神经元的健康没有明显影响。但重复次数超过150个CAG的神经元表现出严重的基因表达扭曲,失去关键基因的表达,然后死亡。
McCarroll团队还使用实验数据的计算机建模来估计纹状体投射神经元中CAG重复扩增的速率和时间。他们发现CAG重复片段最初生长缓慢,在生命的前二十年里每年不到一次。但是,当神经元的CAG重复片段道达到大约80个时——通常在几十年后——它的扩增速度会急剧加快,在短短几年内就会扩增到150个CAG。
此时,神经元在几个月后死亡。这意味着它的95%以上的生命都与无害的HTT基因有关。此外,由于不同细胞中的CAG重复序列在不同时间跨越这一毒性阈值,这些细胞作为一个群体,在很长一段时间内缓慢消失,从症状出现前约20年开始,随着症状的出现而更快消失。
论文共同第一作者Robert E. Handsaker说,“在我们开始这项研究之前,人们对亨廷顿病了解很多,但我们的集体理解存在差距和不一致。我们能够拼凑出几十年来在单个神经元中展开的病理学的完整轨迹,这为我们提供了可能进行治疗干预的许多不同时间点。”
Berretta说,“分析亨廷顿病患者的大脑组织对这项研究至关重要。我们感谢那些选择做一些非常困难的事情的家庭。如果没有许多大脑捐献者的利他主义,这是不可能的,他们留下了将持续下去并使许多其他人受益的知识遗产。”
治疗可能性
McCarroll团队建议,与其靶向HTT蛋白,一种补充或可能更好的治疗方法可能是减缓或阻止CAG重复扩增,这可能有助于延缓甚至预防这种疾病。
之前对亨廷顿病的遗传研究已提示着减缓这种扩增的潜在方法。这些研究表明,参与维持和修复DNA的细胞蛋白有时会破坏DNA重复片段的稳定性。例如,MSH3蛋白通常有助于细胞监测其DNA中的潜在突变,但由额外CAG形成的DNA中的环状结构会迷惑这种蛋白,从而扩大CAG重复。
一个国际人类遗传学家团队已发现,编码这些DNA修复蛋白的基因中的常见遗传变异可以加速或延迟亨廷顿病患者症状的发作——McCarroll 说,这一发现直接启发了他的团队专注于开发测量单个细胞中CAG重复的方法。
他补充说,用分子疗法减缓某些DNA维持过程可能会通过允许其他不易出错的DNA修复机制来解决DNA中的这些环状结构,从而减缓DNA重复扩增。
与此同时,这些作者正在努力了解超过150个CAG的DNA重复片段如何导致神经元损伤和死亡,以及为什么某些类型的神经元中的CAG重复片段比其他类型的神经元扩增得更多。他们还使用单细胞RNA测序与DNA重复谱的类似组合来了解DNA重复扩增与其他涉及DNA重复的细胞变化和患者疾病较晚发作之间的联系。
50多种人类脑部疾病,包括脆性X综合征和强直性肌营养不良,是由多个基因中DNA重复序列的扩增引起的。
McCarroll 说,“要找到减缓DNA重复扩增的治疗方法,需要许多人进行大量的科学研究。但我们希望,将这理解为一个由疾病驱动的核心过程,可以带来深入的关注和新的选择。”(生物谷 Bioon.com)
参考资料:
Robert E. Handsaker et al. Long somatic DNA-repeat expansion drives neurodegeneration in Huntington disease. Cell , 2025, doi:10.1016/j.cell.2024.11.038.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


