Nat Mater:新研究发现肿瘤细胞黏度指导癌症扩散的关键步骤
来源:生物谷原创 2026-02-17 14:13
研究证明,帮助肿瘤细胞离开血流的机械特征可能与支持其在远处部位后续生长的特征相冲突,这说明在转移过程中可能需要进行机械适应性调整
每年全球有数百万人被诊断出患有癌症。在晚期肿瘤疾病中,癌细胞会从原发肿瘤上脱落,并在身体其他部位定居形成转移灶。在其过程中,它们必须通过人体自身的运输系统(如血液或淋巴血管系统)进行扩散,并克服众多的机械障碍。

一个多学科研究团队调查了在血管中循环的肿瘤细胞的机械特性如何影响其转移路径。最近发表在《自然-材料》上的研究结果,为理解转移提供了重要的基础构件。
肿瘤细胞离开原始组织并定居在身体远处器官的过程被称为原发肿瘤的转移。由于在大多数情况下,导致癌症相关死亡的并非原发肿瘤而是转移灶,因此从根本上理解肿瘤细胞如何克服人体自身的屏障对于成功的癌症治疗至关重要。
肿瘤细胞如何克服障碍
为了形成转移灶,肿瘤细胞必须从原发肿瘤脱离、进入血流、通过循环系统移动、滞留在小血管中、穿出血管(外渗),最后在新的组织中定植。尽管已知机械特性会影响转移的成功率,但其背后的基本机制仍不清楚。
一个由生物学和转移专家以及物理学家组成的合作研究团队,涉及马克斯·普朗克物理与医学中心以及斯特拉斯堡生物医学研究中心,分析了肿瘤细胞在转移途中面临的物理约束,并研究了它们的力学行为如何影响其在转移过程中的进展。
由 Jacky G. Goetz 教授、Jochen Guck 教授和 Salvatore Girardo 博士领导的科学家们,将循环肿瘤细胞视为具有一定大小和可变形性的物体。它们在循环系统中移动并侵袭周围组织时会受到力的作用。
该团队关注细胞对这些力作出弹性或粘性响应的能力。细胞是粘弹性的,这意味着它们既具有粘性又具有弹性。当你缓慢推压它们时,它们表现得像液体,逐渐流动或变形(粘性行为)。当你快速推压它们时,它们表现得像弹簧,一旦移除外力就会弹回原状(弹性行为)。科学家们将生物学模型与量身定制的生物物理学工具相结合来探测细胞行为。
这种结合首次使他们能够直接研究弹性和粘性行为如何影响转移过程中肿瘤细胞的循环、滞留和穿出血管。他们开发了两种生物物理学工具:模拟细胞弹性行为的微水凝胶珠,以及经过改造以表现出特定粘弹性特征的工程化细胞。
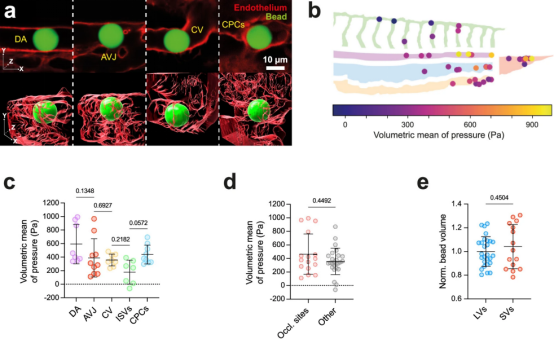
这些系统与两种动物模型(斑马鱼和小鼠)的活体成像技术相结合,使团队能够在循环系统中追踪它们的行为。研究人员证明,粘度而非弹性,决定了循环物体是否进入小血管、在何处停滞以及它们如何外渗并侵袭周围组织。
此外,他们表明粘度是通过内皮重塑实现有效外渗所必需的。同时,他们发现支持外渗的机械特性并不一定支持后续的转移性生长。
对癌症治疗策略的意义
"我们的工作确定了细胞粘度是控制血管内转移过程多个步骤的关键机械参数," MPZPM 片上实验室核心设施的负责人 Girardo 说。
"我们证明,帮助肿瘤细胞离开血流的机械特征可能与支持其在远处部位后续生长的特征相冲突。这表明在转移过程中可能需要进行机械适应性调整," Goetz 补充道,他与 MPL 前主任兼细胞物理学部门负责人 Jochen Guck† 共同制定了这项研究方案。
理解并可能控制细胞粘度等参数,可能为通过力学手段应对癌症提供新的途径。"这项工作深深植根于 Guck 的愿景," Girardo 和 Goetz 表示。"他坚信应从新的物理学角度应对医学挑战,并将其与生物学理解相结合,以实现对疾病更全面的认识。这种思维方式持续激励着我们,因为它为真正新颖的诊断和治疗方法打开了大门。"(生物谷Bioon.com)
参考文献:
Valentin Gensbittel et al, Cell viscosity influences haematogenous dissemination and metastatic extravasation of tumour cells, Nature Materials (2026). DOI: 10.1038/s41563-025-02462-w.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


