Nat Biotechnol:蛋白疗法通过逆转聚糖“刹车”来增强对肿瘤的免疫攻击
来源:生物谷原创 2025-12-17 09:48
通过使用称为凝集素的分子阻断这些聚糖,研究人员证明能显著增强免疫系统对癌细胞的反应。为此,他们创建了名为AbLecs的多功能分子,将凝集素与靶向肿瘤的抗体相结合。
麻省理工学院(MIT)与斯坦福大学的研究人员开发出一种刺激免疫系统攻击肿瘤细胞的新方法,该策略有望使癌症免疫疗法适用于更多患者。他们方法的关键在于逆转癌细胞启动的一种"刹车"机制,该机制会阻止免疫细胞发起攻击。这种刹车由癌细胞表面的糖分子(称为聚糖)控制。

通过使用称为凝集素的分子阻断这些聚糖,研究人员证明能显著增强免疫系统对癌细胞的反应。为此,他们创建了名为AbLecs的多功能分子,将凝集素与靶向肿瘤的抗体相结合。
"我们创造了一种新型蛋白质疗法,可以阻断基于聚糖的免疫检查点并增强抗癌免疫反应。由于已知聚糖在多种肿瘤类型中会抑制对癌症的免疫反应,我们推测我们的分子可能为许多癌症患者提供新的、可能更有效的治疗选择,"MIT生物工程系和化学工程系教授Jessica Stark表示。
Stark同时也是是该论文的第一作者。斯坦福大学化学教授兼Sarafan ChEM-H研究所主任Carolyn Bertozzi是该研究的资深作者。该研究发表在《自然-生物技术》上。
解除刹车
训练免疫系统识别并摧毁肿瘤细胞是治疗多种癌症的有效方法。一类被称为检查点抑制剂的免疫疗法药物,通过阻断PD-1和PD-L1蛋白之间的相互作用来刺激免疫细胞。这解除了肿瘤细胞用以阻止T细胞等免疫细胞杀伤癌细胞的这种刹车机制。
靶向PD-1-PD-L1检查点的药物已被批准用于治疗多种癌症。对部分患者,检查点抑制剂可带来持久的缓解,但对许多其他患者则完全无效。
为了在更多患者中激发免疫反应,研究人员正在寻找靶向癌细胞与免疫细胞之间其他免疫抑制性相互作用的方法。其中一种相互作用发生在肿瘤细胞的聚糖和免疫细胞表面的受体之间。
聚糖存在于几乎所有活细胞上,但肿瘤细胞通常表达健康细胞所没有的聚糖,包括含有称为唾液酸的单糖的聚糖。当唾液酸与位于免疫细胞上的凝集素受体结合时,会开启免疫细胞中的免疫抑制通路。这些能与唾液酸结合的凝集素被称为Siglecs。
"当免疫细胞上的Siglecs与癌细胞上的唾液酸结合时,它会抑制免疫反应。就像PD-1与PD-L1结合时发生的情况一样,这阻止了免疫细胞被激活去攻击和摧毁癌细胞,"Stark解释道。
目前,尽管已有多种药物开发方法尝试,但尚无获批的疗法靶向这种Siglec-唾液酸相互作用。例如,研究人员曾尝试开发能结合唾液酸并阻止其与免疫细胞相互作用的凝集素,但迄今为止,这种方法效果不佳,因为凝集素结合力不够强,无法在癌细胞表面大量积累。
为了克服这个问题,Stark和她的同事开发了一种方法,通过将凝集素附着在靶向癌细胞的抗体上,从而递送更大剂量的凝集素。一旦到达癌细胞表面,凝集素即可与唾液酸结合,阻止唾液酸与免疫细胞上的Siglec受体相互作用。
这解除了免疫反应的刹车,使巨噬细胞和自然杀伤(NK)细胞等免疫细胞能够对肿瘤发起攻击。
"这种凝集素结合域的亲和力通常相对较低,因此无法单独用作疗法。但是,当凝集素结构域与高亲和力的抗体连接时,就可以将其递送到癌细胞表面,在那里结合并阻断唾液酸,"Stark说。
模块化系统
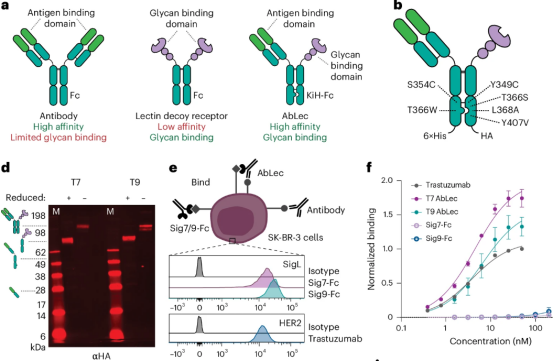
在这项研究中,研究人员基于抗体曲妥珠单抗设计了一种AbLec。曲妥珠单抗可结合HER2,是已获批用于治疗乳腺癌、胃癌和结直肠癌的疗法。为了形成AbLec,他们用凝集素(Siglec-7或Siglec-9)替换了抗体的一条臂。
使用实验室培养的细胞进行的测试表明,这种AbLec能够"重编程"免疫细胞,使其攻击并摧毁癌细胞。
随后,研究人员在一种经过基因改造、能表达人Siglec受体和抗体受体的小鼠模型中测试了他们的AbLecs。这些小鼠被注射了能在肺部形成转移瘤的癌细胞。用AbLec治疗后,这些小鼠的肺转移瘤数量比单独使用曲妥珠单抗治疗的小鼠要少。
研究人员还证明,他们可以置换其他肿瘤特异性抗体,例如靶向CD20的利妥昔单抗,或靶向EGFR的西妥昔单抗。他们还可以置换靶向其他参与免疫抑制的聚糖的凝集素,或靶向PD-1等检查点蛋白的抗体。
"AbLecs真正实现了即插即用,它们是模块化的。你可以想象替换不同的诱饵受体结构域来靶向凝集素受体家族的不同成员,也可以替换抗体臂。这很重要,因为不同的癌症类型表达不同的抗原,你可以通过改变抗体的靶点来解决这个问题,"Stark表示。
Stark、Bertozzi等人已创立一家名为Valora Therapeutics的公司,目前正致力于开发AbLec候选药物。他们希望在两到三年内开始临床试验。(生物谷Bioon.com)
参考文献:
Jessica C. Stark et al, Antibody-lectin chimeras for glyco-immune checkpoint blockade, Nature Biotechnology (2025). DOI: 10.1038/s41587-025-02884-6.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


