银屑病关节炎(PsA)新药!优时比IL-17A/17F双效抑制剂Bimzelx第二项3期临床研究成功!
来源:本站原创 2022-01-22 01:36
Bimzelx(bimekizumab)强效中和IL-17A和IL-17,已被批准治疗斑块型银屑病,疗效击败修美乐(Humira)、喜达诺(Stelara)、可善挺(Cosentyx)。
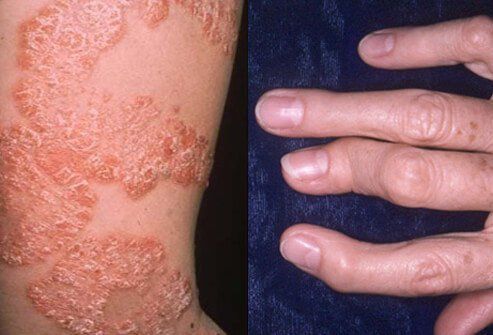
银屑病关节炎(图片来源:onhealth.com)
2022年01月21日讯 /生物谷BIOON/ --优时比(UCB)近日公布了3期BE COMPLETE研究(NCT03896581)的阳性顶线中期分析结果。该研究在接受抗肿瘤坏死因子α(anti-TNF-α)疗法治疗应答不足或不耐受的活动性银屑病关节炎(PsA)成人患者中开展,正在评估新型抗炎药——IL-17A/IL-17F双效抑制剂Bimzelx(bimekizumab)的疗效和安全性。
BE COMPLETE是评估Bimzelx治疗活动性PsA的第二项阳性3期研究。结果显示,研究达到了主要终点和全部次要终点,在所有终点上均显示出统计学意义和临床意义。
主要终点方面:在治疗第16周,采用ACR50应答评估,与安慰剂组相比,Bimzelx治疗组有显著更高比例的患者疾病体征和症状相对基线改善≥50%。该研究中,使用ACR50高治疗目标作为主要结果指标,而不是ACR20。ACR50和ACR20是指疾病体征和症状相对基线改善50%或20%。
次要终点方面:治疗第16周,与安慰剂组相比,Bimzelx治疗组患者在身体功能(采用健康评估问卷残疾指数[HAQ-DI]测量)、皮损清除(采用银屑病面积和严重程度指数至少改善90%[PASI90]来衡量)、身体健康状况(采用健康状况调查简表[SF-36]躯体健康总测量[PCS]评分衡量)、低疾病活动度(采用最低疾病活动度[MDA]指数测定)表现出显著改善。
Bimzelx的安全性与先前研究中的安全性结果一致,没有观察到新的安全性信号。BE COMPLETE研究的全部结果将在即将召开的医学会议上公布,并将发表于同行评议的医学期刊。
BE COMPLETE研究是评估Bimzelx治疗活动性银屑病关节炎(PsA)的2项3期研究之一。另一项研究BE OPTIMAL正在评估Bimzelx治疗先前没有接受过生物类疾病修饰抗风湿药物(bDMARD-naive)的活动性PsA成人患者,阳性顶线中期分析结果已于2021年11月公布,该研究也达到了主要终点和全部次要终点:与安慰剂相比,Bimzelx显著改善了PsA患者的一系列体征和症状,并具有良好的安全性。
基于BE OPTIMAL研究和BE COMPLETE研究的结果,UCB计划在2022年第三季度在美国和欧盟提交Bimzelx治疗PsA的新适应症申请。
UCB免疫解决方案执行副总裁兼美国负责人Emmanuel Caeymaex表示:“BE COMPLETE研究的结果,标志着Bimzelx治疗银屑病关节炎(PsA)和中轴型脊柱关节炎(axSpA)的一系列3期临床试验的最新阳性数据。我们相信,这些一致且强有力的结果,有潜力提高患者的护理水平。PsA项目中2项3期研究均使用ACR50作为主要结果指标,2项研究的阳性结果强调了Bimzelx治疗先前没有接受过生物疗法的PsA患者、以及先前接受过抗TNF-α疗法的PsA患者的临床潜力。”

Bimzelx是一款IL-17A/IL-17F抑制剂,于2021年8月获欧盟批准,用于治疗适合系统治疗的中度至重度斑块型银屑病成人患者。值得一提的是,Bimzelx是第一个旨在同时选择性抑制IL-17A和IL-17F的斑块型银屑病治疗药物。同样在8月,Bimzelx获得了英国药品和保健品管理局(MHRA)的批准,该药是通过新的脱欧后审批途径获得批准的首批药物之一。
Bimzelx将提供一个受欢迎的新治疗选择,帮助更多中重度斑块型银屑病患者实现治疗目标。用药方面,Bimzelx推荐剂量为320mg(皮下注射2针),每4周一次至第16周,之后每8周一次。对于一些体重≥120kg且在第16周未达到完全皮损清除的患者,第16周后给予每4周一次320mg可进一步改善治疗反应。
在治疗中重度斑块型银屑病的3期临床研究中,Bimzelx疗效已被证实优于艾伯维Humira(修美乐,阿达木单抗,adalimumab,TNF抑制剂)、强生Stelara(喜达诺,乌司奴单抗,ustekinumab,IL-12/IL-23抑制剂)、诺华Cosentyx(可善挺,司库奇尤单抗,secukinumab,IL-17A抑制剂),显示出更高水平的皮损清除。在这些研究中,Bimzelx治疗的患者中约60%在第16周达到了皮损完全清除且反应持续一年,并且总体耐受性良好。

bimekizumab作用机制(图片来源:mosmedpreparaty.ru)
Bimzelx的活性药物成分bimekizumab是一种具有双重作用机制的独特分子,这是一种新型人源化单克隆IgG1抗体,能强效、选择性地中和IL-17A和IL-17F,这是驱动炎症过程的2种关键细胞因子。IL-17A和IL-17F具有相似的促炎功能,并独立地与其他炎症介质合作,在多个组织中驱动慢性炎症和损害。
bimekizumab独特的IL-17A/IL-17F双重抑制可能为治疗免疫介导的炎症性疾病提供一种新的靶向疗法。在疾病相关细胞中的临床前研究显示,在抑制IL-17A的同时抑制IL-17F能够减少皮肤和关节炎症以及病理性骨形成,其程度大于单独抑制IL-17A的程度。目前,bimekizumab正处于III期临床开发,用于治疗多种炎症性疾病,包括斑块型银屑病、银屑病关节炎、中轴型脊柱关节炎、化脓性汗腺炎。
此前,医药市场调研机构Evaluate Vantage发布报告预测,bimekizumab上市后,2026年的全球销售额将达到26亿美元。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


