研究开发出纳米药物免疫联合疗法促使“冷”肿瘤转变为“热”肿瘤
来源:深圳先进技术研究院 2021-09-04 08:51
近日,中国科学院深圳先进技术研究院医药所高分子中心副研究员李洋团队有关新型肿瘤穿透纳米凝胶药物免疫联合疗法的研究成果以Reinforcing the Combinational Immuno-Oncotherapy of Switching “Cold” Tumor to “Hot” by Responsive Penetrating
近日,中国科学院深圳先进技术研究院医药所高分子中心副研究员李洋团队有关新型肿瘤穿透纳米凝胶药物免疫联合疗法的研究成果以Reinforcing the Combinational Immuno-Oncotherapy of Switching “Cold” Tumor to “Hot” by Responsive Penetrating Nanogels为题,发表在ACS applied Materials & Interfaces上。
肿瘤中存在的免疫抑制肿瘤微环境会导致效应淋巴细胞浸润不足、功能耗尽,大幅削弱抗肿瘤免疫效应,促使肿瘤变“冷”,使肿瘤免疫治疗效果远低于预期。因此,设计合理的治疗策略,有效地将“冷”肿瘤转变为效应淋巴细胞活跃的“热”肿瘤,是提高抗肿瘤免疫治疗效果的关键。
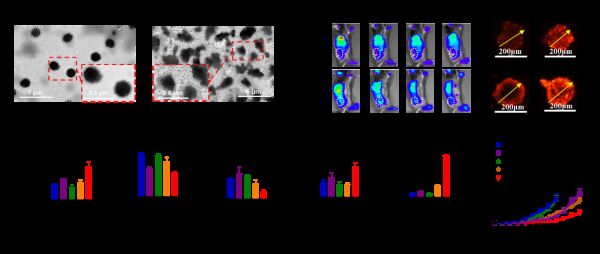
研究团队研发了一种肿瘤微环境响应型深层渗透纳米凝胶药物(E&R@NG)。这种均一、稳定、柔性的纳米凝胶药物可快速富集于肿瘤部位,并在肿瘤微环境下可控释放内部更小尺寸的环糊精-药物包合物,显着改善了免疫调节药物雷西莫特(R848,R)和茶多酚(EGCG,E)在肿瘤部位的富集、渗透与药效。纳米药物在生理条件下可保持完整球形(图A),进入肿瘤微酸环境时,会破碎释放小粒径环糊精-药物包合物(HCD-A)(图B),从而更有效促使药物在肿瘤部位富集(图C),并穿透到达深部肿瘤(图D)。
纳米药物可与抗体激动剂OX40(αOX40)联合应用,可协同增强树突状细胞(DC)的熟化(图E),降低肿瘤组织免疫检查点PD-L1的表达(图F),解除调节性T细胞(Treg)的免疫抑制功能(图G),最终协同增强细胞毒性T淋巴细胞(CTL)的活化和肿瘤浸润(图H),促使肿瘤中活性CTLs与Tregs的比值增加(20.66倍)(图I),从而成功实现“冷”肿瘤向“热”肿瘤的转变,将肿瘤抑制率提升至91.56%(图J),显着增强抗肿瘤免疫治疗效果。该策略还适用于多种肿瘤免疫治疗方案,有望改善临床上肿瘤免疫治疗有效性欠佳的问题。该新型肿瘤穿透型纳米凝胶在肿瘤免疫治疗方面具有良好的转化与应用前景。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


