偏头痛新药!艾伯维口服CGRP受体拮抗剂atogepant:预防性治疗发作性偏头痛,疗效显著,安全!
来源:本站原创 2021-08-30 16:47
如果获批,atogepant将为偏头痛患者提供一种简单、每日口服一次、安全有效的预防性治疗药物。

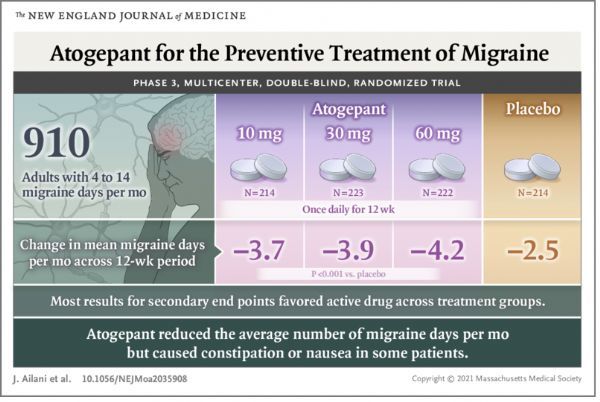
2021年08月29日讯 /生物谷BIOON/ --艾伯维(AbbVie)近日宣布,评估口服降钙素基因相关肽(CGRP)受体拮抗剂(gepant)atogepant预防性治疗偏头痛的3期ADVANCE试验的12周结果已发表于国际医学期刊《新英格兰医学杂志》(NEJM)。文章标题为:Atogepant for the Preventive Treatment of Migraine。
该试验在达到发作性偏头痛(EM)标准的成人患者中开展,入组患者每月经历的偏头痛天数为4-14天。主要终点结果显示:在12周治疗期间,与安慰剂相比,所有剂量(10mg、30mg、60mg,每日口服一次)atogepant将每月平均偏头痛天数从基线水平在统计学上显著降低。次要终点方面,与安慰剂相比,所有剂量atogepant治疗的患者中,有更高比例的患者每月平均偏头痛天数减少≥50%。此外,2种高剂量(30mg、60mg)atogepant在全部6个预先指定的、多重控制的次要终点方面均显示统计学上的显著改善,包括急性药物使用的减少、功能损害测量结果。
atogepant是一种口服CGRP受体拮抗剂(gepant),目前正在接受美国FDA的审查:用于达到发作性偏头痛(EM)标准的成人患者,预防性治疗偏头痛。FDA预计将在2021年第三季度末做出监管决定。如果获得批准,atogepant将是第一个也是唯一一个专门为预防性治疗发作性偏头痛(EM)而开发的口服gepant,将为患者提供一种简单、每天口服一次、安全有效的预防性治疗药物。
艾伯维神经科学开发副总裁Michael Gold表示:“全世界有太多人面临偏头痛带来的挑战,这给患者、护理人员和医疗系统带来了沉重的负担。在艾伯维,我们坚定地致力于在偏头痛连续体中推进新的治疗方案。这些数据增强了我们对atogepant作为偏头痛预防治疗潜在选择的信心。”
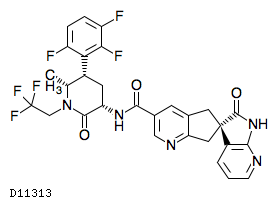
atogepant化学结构式(图片来源:genome.jp)
偏头痛是一种复杂的慢性疾病,其发作通常会使患者失去正常生活或工作的能力,可包括头部剧痛以及神经和自主神经症状。偏头痛症状和严重程度在个体中变化很大。偏头痛发作会使人衰弱,但偏头痛是一种可以治疗的疾病。
atogepant是一种口服降钙素基因相关肽(CGRP)受体拮抗剂(gepant),专门开发用于偏头痛的预防性治疗。CGRP及其受体表达于与偏头痛病理生理相关的神经系统区域。研究表明,CGRP水平在偏头痛发作期间升高,选择性CGRP受体拮抗剂对偏头痛有临床疗效。
atogepant NDA基于一个强大的临床项目数据支持。该项目在近2500名每月偏头痛4-14天的患者中开展,评估了口服atogepant用于偏头痛预防性治疗的疗效、安全性和耐受性,项目中包括关键3期ADVANCE研究、关键2b/3期研究(CGP-MD-01)和3期长期安全性研究。
在偏头痛领域,艾伯维正在销售BOTOX(保妥适®,肉毒杆菌毒素A,onabotulinumtoxinA)和Ubrelvy(ubrogepant)。其中,BOTOX是美国FDA批准的第一个针对成人慢性偏头痛的预防性药物,Ubrelvy则是美国FDA批准的第一种口服CGRP受体拮抗剂(gepant),用于成人偏头痛(有或无先兆)的急性治疗。
ADVANCE研究主要终点结果(图片来源:NEJM)
ADVANCE是一项多中心、随机、双盲、安慰剂对照、平行组3期试验,旨在评估口服atogepant预防偏头痛的有效性、安全性和耐受性。共有910名患者被随机分为4个治疗组,分别为3种剂量(10mg、30mg、60mg)atogepant、安慰剂,每日口服一次。疗效分析基于873名患者的改良意向治疗(mITT)人群。
主要终点是在12周治疗期间,每月平均偏头痛天数与基线相比的变化。数据显示,所有atogepant剂量组均达到主要终点,且与安慰剂相比每月平均偏头痛天数在统计学上显著减少。10mg/30mg/60mg atogepant组分别减少了3.7/3.9/4.2天、安慰剂组减少了2.5天(所有剂量组与安慰剂组相比,p<0.0001)。
在12周治疗期间,预先指定的、多重控制的次要终点疗效结果包括:
——每月平均头痛天数:10mg/30mg/60mg atogepant组分别显著减少了3.9(基线8.4)、4.0(基线8.8)、4.2(基线9.0)天,安慰剂组减少了2.5天(基线8.4天)(所有剂量组与安慰剂组相比,p<0.0001)。
——每月平均急性药物使用天数:10mg/30mg/60mg atogepant组与基线相比分别减少了3.7/3.7/3.9天,安慰剂组减少了2.4天(所有剂量组与安慰剂组相比,p<0.0001)。
——每月偏头痛天数减少≥50%的患者比例:12周治疗期间,10mg/30mg/60mg atogepant组分别有55.6%/58.7%/60.8%的患者减少≥50%、安慰剂组患者达标比例为29.0%(所有剂量组与安慰剂组相比,p<0.0001)。
——偏头痛特异性生活质量问卷2.1版(MSQ v2.1)角色功能限制性域得分:在第12周,与安慰剂组相比,10mg/30mg/60mg atogepant组均显著改善(9.9分、10.1分、10.8分;所有剂量组与安慰剂组相比,p<0.0001)。
——平均每月偏头痛日记中的活动障碍(AIM-D)日常活动域得分:与安慰剂组相比,观察到30mg组和60mg组的平均每月AIM-D日常活动域得分显著提高,30mg组为-2.5分(p=0.0005),60mg组为-3.3分(p<0.0001)
——与日常活动域的表现类似,AIM-D评分中的身体损伤域显示:与安慰剂组相比,30 mg和60mg atogepant组在统计学上有更大的改善,30mg组改善幅度为-2.0(p=0.0021),60mg组改善幅度为-2.5(p=0.0002)。
该研究中,所有剂量atogepant均耐受性良好。在至少一个atogepant治疗组中报告的最常见(≥5%)不良事件为便秘(各剂量组为6.9-7.7%,安慰剂组为0.5%)、恶心(各剂量组为4.4-6.1%,安慰剂组为1.8%)、上呼吸道感染(各剂量组为3.9-5.7%,安慰剂组为4.5%)。便秘、恶心和上呼吸道感染的大多数病例的严重程度为轻度或中度,并未导致停药。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->