2021年7月CRISPR/Cas研究进展
来源:本站原创 2021-07-31 23:57
2021年7月31日讯/生物谷BIOON/---基因组编辑技术CRISPR/Cas9被《科学》杂志列为2013年年度十大科技进展之一,受到人们的高度重视。2020年10月,德国马克斯-普朗克病原学研究所的Emmanuelle Charpentier博士以及美国加州大学伯克利分校的Jennifer A. Doudna博士因在CRISPR-Cas9基因编辑方面做
2021年7月31日讯/生物谷BIOON/---基因组编辑技术CRISPR/Cas9被《科学》杂志列为2013年年度十大科技进展之一,受到人们的高度重视。2020年10月,德国马克斯-普朗克病原学研究所的Emmanuelle Charpentier博士以及美国加州大学伯克利分校的Jennifer A. Doudna博士因在CRISPR-Cas9基因编辑方面做了的贡献荣获2020年诺贝尔化学奖。
CRISPR是规律间隔性成簇短回文重复序列的简称,Cas是CRISPR相关蛋白的简称。CRISPR/Cas最初是在细菌体内发现的,是细菌用来识别和摧毁抗噬菌体和其他病原体入侵的防御系统。
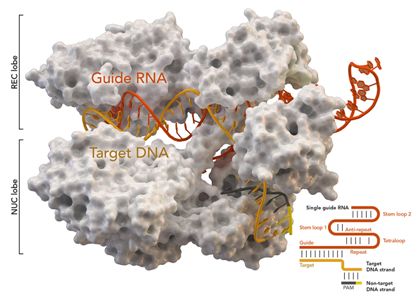
图片来自Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0)。
2018年11月26日,中国科学家贺建奎声称世界上首批经过基因编辑的婴儿---一对双胞胎女性婴儿---在11月出生。他利用一种强大的基因编辑工具CRISPR-Cas9对这对双胞胎的一个基因进行修改,使得她们出生后就能够天然地抵抗HIV感染。这也是世界首例免疫艾滋病基因编辑婴儿。这条消息瞬间在国内外网站上迅速发酵,引发千层浪。有部分科学家支持贺建奎的研究,但是更多的是质疑,甚至是谴责。
即将过去的7月份,有哪些重大的CRISPR/Cas研究或发现呢?小编梳理了一下这个月生物谷报道的CRISPR/Cas研究方面的新闻,供大家阅读。
1.Nat Commun:利用CRISPR-Cas13b基因编辑技术高效阻止新冠病毒及其变体在人细胞中的复制
doi:10.1038/s41467-021-24577-9
最近,令人担忧的SARS-CoV-2病毒变体的出现突出表明需要创新方法以便同时抑制病毒复制和防止病毒逃避宿主免疫反应和抗病毒药物治疗。在一项新的研究中,澳大利亚研究人员使用一种称为CRISPR-Cas13b的基因编辑技术成功地阻止SARS-CoV-2病毒在受感染的人类细
胞中的复制,这可能为治疗COVID-19铺平道路。鉴于这种CRISPR基因编辑工具在实验室测试中可有效阻止这种病毒复制,他们希望尽快开始动物实验。相关研究结果于2021年7月13日发表在Nature Communications期刊上,论文标题为“Reprogrammed CRISPR-Cas13b
suppresses SARS-CoV-2 replication and circumvents its mutational escape through mismatch tolerance”。

CRISPR-Cas13b设计原理,图片来自Nature Communications, 2021, doi:10.1038/s41467-021-24577-9。
论文通讯作者、澳大利亚彼得-多尔蒂感染与免疫研究所的Sharon Lewin博士表示,他们设计的CRISPR-Cas13b能够识别导致COVID-19的SARS-CoV-2病毒。在识别后,Cas13b就会切割这种病毒的基因组,从而阻止它在人细胞中的复制。
2.Mol Ther:腺嘌呤碱基编辑有望治疗α-1-抗胰蛋白酶缺乏症
doi:10.1016/j.ymthe.2021.06.021
单基因疾病α-1-抗胰蛋白酶缺乏症(Alpha-1 antitrypsin deficiency, AATD)是一种常见的遗传性疾病,会影响肝脏和肺部。一项新的研究显示一种新的基因编辑形式能够有效地校正AATD患者细胞中的突变。这种称为腺嘌呤碱基编辑的新方法与包括CRISPR在内的其他
编辑形式不同,因为这种碱基编辑不会诱发DNA断裂,这有助于防止双链断裂、潜在的脱靶编辑以及细胞修复过程中不需要的突变。相关研究结果于2021年7月1日在线发表在Molecular Therapy期刊上,论文标题为“Adenine Base Editing Reduces Misfolded Protein
Accumulation and Toxicity in Alpha-1 Antitrypsin Deficient Patient ipsC-Hepatocytes”。
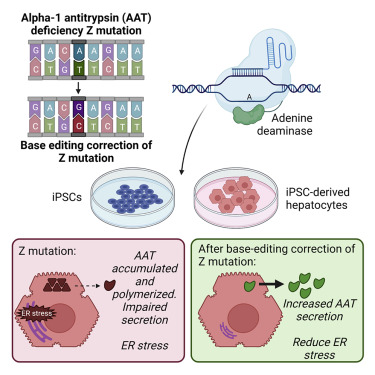
图片来自Molecular Therapy, 2021, doi:10.1016/j.ymthe.2021.06.021。
Wilson说,“这项研究显示了成功应用碱基编辑技术来校正AATD患者衍生性肝细胞中导致这种疾病的突变。我希望这些结果将为利用这项技术帮助AATD和其他单基因疾病的患者提供机会。”
3.Nat Commun:科学家成功利用CRISPR碱基编辑技术纠正产前溶酶体贮积病
doi:10.1038/s41467-021-24443-8
子宫内的碱基编辑或有望在机体病变发生之前来纠正致病性的突变,1型黏多糖病(MPS-IH,贺勒氏症,指任何一种涉及黏多糖先天性代谢紊乱的疾病)是一种影响机体多个器官功能的溶酶体贮积病(LSD,lysosomal storage disease),其通常会导致个体出生后发生早
期的心肺衰竭。如今越来越多的研究证据证实了在出生前纠正致死性的遗传性疾病可行性,近日,一篇发表在国际杂志Nature Communications上题为“In utero split AAV9 adenine base editing corrects the multi-organ pathology in a lethal lysosomal
storage disease”的研究报告中,来自费城儿童医院等机构的科学家们通过研究成功利用DNA碱基编辑技术对产前小鼠模型进行研究,纠正了一种被称为贺勒氏症的溶酶体贮积病。利用一种在腺相关病毒载体中运输的腺嘌呤碱基编辑器,研究人员就能纠正负责这种疾病
的单一碱基突变,这种疾病在个体出生前就已经开始进展了,其会影响多个器官的功能,如果不及时治疗的话,有可能会导致个体在儿童期就发生死亡。
医学博士William H. Peranteau表示,本文研究结果表明,在临床前小鼠模型中利用产前碱基编辑技术来治疗贺勒氏症是可行的。除了能够展示出生前治疗该疾病的益处外,研究者还发现,利用这种碱基编辑工具还能在个体出生后对其进行矫正,这就突出了该技术在产
前和产后治疗贺勒氏症的前景和希望。贺勒氏症是一种溶酶体贮积病,在西方国家中,大约每10万名婴儿中就有1名婴儿会受到该病的影响,该病的发生通常是由单一DNA碱基突变所引起的,即腺嘌呤代替了鸟嘌呤;患儿出生后6个月时,其就会出现肝脏和脾脏肿胀、腹壁
疝气、肌肉骨骼异常、视网膜和神经认知退化及心脏病等疾病表现;如果不加以治疗的话,患者在5-10岁时会因心肺并发症而发生死亡;即使接受了治疗,患者也会出现一定的疾病并发症,因为目前的治疗方法所产生的治疗效果非常有限,尤其是在患儿延迟治疗的情况
下。
由于这种疾病的病理学表现在患者出生前就已经开始了,因此研究人员认为,该综合征是产前治疗的最佳候选对象,基于这一考虑,研究人员利用CRISPR碱基编辑技术成功将MPS-IH小鼠模型中突变的腺嘌呤转换成了鸟嘌呤,该技术只需要单链DNA的破裂,其要比其它编辑
方法更加有效且安全。文章中,研究人员使用了一种腺相关病毒9(AAV9)病毒载体来讲碱基编辑器运输到胎儿小鼠模型中,结果发现,接受产前治疗的小鼠模型表现出了存活率的提高和机体代谢、骨骼和心脏疾病病理学表现的改善。值得注意的是,研究人员在模型机体
中的肝脏和心脏中都观察到了修正细胞的存在,这就表明这种疗法或能对多个器官有效。
4.Cell:揭示DNA修复蛋白RAD51可让CRISPR基因编辑更高效
doi:10.1016/j.cell.2021.04.035
基因编辑是有目的地改变基因的DNA序列,是研究突变如何导致疾病,以及为治疗目的改变一个人的DNA的有力工具。在一项新的研究中,美国麻省理工学院大脑与认知科学教授Guoping Feng及其团队开发出一种可用于这两种目的的新型基因编辑方法。相关研究结果近期
发表在Cell期刊上,论文标题为“Efficient embryonic homozygous gene conversion via RAD51-enhanced interhomolog repair”。
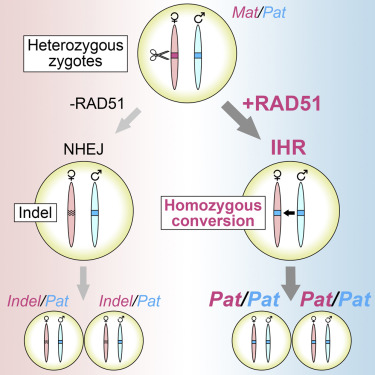
图片来自Cell, 2021, doi:10.1016/j.cell.2021.04.035。
Feng实验室接下来着手了解RAD51增强基因编辑的机制。他们假设RAD51参与了一种叫做同源体间修复(interhomolog repair, IHR)的过程,即一条染色体上的DNA断裂以该染色体的第二个拷贝(来自另一个亲本)为模板进行修复。为了测试这一点,他们给小鼠胚胎注射 了RAD51和CRISPR,但没有注射模板DNA。他们对CRISPR进行编程,只切割其中一条染色体上的基因序列,然后测试它是否被修复以匹配未切割染色体拷贝上的序列。在这个实验中,他们不得不使用母体和父体染色体上的序列不同的小鼠。他们发现,单独注射CRISPR的对 照组胚胎很少出现IHR修复。然而,添加RAD51显著增加了编辑CRISPR靶向基因以匹配未切割染色体拷贝的胚胎数量。
Wilde说,“以前对IHR的研究已发现,它在大多数细胞中的效率低得惊人。我们发现它在胚胎细胞中更容易发生,并且可以被RAD51增强,这表明更深入地了解是什么使胚胎允许这种类型的DNA修复,可能帮助我们设计更安全和更有效的基因疗法。”
5.eLife:改造蚊子基因是否阻止传播疟疾
doi:10.7554/eLife.58791
越来越多的蚊子对杀虫剂的抗药性,以及疟疾寄生虫对抗疟药物的抗药性,使人们迫切需要新的方法来对抗这种疾病。蚊虫媒介抗药性和寄生虫抗药性的上升突出表明,如果要使消灭疟疾继续成为可行的目标,就迫切需要开发新的工具。在 eLife发表的一项初步研究表
明,改变蚊子的肠道基因,使其将抗疟基因传播给下一代蚊子,有望成为遏制疟疾的一种方法。
这项研究是利用CRISPR-Cas9基因编辑技术对蚊子基因进行改变的一系列步骤中的最新一步,这些基因可能会降低蚊子传播疟疾的能力。如果进一步的研究支持这一方法,它将为减少疟疾引起的疾病和死亡提供一种新的方法,也是控制疟疾的很有希望的工具。
研究人员对传播疟疾的蚊子冈比亚按蚊进行了基因改造。他们使用CRISPR-Cas9技术在蚊子进食血粉后打开的基因中插入了一种编码抗疟蛋白的基因。研究小组这样做的方式,使整个部分的DNA也发挥了基因驱动作用,可以传递给大多数蚊子的后代。他们最初将该基因与
荧光标记一起插入,以帮助他们在DNA中的三个不同点追踪该基因,然后移除该标记,只留下一个小的基因修饰。接下来,他们培育了这些蚊子,看看它们是否能够成功繁殖并保持健康。他们还测试了疟原虫在蚊子体内的发育情况。
这些基因改造是被动的,可以在现场进行测试,并经过严格的监管程序,保证它们能够安全有效地阻断寄生虫,不会引起人们对环境中意外传播的担忧。把它们和其他蚊子结合在一起,再加上一种活跃的基因驱动,它们就会变成基因驱动,而不需要任何进一步的改变。
这些研究使基因驱动技术在这一领域更接近于作为一种消灭疟疾的策略而被测试。
6.Cell:新研究揭示结核杆菌的脆弱性基因和非脆弱性基因
doi:10.1016/j.cell.2021.06.033
开发防治结核病的药物可能是一件令人沮丧的事情。一旦发现对细菌的生命周期至关重要的基因,科学家们急于开发抑制该靶标的药物,然后是失望。一系列靶向必需基因靶标的化合物对结核杆菌的生长几乎没有影响。这种细菌继续生存。科学家们又回到了原点。如今
,一项新的研究有助于解释为何基于靶标的抗生素在起步阶段遇到如此多的麻烦。一个答案是,必需基因靶标在对抗生素的脆弱程度上有所不同。来自美国洛克菲勒大学和威尔康乃尔医学院的研究人员发现,理想的靶标是如此容易受到攻击,以至于当它被轻微抑制时,
细胞就无法生存。另一方面,非脆弱性基因(invulnerable gene)可以经受住几乎完全的抑制,在遭受抗生素的攻击时也能勉强维持足够的靶标活性而使细胞存活。此外,这些作者首次对病原体的脆弱性进行了量化,产生了一个指数,用于根据使基因失效并使细胞瘫痪
所需的抑制量对结核杆菌中的几乎每一个必需基因进行排名。相关研究结果于2021年7月22日在线发表在Cell期刊上,论文标题为“Genome-wide gene expression tuning reveals diverse vulnerabilities of M. tuberculosis”。

图片来自Cell, 2021, doi:10.1016/j.cell.2021.06.033。
论文共同第一作者、Rock实验室医生科学家Barbara Bosch说,“我们开发了一种可以调整的系统,从没有抑制到几乎100%的抑制。这使我们能够确定这种细菌是否有严重的适应度成本(fitness cost),或者它们是否仍然活着和活跃。”
由此产生的脆弱性指数,将抑制百分比与细菌的适应度联系起来,表明脆弱性是决定抗生素是否成功的一个关键因素。例如,两个最脆弱的基因恰好也是市场上两种最强效的抗结核病药物的靶标。相反,两个最不脆弱的基因,即coaA和def,曾经是很有希望的药物靶标, 但是靶向这些基因的抗生素却未能杀死这种细菌。这些靶标的非脆弱性可能是这些药物失败的一个原因。
这种脆弱性指数还确定了几个新的靶标,这些靶标是必需的,高度脆弱的,而且是药物开发商尚未探索的。其中的一些靶标甚至比目前的一线抗结核病药物更脆弱,并令人吃惊地影响着细胞中的各种活动。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


