RNAi治疗罕见肝病!美国FDA授予Arrowhead第二代皮下RNAi疗法ARO-AAT突破性疗法认定!
来源:本站原创 2021-07-30 17:47
ARO-AAT用于治疗与α-1抗胰蛋白酶缺乏症(AATD)相关的罕见遗传性肝病。
肝脏(图片来源:futuremedicineindia.com)
2021年07月29日讯 /生物谷BIOON/ --Arrowhead制药公司近日宣布,美国食品和药物管理局(FDA)已授予RNAi药物ARO-AAT(也称为TAK-999)突破性疗法认定(BTD),用于治疗与α-1抗胰蛋白酶缺乏症(AATD)相关的罕见遗传性肝病,这种疾病可严重损害患者的肝脏和肺脏。此前,ARO-AAT还获得FDA授予孤儿药资格(ODD)和快速通道资格(FTD),并获得欧盟委员会授予ODD。
ARO-AAT是Arrowhead公司的第二代皮下给药RNAi疗法,目前正与武田制药共同开发。ARO-AAT旨在抑制突变的α-1抗胰蛋白酶(Z-AAT)蛋白在肝脏的产生,这是AATD患者进行性肝病的原因。减少炎症性Z-AAT蛋白的产生有望阻止肝病的进展,并可能使肝脏再生和修复。
BTD是FDA的一个新药评审通道,旨在加快开发及审查用于治疗严重或威及生命的疾病、并且有初步临床证据表明与现有治疗药物相比能够实质性改善病情的新药。获得BTD的药物,在研发时能得到包括FDA高层官员在内的更加密切的指导,在审查时有资格进行滚动审查和潜在优先审查,以保障在最短时间内为患者提供新的治疗选择。
Arrowhead首席医疗官Javier San Martin医学博士表示:“AATD相关肝病患者目前除了肝移植外没有其他治疗选择。获得FDA的突破性疗法认定,是ARO-AAT研究项目的一个重要里程碑。Arrowhead和我们在武田的合作者对AATD患者有着共同的承诺。我们打算利用BTD提供的优势,包括加强获得FDA高层官员和经验丰富的审查人员的指导,来加快ARO-AAT的开发。我们希望尽快将这一重要的药物提供给患者。”
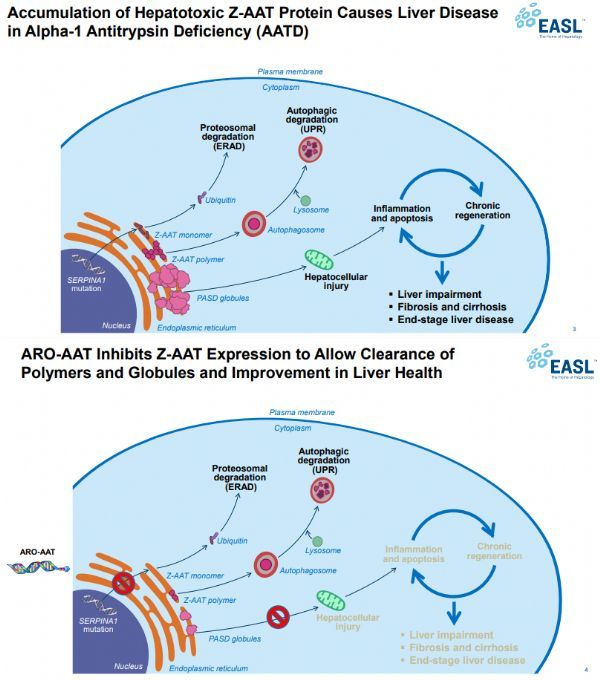
AATD相关肝病及ARO-AAT作用机制
ARO-AAT 2期SEQUOIA研究最近已完成全部40例患者入组。Arrowhead公司最近在2021年欧洲肝脏研究协会(EASL)国际肝脏大会上公布的ARO-AAT2002 2期开放标签研究的中期结果非常令人鼓舞。
这些中期结果表明,ARO-AAT持续减少了毒性突变Z-AAT蛋白的产生,该蛋白已被确定为AATD患者进展性肝病的原因。
此外,在6个月和12个月期间毒性突变Z-AAT蛋白产生的减少,在AATD所致肝纤维化患者中已导致与肝脏疾病愈合相关的多个重要信号。(详细结果见EASL会议报告:EASL 2021 ARO-AAT2002 Presentation)
ARO-AAT2002 2期开放标签研究结果
α-1抗胰蛋白酶相关缺乏症(AATD)是一种罕见的遗传性疾病,与儿童和成人中的肝病以及成人中的肺部疾病相关。据估计,AATD在美国每3000-5000人中影响1人,在欧洲每2500人中影响1人。AAT蛋白主要由肝细胞合成和分泌,它的功能是抑制分解正常结缔组织的酶。最常见的疾病变体,Z突变体,有一个单个氨基酸替代,导致蛋白质的不正确折叠。突变蛋白不能有效分泌,并在肝细胞内以球状聚集。这会引发持续的肝细胞损伤,导致纤维化、肝硬化和肝细胞癌风险增加。
纯和PiZZ基因型个体严重缺乏功能性AAT,导致肺部疾病和肝脏疾病。肺部疾病常采用AAT强化治疗。然而,强化治疗对肝脏疾病没有任何治疗作用,也没有针对肝脏表现的特异性治疗方法。肝移植是目前唯一有效的治疗选择,因此该领域存在大量未满足的需求。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->