每年补液2次!罗氏新型眼内给药系统ranibizumab PDS(眼内植入物)美国进入优先审查:疗效媲美每月注射!
来源:本站原创 2021-06-27 02:04
这款PDS植入物仅一粒米大小,可连续补液(6个月一次),如果上市将有望大幅降低患者治疗负担。
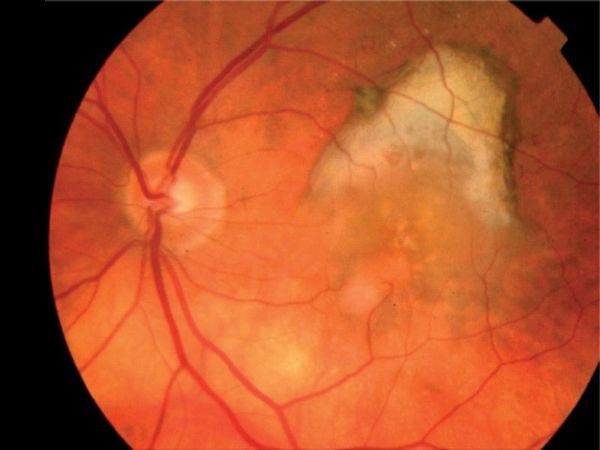
nAMD(图片来源:medscape.com)
2021年06月26日讯 /生物谷BIOON/ --罗氏(Roche)旗下基因泰克近日宣布,美国食品和药物管理局(FDA)已受理该公司提交的一份生物制品许可申请(BLA),该BLA正处于优先审查。此次BLA有关一种新的眼内给药系统ranibizumab PDS(雷珠单抗玻璃体植入物),用于治疗新生血管性年龄相关性黄斑变性(nAMD,又名“湿性AMD”,wet-AMD)。FDA预计将在2021年10月23日前做出审批决定。在欧洲,PDS营销授权申请(MAA)已被欧洲药品管理局(EMA)受理,目前正在审查中。
PDS(Port Delivery System)是一种永久性的、可重复填充药物的眼内植入物,大小约为一粒米,可在数月内持续递送定制配方的雷珠单抗(ranibizumab),有潜力减少频繁眼部注射带来的治疗负担。
PDS可连续补液(6个月一次),如果获得批准,PDS将成为第一个也是唯一一个可持续递送药物的眼内植入物,将为湿性AMD患者提供一种替代频繁眼内注射抗血管内皮生长因子(VEGF)的治疗方法,后者是当前湿性AMD的标准护理方案。
罗氏首席医学官兼全球产品开发主管 Levi Garraway博士表示:“抗VEFG疗法能为湿性AMD患者带来显著的益处,但要达到最佳效果,患者就必须经常去医院进行眼部注射。这一负担使许多患者治疗不足,容易视力下降。如果获得批准,PDS将通过提供长达6个月的不间断治疗来改变湿性AMD的治疗方法,与目前在临床上取得的结果相比,这种治疗方法可能潜在地改善视力。”
PDS BLA提交,基于3期ARCHWAY研究(NCT03677934)的积极结果。该研究达到了主要终点,数据显示:接受PDS治疗的湿性AMD患者中,98%以上的患者在补药前能够长达6个月不需要额外治疗。此外,这些患者获得的视力结果,与每月一次接受0.5mg雷珠单抗注射的患者一致。该研究中,PDS的耐受性良好,并具有良好的益处风险概况。
PDS在临床试验中的安全性已被充分了解,并将继续受到密切监测。如果获得批准,PDS将是第一个也是唯一一个允许6个月间隔的湿性AMD疗法。
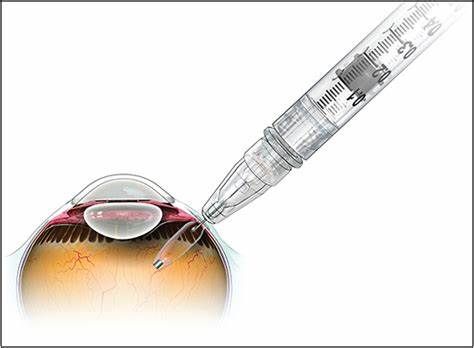
PDS补液操作示意图(retinalphysician.com)
新生血管性AMD(nAMD)是全球60岁及以上人群致盲的主要原因,目前对nAMD的标准护理方案要求患者每月去看眼科医生,接受抗血管内皮生长因子(VEGF)的眼部注射,以帮助维持视力增益和/或防止视力下降。抗VEGF疗法的高治疗负担可能导致nAMD治疗不足、潜在低于最佳视力的结果。
雷珠单抗是一种血管内皮生长因子(VEGF)抑制剂,旨在结合和抑制VEGF-A,这是一种在新血管形成和血管渗漏中起关键作用的蛋白质。
PDS含有未经监管机构批准的雷珠单抗定制配方,它不同于雷珠单抗玻璃体腔注射液(Lucentis®,雷珠单抗注射液),后者已被批准用于治疗nAMD和其他视网膜疾病。
通过每年2次补液保持雷尼珠单抗的治疗药物浓度水平,PDS能够为nAMD患者在视力增益和维持这些增益方面提供更大的结果确定性。此外,通过减少频繁注射和医生就诊的需要,PDS可以减轻与标准抗VEGF治疗相关的治疗负担。
除了ARCHWAY研究之外,PORTAL研究正在调查PDS治疗nAMD的长期安全性和耐受性。此外,PAGODA研究正在调查PDS治疗糖尿病黄斑水肿(DME),这是糖尿病的视力威胁性并发症。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->