Brain Behavior and Immunity:粪便移植探索菌群与阿尔茨海默病的联系
来源:本站原创 2021-06-23 16:35
肠道微生物区系被证明与阿尔茨海默病(AD)β淀粉样蛋白(Aβ)病理的发生有关。由于将基于无菌小鼠的微生物区系研究结果转化为临床实践存在困难,在此,作者使用短期抗生素疗法来开发一种新的模型,该模型具有接近无菌状态并且不影响Aβ病理。3月龄APPswe/ps1ΔE9小鼠经灌胃给予抗生素2周,使其接近无菌状态,然后接受16月龄APPswe/ps1ΔE9小鼠的供体粪
肠道微生物区系被证明与阿尔茨海默病(AD)β淀粉样蛋白(Aβ)病理的发生有关。由于将基于无菌小鼠的微生物区系研究结果转化为临床实践存在困难,在此,作者使用短期抗生素疗法来开发一种新的模型,该模型具有接近无菌状态并且不影响Aβ病理。3月龄appswe/ps1ΔE9小鼠经灌胃给予抗生素2周,使其接近无菌状态,然后接受16月龄appswe/ps1ΔE9小鼠的供体粪便,连续7d。在抗生素治疗前、抗生素暴露后、粪便微生物区系移植前后收集粪便颗粒进行肠道微生物区系分析。令人惊讶的是,植入微生物菌群后,Aβ斑块周围的星形胶质细胞激活受到抑制,而不是小胶质细胞,小胶质细胞是Aβ清除过程中公认的斑块吞噬细胞类型。作者的发现为从肠道-脑轴理解阿尔茨海默病的机制和将肠道微生物区系操作从实验台转化到临床实践提供了一个新的框架。
图片来源:https://doi.org/10.1016/j.bbi.2021.06.003
微生物在人类健康和疾病发展中扮演着重要而多样的角色。一方面,它们被积极地用于预防和/或治疗疾病。另一方面,致病微生物形式对健康和福祉构成潜在威胁。胃肠道(GIT)仍然是人体内最大的微生物种群储存库。据估计,人类的微生物区系由数万亿个微生物组成,而这个复杂的微生物群落已被证明会影响宿主的动态平衡。几十年的研究结果表明,肠道微生物区系和中枢神经系统(CNS)之间通过肠道-脑轴进行双向交流。肠道微生物区系的改变不仅会影响各种肠道疾病,还会影响中枢神经系统疾病,如焦虑、抑郁、帕金森氏病和阿尔茨海默病(AD)。
AD是最常见的痴呆症,是一种与年龄相关的进行性神经退行性疾病,主要特征是β-淀粉样蛋白(A-β)主要沉积在大脑皮层和海马区,导致进行性学习和记忆障碍。尽管研究成果有了很大的进步,但对AD的病因、预防和治疗的完全了解仍然是难以捉摸的。最近的研究表明,肠道微生物区系组成的改变与阿尔茨海默病有关。例如,一项研究表明,在appSWE/PS1ΔE9雄性小鼠中,长期服用抗生素导致肠道菌群组成发生变化,并减少了Aβ淀粉样变。Cox等人的研究发现脆弱类杆菌在TG2576转基因小鼠促进斑块沉积中的作用。此外,接受app-小鼠粪便微生物区系移植的app+小鼠认知功能得到改善,Aβ沉积减少。更重要的是,一种名为低聚甘露酸钠的新药已经被发现可以治疗重塑肠道微生物区系,抑制肠道细菌氨基酸形状的神经炎症,从而抑制AD的进展。这些发现提示肠道微生物区系可能与AD病理有关。用来自(12个月大)常规app/PS1-21小鼠的粪便样本对无菌(GF)小鼠的定植进一步证实了这一点。然而,这些结果并不能确凿地支持肠道微生物区系在促进AD病理进展中的具体作用。虽然GF小鼠已经成为研究肠道微生物区系在不同疾病中的生理作用的标准模型,但由于无法在人类中获得GF状态,使得这种方法很难在人类身上复制,因此不可能转化为临床实践。因此,迫切需要一种能够模拟AD生理微生物区系变化过程的模型。
先前的研究发现,用抗生素治疗可能会耗尽肠道微生物区系,从而获得受操纵的近乎无菌的小鼠模型,它们很容易与来自供体的肠道微生物区系定植,可广泛应用于评估微生物区系功能。作者首先想要调查抗生素治疗可以在多大程度上耗尽app/PS1转基因小鼠的肠道微生物区系。通过对appSWE/PS1βE9小鼠肠道微生物区系组成和Δ淀粉样变性的分析,评价短期抗生素治疗(2周)的效果。然后将5岁(16个月大)appswe/ps1、Δ、E9转基因小鼠的粪便微生物区系移植给经抗生素处理的小鼠。通过检测移植小鼠脑内Aβ沉积和胶质细胞活化来评价FMT的作用。此外,作者探索了氟米特诱导的肠道微生物区系的时间进程,并强调了在Aβ斑块发展中可能有重要意义的潜在的区分微生物种类。
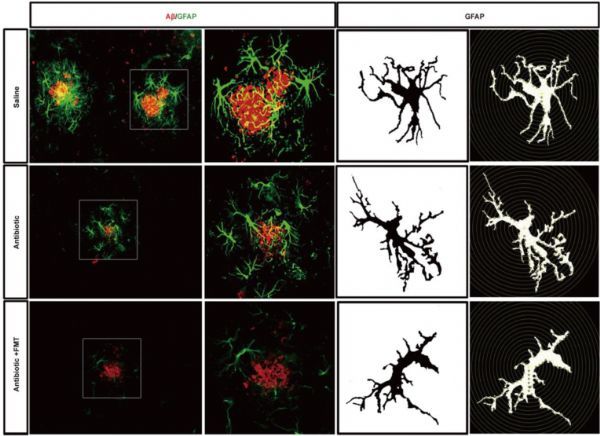
免疫荧光图像显示FMT后星形胶质细胞的形态
图片来源:https://doi.org/10.1016/j.bbi.2021.06.003
总之,作者的发现强调了AD与肠道微生物区系组成的改变有关,而肠道微生物区系组成的改变也与Aβ病理和星形胶质细胞形态有关。此外,作者发现短期抗生素治疗引起的肠道微生物区系的改变导致了近无菌状态,但对appSWE/PS1βE9小鼠的AΔ病理和星形胶质细胞形态没有明显的影响。然而,与空载对照处理的appswe/ps1βE9小鼠相比,fmt诱导的肠道微生物区系改变足以显著增加AΔ斑块的沉积,并伴随星形胶质细胞形态的改变。这些观察表明,微生物区系的改变本身可能不足以影响Aβ的发育,表明影响AD进展的微生物区系变化必须与与AD严重程度和遗传背景一致的细菌群落相关。作者的发现为从肠道-脑轴了解AD的发病机制提供了一个新的框架,也为AD的基础研究和翻译研究开发了一种新的加速小鼠模型。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。