多发性硬化(MS)新药!新型糖工程化抗CD20单抗ublituximab 3期临床疗效优于Aubagio(特立氟胺)!
来源:本站原创 2021-06-21 03:08
Aubagio(奥巴捷)是一款行业领先的口服MS药物,于2018年7月在中国获批上市。

多发性硬化(MS,图片来源:medgadget.com)
2021年06月20日讯 /生物谷BIOON/ --TG Therapeutics公司近日公布了2项全球性阳性药物对照3期临床试验(ULTIMATE I & II)的数据。这些试验在复发型多发性硬化(RMS)患者中开展,将ublituximab与目前广泛使用的一线口服标准护理药物Aubagio(teriflunomide,特立氟胺)进行了比较。(结果详见:ULTIMATE I & II EAN2021 Steinman FNAL PDF)。
这2项研究是在与美国FDA达成的特别方案评估(SPA)协议下开展的。2项研究均达到了主要终点:结果显示在治疗96周期间,ublituximab与Aubagio相比将年化复发率(ARR)在统计学上显著降低(每个试验中p<0.005)。2项研究中,ublituximab治疗组的ARR均<0.10,与Aubagio组相比ARR相对降低率分别约为60%和50%。2项研究也达到了磁共振成像(MRI)关键次要终点。这些数据,将用于支持ublituximab治疗RMS的生物制品许可申请(BLA),该BLA计划2021年第三季度提交。
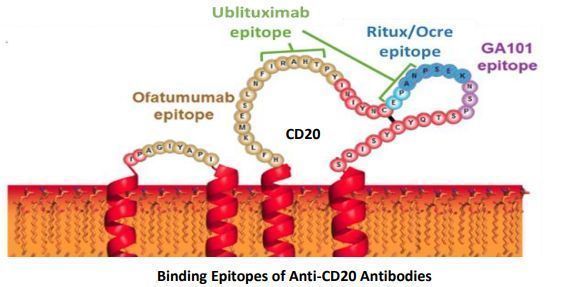
ublituximab是一种新型糖工程化抗CD20单克隆抗体,靶向成熟B淋巴细胞上CD20抗原的独特表位,该表位与目前已上市的多款CD20单抗不同,包括ofatumumab、ocrelizumab/rituximab、obinutuzumab(GA101)。目前,ublituximab正处于III期临床开发,用于治疗多发性硬化(MS)和慢性淋巴细胞白血病(CLL)。
Aubagio是赛诺菲的一款口服药物,分别于2012年9月、2013年8月在美国和欧盟获批上市,用于治疗RMS成人患者。该药是一款行业领先的口服多发性硬化(MS)药物,已在全球超过80个国家和地区上市。最近,Aubagio还获得欧盟批准一线治疗10-17岁儿科患者,成为该地区一线治疗MS儿童和青少年的第一个口服MS疗法。
在中国,Aubagio(中文商品名:奥巴捷)于2018年7月获批上市,是国内批准治疗MS的首个口服疾病修正治疗(DMT)药物。
ULTIMATE I & II研究(NCT03277261;NCT03277248)调查了ublituximab 450mg静脉输注(第1天150mg[静脉输注4小时以上],第15天450mg[静脉输注1小时以上],之后每6个月给药一次450mg[静脉输注1小时以上])、Aubagio(14mg口服片,每日一次)治疗RMS患者的疗效和安全性。2项研究的结果如下:
——主要终点-年化复发率(ARR)结果:在ULTIMATE I研究中,ublituximab治疗组的ARR为0.076,而Aubagio治疗组的ARR为0.188,相对降低了约60%(p<0.0001)。在ULTIMATE II研究中,ublituximab治疗组的ARR为0.091,而Aubagio治疗组的ARR为0.178,相对降低了约50%(p=0.0022)。
——MRI结果:在ULTIMATE I和ULTIMATE II研究中,ublituximab治疗组与Aubagio治疗组相比,MRI扫描的T1钆增强(Gd+T1)病灶总数分别减少了97%和96%(p<0.0001)、新的或扩大的T2病灶数量分别接受了92%和90%(p<0.0001)。
——无疾病活动证据(NEDA)结果:在ULTIMATE I研究中,ublituximab治疗组有44.6%的患者达到NEDA,比Aubagio治疗组改善198%(p<0.0001)。在ULTIMATE II研究中,ublituximab治疗组有43%的患者达到NEDA,比Aubagio治疗组改善了277%(p<0.0001)。
——预先指定的汇总残疾结果:(1)所有治疗组的残疾进展率都很低。ublituximab治疗组有5.2%(Aubagio治疗组有5.9%)的患者出现12周确认残疾进展(CDP)、有3.3%(Aubagio治疗组有4.8%)的患者出现24周CDP。2者在统计学上均没有显著差异。(2)ublituximab治疗组实现12周确认残疾改善(CDI)和24周CDI的患者比例增加,与Aubagio相比12周CDI几率增加了116%(12% v 6%;p=0.0003)、24周CDI几率增加103%(9.6% v 5.1%;p=0.0026)。
——安全性:ublituximab总体耐受性良好,无意外安全信号。总体而言,在2项研究的汇总分析中,ublituximab组发生不良事件的患者比例与Aubagio组相似(每个治疗组约88%);与ublituximab相关的最常见不良事件是输液相关反应(ublituximab组有47.7%的患者出现至少一次输液相关反应,而Aubagio组为12.2%)。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



