肿瘤免疫微环境中的外泌体研究进展
来源:本站原创 2021-06-11 09:47
近几十年来,细胞外小泡(EVs)作为细胞间通讯的主要媒介,参与了多种重要的生理和病理过程,引起了人们的极大关注。它们几乎由所有类型的细胞分泌,并携带生物活性物质,如蛋白质、脂质和核酸,这些物质可以从宿主细胞传递给受体细胞,从而引发受体细胞的表型和功能变化。新近研究表明,EVS在重塑肿瘤免疫微环境(TIME)中起重要作用。来源于肿瘤细胞和免疫细胞的EV介导近端
近几十年来,细胞外小泡(EVs)作为细胞间通讯的主要媒介,参与了多种重要的生理和病理过程,引起了人们的极大关注。它们几乎由所有类型的细胞分泌,并携带生物活性物质,如蛋白质、脂质和核酸,这些物质可以从宿主细胞传递给受体细胞,从而引发受体细胞的表型和功能变化。新近研究表明,EVS在重塑肿瘤免疫微环境(TIME)中起重要作用。来源于肿瘤细胞和免疫细胞的EV介导近端和远端的相互通讯,决定肿瘤的命运和抗肿瘤的疗效。本文就EVS在重塑时间和调节肿瘤特异性免疫中的作用及其研究现状作一综述。作者主要讨论了肿瘤细胞和肿瘤浸润性免疫细胞之间通过EVS的递送相互调节,还描述了目前研究的局限性,并讨论了进一步研究的方向。
图片来源:https://doi.org/10.1016/j.canlet.2021.05.032
肿瘤不仅包括不同亚群的肿瘤细胞,还包括与肿瘤相关的成纤维细胞、天然和获得性免疫细胞(如单核/巨噬细胞、树突状细胞、中性粒细胞、髓系抑制细胞、自然杀伤细胞、T细胞和B细胞)、血管系统、分泌因子和广泛的细胞外基质(ECM)网络,统称为肿瘤微环境(TME)。酸度、缺氧和营养缺乏是TME的共同特征,在肿瘤进展过程中提供了强大的选择压力。肿瘤在恶劣和复杂的肿瘤微环境中发展,细胞间的通讯通过各种信号网络发生,这些信号网络在肿瘤的进展和转移中起着关键作用。TME中的细胞间通讯介质包括细胞因子、趋化因子、生长因子、信号分子及其受体、肿瘤细胞和间质细胞以及细胞外小泡。
细胞外小泡(EVs)是几乎所有类型的细胞都能分泌的膜包裹小泡,它们可以将生物活性物质(如蛋白质、核酸、脂质和代谢物)从宿主细胞转移到邻近的受体细胞和远端受体细胞,从而在细胞外空间协调一个持久的通讯网络。肠病毒广泛存在于血液、尿液、唾液和母乳等体液中,具有生物相容性、生物屏障通透性、低毒和低免疫原性等特性。由于这些独特的特征,EV被认为是很有前途的临床生物标志物和纳米载体,能够对疾病进行非侵入性的早期诊断、监测和治疗。Ev最初被认为是清除不需要的细胞成分的"废物处理手段";相反,它们现在被认为是参与各种基本生理和病理过程的细胞间调节的重要介质。在TME中,来自不同来源的EV,包括肿瘤细胞、免疫细胞和其他基质细胞,在肿瘤进展的多个方面发挥着不同的关键作用。在这篇综述中,作者提供了对EVS的生物发生、排泄和摄取的最新见解,并重点介绍了EVS在重塑肿瘤免疫微环境(TIME)中的作用。最后讨论了当前研究的局限性和进一步研究的方向。
肿瘤微环境被认为是一个复杂的环境,以缺氧、低pH和营养缺乏为主要特征,肿瘤细胞经常与肿瘤浸润的免疫细胞进行通讯,以支持肿瘤的发展。肿瘤微环境应激已被证明在肿瘤免疫逃逸和肿瘤进展中起关键作用。例如,微环境酸中毒可以诱导广泛的免疫逃逸机制的启动,通过这种机制,肿瘤细胞损害免疫细胞(包括T细胞、NK细胞和树突状细胞)的抗肿瘤活性,并促进免疫抑制细胞亚群的积累和激活,如髓系来源的抑制细胞和调节性T细胞,从而有利于肿瘤的进展。许多研究表明,通过细胞外小泡传递肿瘤产生的抑制或激活分子信号可以导致肿瘤浸润的免疫细胞重新编程,使免疫细胞在肿瘤进展过程中发挥重要作用。
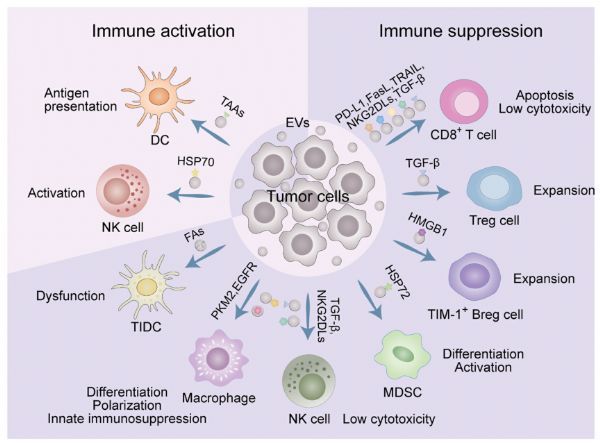
肿瘤来源的EV通过招募和诱导免疫抑制细胞(包括调节性B细胞(Breg)、调节性T细胞(Treg)、髓源性抑制细胞(MDSCs)、M2样肿瘤相关巨噬细胞(TAMs)和中性粒细胞)的分化来发挥免疫抑制活性,这些细胞包括调节性B细胞(Breg)、调节性T细胞(Treg)、髓源性抑制细胞(MDSCs)、M2样肿瘤相关巨噬细胞(TAMs)和中性粒细胞。肿瘤来源的EV已被证明可以调节Breg细胞的促肿瘤特性。肝细胞癌(HCC)来源的胞外体高迁移率族蛋白1(HMGB1)可诱导T细胞免疫球蛋白和粘蛋白结构域1(Tim-1)+Breg细胞增殖,这些细胞通过分泌白细胞介素10(IL-10)和损害CD8+T细胞功能而产生免疫抑制的微环境。同样,肿瘤来源的胞外体转化生长因子β(tgf-β)参与了外周血中前体细胞对treg细胞的扩增,扩增后的细胞可以产生转化生长因子-β(tcf-β),进而发挥抑制作用。髓系来源的抑制细胞(MDSCs)也被肿瘤来源的EVS激活。一个例子是肿瘤来源的胞外表面蛋白72 kDa热休克蛋白(Hsp72),它可以通过Hsp72-Toll样受体2(TLR2)轴介导的信号转导和转录激活因子3(STAT3)激活来触发MDSCs的T细胞依赖性免疫抑制功能。此外,肿瘤来源的外切体可以通过转化生长因子-β介导的抑制T细胞增殖和细胞溶解功能,使单核细胞向MDSCs分化。
肿瘤细胞外小泡在肿瘤免疫微环境中的作用
图片来源:https://doi.org/10.1016/j.canlet.2021.05.032
近几十年来,对细胞外小泡的生物学、功能和生物医学应用的了解已经取得了重大进展,但还需要进一步的研究,以完全解决EV亚型的准确分类,并阐明这些EV如何在肿瘤进展和肿瘤免疫治疗中发挥多种作用。来源细胞对EVS的选择性分选,受体细胞对某些EVS的特异性摄取,以及EV货物在受体细胞中的独特功能,似乎是EVS在当时不同功能的主要决定因素。对不同EV亚群的生物发生、性质和有效成分的研究进展,不仅有助于理解EV亚群在当时的功能作用,而且有助于识别临床生物标志物和设计治疗肿瘤的药物干预措施。尽管人们对胞外囊泡的兴趣与日俱增,为利用胞外体和胞外体作为临床生物标记物、肿瘤疫苗和药物载体开辟了一条道路,但挑战依然存在。目前还不清楚哪些细胞类型适合生产临床级EV。此外,临床急需规模化的EV纯化、生产和保存技术。还应提高EVS的抗原或药物载药率,以开发令人满意的EV疫苗和抗肿瘤疗法。总之,深入了解EVS在肿瘤免疫微环境中的不同作用以及开发精确设计EVS的方法将有助于EV抗肿瘤治疗。(生物谷 Bioon.com)
参考资料
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->