2020年8月HIV研究亮点进展
来源:本站原创 2020-08-30 23:56
2020年8月30日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴
2020年8月30日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,导致免疫系统瘫痪,从而致使各种疾病在人体内蔓延,最终导致艾滋病。由于HIV的变异极其迅速,难以生产特异性疫苗,至今无有效治疗方法,对人类健康造成极大威胁。
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的8月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Lancet HIV:新研究简化儿童HIV感染者服用度鲁特韦的剂量
doi:10.1016/S2352-3018(20)30189-2
感染HIV病毒的儿童如今可以受益于一种经过调整的、更简单的联合疗法。在联合疗法中,同时使用两种或三种药物来抑制HIV。其中的一种药物是度鲁特韦(dolutegravir)。在一项新的研究中,来自荷兰拉德堡德大学、英国伦敦大学学院、津巴布韦大学、乌干达联合临床研究中心、贝勒医学院儿童基金会、西班牙10月12日医院和意大利帕多瓦大学的研究人员发现在儿童中使用一种广泛可获得的度鲁特韦药丸在效果上与使用几种不太容易获得的这种药物药丸的组合一样好。特别是在感染人数较多且不易获得良好护理的国家,这使得治疗儿童更容易。这些研究结果被列入世界卫生组织(WHO)的治疗指南中。相关结果发表在2020年8月的Lancet HIV期刊上,论文标题为“Simplified dolutegravir dosing for children with HIV weighing 20 kg or more: pharmacokinetic and safety substudies of the multicentre, randomised ODYSSEY trial”。
这项研究的重点是简化儿童每天应该服用的度鲁特韦的剂量,这种剂量应该同样有效,而且不应该引起任何额外的副作用。他们的做法是给62名来自乌干达和津巴布韦的6至18岁的HIV阳性儿童服用不同剂量的度鲁特韦,并考虑到他们的体重。对他们进行了近半年的监测。结果显示,每天服用一粒50毫克的度鲁特韦,与成年人的剂量相同,对儿童的效果很好,他们的身体对这种药物的反应与更难给药的剂量相同。
2.Science子刊:我国科学家发现利用小分子ACA靶向TGF-β信号通路,可抑制包括新冠病毒、HIV和甲流病毒在内的一系列病毒
doi:10.1126/sciadv.aba7910
在一项新的研究中,来自中国香港大学、玛丽医院和海南医学院的研究人员鉴定出一种小分子,它通过靶向TGF-β信号通路,在组织培养物和小鼠体内抑制包括SARS-CoV-2在内的多种不同病毒。通过鉴定出多种病毒成功感染所依赖的一种宿主细胞途径,这一发现为开发广谱抗病毒药物提供了一种潜在的靶标。相关研究结果近期发表在Science Advances期刊上,论文标题为“Viruses harness YxxØ motif to interact with host AP2M1 for replication: a vulnerable broad-spectrum antiviral target”。
为了研究TGF-β信号通路是否可以作为对抗众多病毒的抗病毒疗法的靶点,香港大学微生物学系博士后研究员袁硕峰(Shuofeng Yuan)及其同事们对之前发现的该信号通路的抑制剂进行了筛选。他们发现一种这样的化合物,即小分子N-(p-Amylcinnamoyl)anthranilic acid(简称ACA),在组织培养物和小鼠中都成功地抑制了甲型流感病毒、MERS-CoV、SARS-CoV-2、HIV、腺病毒和两种小RNA病毒(picornavirus)。
他们还发现,ACA通过阻断AP2M1和许多病毒蛋白中存在的氨基酸基序YxxØ之间的相互作用来实现这种抑制作用。AP2M1是AP2接头复合体中的一个亚基,已知与TGF-β信号通路相互作用。
3.PLoS Pathog:多发性硬化症药物芬戈莫德可阻断HIV在人体免疫细胞中的感染和传播
doi:10.1371/journal.ppat.1008679
在一项新的研究中,美国乔治-华盛顿大学博士后研究员Rachel Resop、助理教授Alberto Bosque及其同事们发现作为一种经批准用于治疗多发性硬化症的免疫调节药物,芬戈莫德(fingolimod, FTY720)可阻断HIV病毒在人类免疫细胞中的感染和传播。虽然在未来还需在动物和人类身体开展研究,但是这些初步研究结果表明这种化合物可能是一种很有前途的HIV治疗和防御的新药物。相关研究结果近期发表在PLoS Pathogens期刊上,论文标题为“Fingolimod inhibits multiple stages of the HIV-1 life cycle”。
Bosque及其同事们研究了一种替代策略来对抗HIV感染:靶向鞘氨醇-1-磷酸(S1P)受体---一种参与感染进展的免疫系统组分。为此,他们重点研究了芬戈莫德---一种耐受性良好的药物,可以阻断S1P受体的作用,并获得了美国食品药物管理局(FDA)的批准用于治疗多发性硬化症。
他们发现,芬戈莫德通过阻碍HIV生命周期中的多个步骤,阻止HIV感染称为CD4+T细胞的人类免疫细胞。比如,芬戈莫德降低了CD4---一种在T细胞表面上发现的蛋白---的密度,从而抑制了这种病毒的结合和融合。这种药物阻断了HIV在细胞间的传播,从而降低了可检测到的潜伏病毒。据他们的介绍,此前尚未有人报道S1P通路在HIV感染建立过程中的作用,之前也没有人报道调节这一途径以改变感染过程或防止在CD4+T细胞中建立潜伏病毒库的潜力,因此,利用芬戈莫德靶向S1P通路可能是一种抑制HIV复制和减少潜伏病毒库的新策略。
4.PNAS:长效药物有助于治疗HIV
doi:10.1073/pnas.2009700117
在最近一项研究中,犹他大学健康科学家与美国国家过敏和传染病研究所(NIAID)的科学家开发了一种可注射的药物,可以阻止HIV进入细胞。这种新药有可能为感染提供长期的保护,而副作用则更少。该研究发表在《PNAS》杂志上。
在这项新研究中,研究人员测试了一种独特的名为CPT31的药物,该药物靶向HIV融合机制中很少突变的关键结构。由于CPT31不会在体内降解。因此,它们的使用寿命比天然多肽更长,因此特别适合作为长效可注射制剂。
5.Cell Rep:利用Sialyl-LewisX糖蛋白可识别在治疗期间潜藏的活跃HIV病毒库,为开发治愈HIV感染方法奠定基础
doi:10.1016/j.celrep.2020.107991
在一项新的研究中,来自美国威斯达研究所等研究机构的研究人员可能发现一种新的方法来鉴定和靶向在抗逆转录病毒药物(ART)治疗期间隐藏的HIV病毒库。这一发现可能对改善HIV阳性者的长期护理具有转化意义。相关研究结果近期发表在Cell Reports期刊上,论文标题为“Sialyl-LewisX Glycoantigen Is Enriched on Cells with Persistent HIV Transcription during Therapy”。
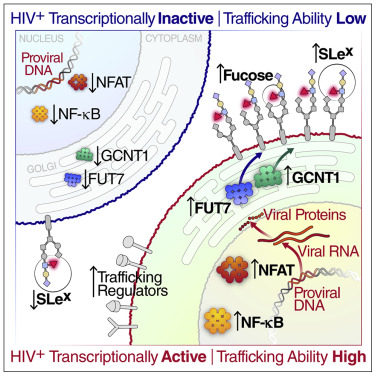
持续感染的免疫细胞可以分为两类:病毒完全沉默而不产生任何病毒RNA的细胞(即沉默的HIV病毒库);病毒产生低水平病毒RNA的细胞(即活跃的HIV病毒库)。靶向并消除这两种类型的HIV病毒库是寻求治愈HIV感染的重点。在这一探索中的一个主要挑战是,我们对这两种类型的感染细胞彼此之间以及与HIV未感染细胞之间有什么不同还没有一个清晰的认识。因此,鉴定能够区分这些细胞的标志物物是至关重要的。
这些作者鉴定出一种名为“岩藻糖基化(fucosylation)”的过程,这是病毒基因组正在积极地被转录的持续感染T细胞的一种特征。岩藻糖基化是一种叫做岩藻糖的糖分子附着在存在于细胞表面的蛋白上,对T细胞的激活至关重要。
这些作者还发现,一种名为Sialyl-LewisX(SLeX)的特异性岩藻糖基化蛋白的表达可以识别体内持续性的HIV转录,而且具有高水平SLeX的原代CD4 T细胞具有更高水平的T细胞通路和已知在ART治疗期间驱动HIV转录的蛋白。在病毒转录不活跃的HIV感染细胞表面上没有发现这样的糖基化模式,这就为这两种细胞类型提供了一个区别性的特征。有趣的是,他们还发现,HIV本身会促进这些细胞表面糖组学变化。
6.eLife:蛋白MARCH8利用不同的机制抑制HIV和VSV感染
doi:10.7554/eLife.57763
在一项新的研究中,来自日本国家传染病研究所、山梨大学和长崎国际大学的研究人员发现为了保护人类免受感染,一种称为MARCH8的蛋白对水泡性口炎病毒(VSV)进行标记以便它随后遭受破坏,而这种蛋白只是将HIV作为人质。相关研究结果于2020年8月11日发表在eLife期刊上,论文标题为“MARCH8 inhibits viral infection by two different mechanisms”。
之前的研究已表明,MARCH8通过靶向HIV和VSV进入人体细胞所必需的病毒蛋白来阻止这两种病毒进入这些细胞。但是这种蛋白如何做到这一点仍不清楚。这些作者猜测,MARCH8可能通过靶向一种名为赖氨酸的特殊氨基酸,对一种重要的VSV包膜蛋白进行标记以便它随后遭受破坏。
论文通讯作者、日本国家传染病研究所病理部首席研究员Kenzo Tokunaga解释说,“VSV G糖蛋白(VSV-G)有一个含有5个赖氨酸的短尾巴,这使得使它成为一个理想的靶标。相比之下,HIV包膜糖蛋白(Env)的尾巴非常长,仅含有两个赖氨酸,这使得MARCH8更难对它进行标记以便它随后遭受破坏。”
7.mBio:揭示HIV下调过氧化物酶体形成机制
doi:10.1128/mBio.03395-19; doi:10.1128/mBio.00967-20
在一项新的研究中,来自加拿大阿尔伯塔大学、蒙特利尔大学和蒙特利尔临床研究所的研究人员揭示在HIV患者中新发现的一种工作机制可能也导致针对COVID-19的新疗法。它揭示了HIV如何攻击过氧化物酶体(peroxisome),即在所有细胞中发现的一种有助于调节免疫系统、脂质代谢、心血管健康、大脑发育和神经功能的细胞器。相关研究结果近期发表在mBio期刊上,论文标题为“The HIV-1 Accessory Protein Vpu Downregulates Peroxisome Biogenesis”。
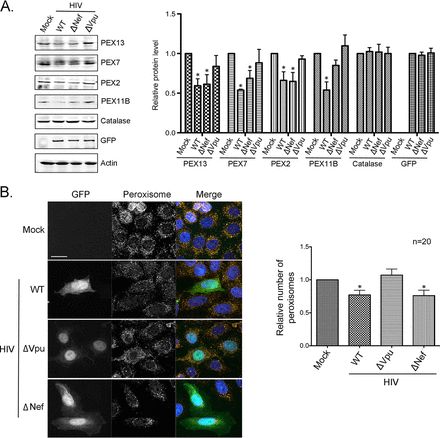
阿尔伯塔大学的Tom Hobman博士说,“我们知道,包括西尼罗河病毒和寨卡病毒在内的其他病毒有几种不同的机制来减少过氧化物酶体,以此来抑制阻止大多数病毒复制的干扰素产生。所有的病毒都有办法阻断这种干扰素反应,这符合过氧化物酶体是病毒感染的一个重要靶标的观点。”
8.Cell Rep:多组学研究揭示HIV-1感染细胞的详细特征和异质性
doi:10.1016/j.celrep.2020.107887
为了消除HIV感染,在体内阐明HIV-1感染细胞的详细特征和异质性就变得非常重要了,近日,一项刊登在国际杂志Cell Reports上的研究报告中,来自东京大学等机构的科学家们通过研究表示,利用基因修饰的HIV-1来感染造血干细胞移植的人源化小鼠模型或有望在体内揭示产生HIV-1的细胞的多种特性。
文章中,研究人员对HIV-1感染的细胞进行多组学分析,多组学分析能对全面调查分析生物性样本的特征,相关研究结果或有望帮助研究人员开发治疗HIV-1的新型疗法。最新开发的组学技术或许就能作为一种强大的工具来识别HIV-1感染细胞的特征,然而,感染者体内大部分的CD4+ T细胞或许并未被感染,因此,体内大量CD4+ T细胞的转录谱或许并不能反映纯粹产生HIV-1的细胞。
这项研究中,研究人员利用人类造血干细胞移植的人源化小鼠模型进行研究,这种模型能在体内相对稳定的免疫状况下维持人类的白细胞产生,同时还含有复制潜能的HIV-1;研究者利用最近新开发的四种技术来调查病毒的基因组和转录组学特征,研究人员进行了四项分析:1)首先利用微滴数字PCR就能揭示感染的人源化小鼠机体中潜在病毒库的存在;2)连接介导的PCR能够解释HIV-1会优先整合到开放的染色质区域,而整合位点的表观遗传学修饰与病毒产生的关联就揭示了这一点;3)数字RNA测序能够定量体内产生HIV-1细胞中病毒的绝对拷贝数,这就进一步能够识别出病毒感染和未感染细胞之间差异表达的基因;4)单细胞RNA测序能够揭示并且阐述体内产生HIV-1细胞的特性和异质性。(生物谷 Bioon.com)
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的8月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Lancet HIV:新研究简化儿童HIV感染者服用度鲁特韦的剂量
doi:10.1016/S2352-3018(20)30189-2
感染HIV病毒的儿童如今可以受益于一种经过调整的、更简单的联合疗法。在联合疗法中,同时使用两种或三种药物来抑制HIV。其中的一种药物是度鲁特韦(dolutegravir)。在一项新的研究中,来自荷兰拉德堡德大学、英国伦敦大学学院、津巴布韦大学、乌干达联合临床研究中心、贝勒医学院儿童基金会、西班牙10月12日医院和意大利帕多瓦大学的研究人员发现在儿童中使用一种广泛可获得的度鲁特韦药丸在效果上与使用几种不太容易获得的这种药物药丸的组合一样好。特别是在感染人数较多且不易获得良好护理的国家,这使得治疗儿童更容易。这些研究结果被列入世界卫生组织(WHO)的治疗指南中。相关结果发表在2020年8月的Lancet HIV期刊上,论文标题为“Simplified dolutegravir dosing for children with HIV weighing 20 kg or more: pharmacokinetic and safety substudies of the multicentre, randomised ODYSSEY trial”。

关于受HIV感染的T细胞的扫描电镜图,图片来自NIAID。
这项研究的重点是简化儿童每天应该服用的度鲁特韦的剂量,这种剂量应该同样有效,而且不应该引起任何额外的副作用。他们的做法是给62名来自乌干达和津巴布韦的6至18岁的HIV阳性儿童服用不同剂量的度鲁特韦,并考虑到他们的体重。对他们进行了近半年的监测。结果显示,每天服用一粒50毫克的度鲁特韦,与成年人的剂量相同,对儿童的效果很好,他们的身体对这种药物的反应与更难给药的剂量相同。
2.Science子刊:我国科学家发现利用小分子ACA靶向TGF-β信号通路,可抑制包括新冠病毒、HIV和甲流病毒在内的一系列病毒
doi:10.1126/sciadv.aba7910
在一项新的研究中,来自中国香港大学、玛丽医院和海南医学院的研究人员鉴定出一种小分子,它通过靶向TGF-β信号通路,在组织培养物和小鼠体内抑制包括SARS-CoV-2在内的多种不同病毒。通过鉴定出多种病毒成功感染所依赖的一种宿主细胞途径,这一发现为开发广谱抗病毒药物提供了一种潜在的靶标。相关研究结果近期发表在Science Advances期刊上,论文标题为“Viruses harness YxxØ motif to interact with host AP2M1 for replication: a vulnerable broad-spectrum antiviral target”。
为了研究TGF-β信号通路是否可以作为对抗众多病毒的抗病毒疗法的靶点,香港大学微生物学系博士后研究员袁硕峰(Shuofeng Yuan)及其同事们对之前发现的该信号通路的抑制剂进行了筛选。他们发现一种这样的化合物,即小分子N-(p-Amylcinnamoyl)anthranilic acid(简称ACA),在组织培养物和小鼠中都成功地抑制了甲型流感病毒、MERS-CoV、SARS-CoV-2、HIV、腺病毒和两种小RNA病毒(picornavirus)。
他们还发现,ACA通过阻断AP2M1和许多病毒蛋白中存在的氨基酸基序YxxØ之间的相互作用来实现这种抑制作用。AP2M1是AP2接头复合体中的一个亚基,已知与TGF-β信号通路相互作用。
3.PLoS Pathog:多发性硬化症药物芬戈莫德可阻断HIV在人体免疫细胞中的感染和传播
doi:10.1371/journal.ppat.1008679
在一项新的研究中,美国乔治-华盛顿大学博士后研究员Rachel Resop、助理教授Alberto Bosque及其同事们发现作为一种经批准用于治疗多发性硬化症的免疫调节药物,芬戈莫德(fingolimod, FTY720)可阻断HIV病毒在人类免疫细胞中的感染和传播。虽然在未来还需在动物和人类身体开展研究,但是这些初步研究结果表明这种化合物可能是一种很有前途的HIV治疗和防御的新药物。相关研究结果近期发表在PLoS Pathogens期刊上,论文标题为“Fingolimod inhibits multiple stages of the HIV-1 life cycle”。

图片来源:NIAID。
Bosque及其同事们研究了一种替代策略来对抗HIV感染:靶向鞘氨醇-1-磷酸(S1P)受体---一种参与感染进展的免疫系统组分。为此,他们重点研究了芬戈莫德---一种耐受性良好的药物,可以阻断S1P受体的作用,并获得了美国食品药物管理局(FDA)的批准用于治疗多发性硬化症。
他们发现,芬戈莫德通过阻碍HIV生命周期中的多个步骤,阻止HIV感染称为CD4+T细胞的人类免疫细胞。比如,芬戈莫德降低了CD4---一种在T细胞表面上发现的蛋白---的密度,从而抑制了这种病毒的结合和融合。这种药物阻断了HIV在细胞间的传播,从而降低了可检测到的潜伏病毒。据他们的介绍,此前尚未有人报道S1P通路在HIV感染建立过程中的作用,之前也没有人报道调节这一途径以改变感染过程或防止在CD4+T细胞中建立潜伏病毒库的潜力,因此,利用芬戈莫德靶向S1P通路可能是一种抑制HIV复制和减少潜伏病毒库的新策略。
4.PNAS:长效药物有助于治疗HIV
doi:10.1073/pnas.2009700117
在最近一项研究中,犹他大学健康科学家与美国国家过敏和传染病研究所(NIAID)的科学家开发了一种可注射的药物,可以阻止HIV进入细胞。这种新药有可能为感染提供长期的保护,而副作用则更少。该研究发表在《PNAS》杂志上。
在这项新研究中,研究人员测试了一种独特的名为CPT31的药物,该药物靶向HIV融合机制中很少突变的关键结构。由于CPT31不会在体内降解。因此,它们的使用寿命比天然多肽更长,因此特别适合作为长效可注射制剂。
5.Cell Rep:利用Sialyl-LewisX糖蛋白可识别在治疗期间潜藏的活跃HIV病毒库,为开发治愈HIV感染方法奠定基础
doi:10.1016/j.celrep.2020.107991
在一项新的研究中,来自美国威斯达研究所等研究机构的研究人员可能发现一种新的方法来鉴定和靶向在抗逆转录病毒药物(ART)治疗期间隐藏的HIV病毒库。这一发现可能对改善HIV阳性者的长期护理具有转化意义。相关研究结果近期发表在Cell Reports期刊上,论文标题为“Sialyl-LewisX Glycoantigen Is Enriched on Cells with Persistent HIV Transcription during Therapy”。

图片来自Cell Reports, 2020, doi:10.1016/j.celrep.2020.107991。
持续感染的免疫细胞可以分为两类:病毒完全沉默而不产生任何病毒RNA的细胞(即沉默的HIV病毒库);病毒产生低水平病毒RNA的细胞(即活跃的HIV病毒库)。靶向并消除这两种类型的HIV病毒库是寻求治愈HIV感染的重点。在这一探索中的一个主要挑战是,我们对这两种类型的感染细胞彼此之间以及与HIV未感染细胞之间有什么不同还没有一个清晰的认识。因此,鉴定能够区分这些细胞的标志物物是至关重要的。
这些作者鉴定出一种名为“岩藻糖基化(fucosylation)”的过程,这是病毒基因组正在积极地被转录的持续感染T细胞的一种特征。岩藻糖基化是一种叫做岩藻糖的糖分子附着在存在于细胞表面的蛋白上,对T细胞的激活至关重要。
这些作者还发现,一种名为Sialyl-LewisX(SLeX)的特异性岩藻糖基化蛋白的表达可以识别体内持续性的HIV转录,而且具有高水平SLeX的原代CD4 T细胞具有更高水平的T细胞通路和已知在ART治疗期间驱动HIV转录的蛋白。在病毒转录不活跃的HIV感染细胞表面上没有发现这样的糖基化模式,这就为这两种细胞类型提供了一个区别性的特征。有趣的是,他们还发现,HIV本身会促进这些细胞表面糖组学变化。
6.eLife:蛋白MARCH8利用不同的机制抑制HIV和VSV感染
doi:10.7554/eLife.57763
在一项新的研究中,来自日本国家传染病研究所、山梨大学和长崎国际大学的研究人员发现为了保护人类免受感染,一种称为MARCH8的蛋白对水泡性口炎病毒(VSV)进行标记以便它随后遭受破坏,而这种蛋白只是将HIV作为人质。相关研究结果于2020年8月11日发表在eLife期刊上,论文标题为“MARCH8 inhibits viral infection by two different mechanisms”。
之前的研究已表明,MARCH8通过靶向HIV和VSV进入人体细胞所必需的病毒蛋白来阻止这两种病毒进入这些细胞。但是这种蛋白如何做到这一点仍不清楚。这些作者猜测,MARCH8可能通过靶向一种名为赖氨酸的特殊氨基酸,对一种重要的VSV包膜蛋白进行标记以便它随后遭受破坏。
论文通讯作者、日本国家传染病研究所病理部首席研究员Kenzo Tokunaga解释说,“VSV G糖蛋白(VSV-G)有一个含有5个赖氨酸的短尾巴,这使得使它成为一个理想的靶标。相比之下,HIV包膜糖蛋白(Env)的尾巴非常长,仅含有两个赖氨酸,这使得MARCH8更难对它进行标记以便它随后遭受破坏。”
7.mBio:揭示HIV下调过氧化物酶体形成机制
doi:10.1128/mBio.03395-19; doi:10.1128/mBio.00967-20
在一项新的研究中,来自加拿大阿尔伯塔大学、蒙特利尔大学和蒙特利尔临床研究所的研究人员揭示在HIV患者中新发现的一种工作机制可能也导致针对COVID-19的新疗法。它揭示了HIV如何攻击过氧化物酶体(peroxisome),即在所有细胞中发现的一种有助于调节免疫系统、脂质代谢、心血管健康、大脑发育和神经功能的细胞器。相关研究结果近期发表在mBio期刊上,论文标题为“The HIV-1 Accessory Protein Vpu Downregulates Peroxisome Biogenesis”。

图片来自mBio, 2020, doi:10.1128/mBio.03395-19。
阿尔伯塔大学的Tom Hobman博士说,“我们知道,包括西尼罗河病毒和寨卡病毒在内的其他病毒有几种不同的机制来减少过氧化物酶体,以此来抑制阻止大多数病毒复制的干扰素产生。所有的病毒都有办法阻断这种干扰素反应,这符合过氧化物酶体是病毒感染的一个重要靶标的观点。”
8.Cell Rep:多组学研究揭示HIV-1感染细胞的详细特征和异质性
doi:10.1016/j.celrep.2020.107887
为了消除HIV感染,在体内阐明HIV-1感染细胞的详细特征和异质性就变得非常重要了,近日,一项刊登在国际杂志Cell Reports上的研究报告中,来自东京大学等机构的科学家们通过研究表示,利用基因修饰的HIV-1来感染造血干细胞移植的人源化小鼠模型或有望在体内揭示产生HIV-1的细胞的多种特性。
文章中,研究人员对HIV-1感染的细胞进行多组学分析,多组学分析能对全面调查分析生物性样本的特征,相关研究结果或有望帮助研究人员开发治疗HIV-1的新型疗法。最新开发的组学技术或许就能作为一种强大的工具来识别HIV-1感染细胞的特征,然而,感染者体内大部分的CD4+ T细胞或许并未被感染,因此,体内大量CD4+ T细胞的转录谱或许并不能反映纯粹产生HIV-1的细胞。
这项研究中,研究人员利用人类造血干细胞移植的人源化小鼠模型进行研究,这种模型能在体内相对稳定的免疫状况下维持人类的白细胞产生,同时还含有复制潜能的HIV-1;研究者利用最近新开发的四种技术来调查病毒的基因组和转录组学特征,研究人员进行了四项分析:1)首先利用微滴数字PCR就能揭示感染的人源化小鼠机体中潜在病毒库的存在;2)连接介导的PCR能够解释HIV-1会优先整合到开放的染色质区域,而整合位点的表观遗传学修饰与病毒产生的关联就揭示了这一点;3)数字RNA测序能够定量体内产生HIV-1细胞中病毒的绝对拷贝数,这就进一步能够识别出病毒感染和未感染细胞之间差异表达的基因;4)单细胞RNA测序能够揭示并且阐述体内产生HIV-1细胞的特性和异质性。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


