新冠疫情:273万!WHO意外泄露中国试验手稿,“人民的希望”瑞德西韦失败了?行业人士说不!
来源:本站原创 2020-04-24 15:06
2020年04月24日讯 /生物谷BIOON/ --目前,国外新冠肺炎疫情仍在迅速蔓延。根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2020年04月24日13时,全球累计确诊超过272.9万例,国外累计确诊超过264万例、死亡超过18.6万例。美国累计确诊超过88.6万例,死亡5万例。新冠疫情形势空前严峻,各国政府正在紧急授权,将有潜力的药物/疗法用

2020年04月24日讯 /生物谷BIOON/ --目前,国外新冠肺炎疫情仍在迅速蔓延。根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2020年04月24日15时,全球累计确诊超过273万例,国外累计确诊超过264.6万例、死亡超过18.6万例。美国累计确诊88.6万例,死亡5万例。
新冠疫情形势空前严峻,各国政府正在紧急授权,将有潜力的药物/疗法用于重症新冠肺炎的治疗,其中包括抗病毒药物、抗疟疾药物、抗炎药物、康复期血浆、血液净化技术等。当前,有多家药企已经投身新冠肺炎新疗法/疫苗研发行列,并已有多种疗法在新冠肺炎治疗方面显示出潜力。
在这些疗法中,来自吉利德的抗病毒药物——“人民的希望”瑞德西韦(remdesivir)关注度最高。今年2月,世界卫生组织(WHO)对瑞德西韦投下信任票,称该药潜力巨大,可能是治疗新冠肺炎的最佳候选药物。目前,瑞德西韦正通过同情用药以及扩大可及方案在重症患者的紧急救治方面发挥越来越大的作用。
可以说,有关瑞德西韦的任何一个消息都时刻牵动着行业的神经。该药最近的一些消息包括《新英格兰医学杂志》(NEJM)上发表的同情用药治疗重症患者的首批数据、吉利德官宣在中国开展的2项临床试验因患者入组不足而提前终止等等。
瑞德西韦是一种广谱抗病毒药物,也是最早被证实有潜力治疗新型冠状病毒肺炎(COVID-19)的药物之一。目前,全世界都在等待该药临床试验结果的公布。本月中旬,美国芝加哥大学医学院泄露了部分早期临床数据,引发了行业轰动:125例患者参与吉利德2项临床试验,其中113例重症,接受瑞德西韦治疗后,几乎全部患者在一周内出院,仅2例死亡。
然而,近日泄露的另一项临床试验数据,为民众对瑞德西韦不断高涨的期望泼了一盆冷水!国外生物技术网站FierceBiotech发表一篇文章称,据英国《金融时报》的报道,世界卫生组织(WHO)意外披露了一项中国临床试验的数据,该研究显示,瑞德西韦既没有改善患者的病情,也没有抑制患者血液中的病毒数量。《金融时报》称,该项试验是“失败的”。
但真的失败了吗?行业人士对这一观点说不!
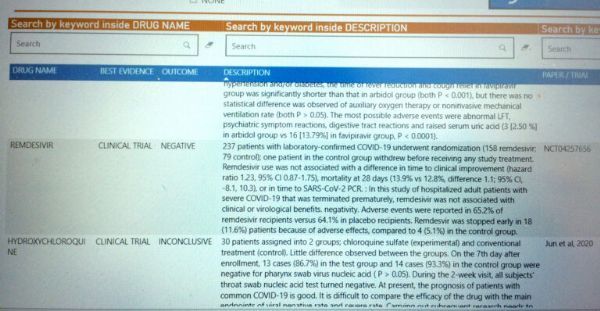
根据WHO无意中公布的文件草稿,这项临床试验最初的设计是招募453例重症成人患者,但实际仅入组了237例,瑞德西韦组有159例患者,对照组有79例患者。数据显示,瑞德西韦组与对照组在临床改善时间(HR=1.23,95%CI:0.87-1.75)和28天死亡率(13.9% vs 12.8%;差异=1.1;95%CI:-8.1,10.3)没有差异、副作用发生率大致相同(65.2% vs 64.1%)。与对照组相比,瑞德西韦组有更多的患者因副作用而提前停止治疗(11.8% vs 5.1%)。文件草稿称,该研究已提前终止,并称瑞德西韦与临床益处或病毒学益处不相关。
这份文件草稿随后被WHO删除,却被《金融时报》和美国媒体STATnews铺捉到。对于此次“意外”,WHO发言人Daniela Bagozzi表示:“作者向WHO提供了一份手稿草稿,并被无意中张贴在了网站上,在发现错误后已经立即删除。这份手稿目前正在接受同行审查,我们正在等待最终版本,之后WHO才会对此发表评论。”
Evercore ISI分析师Umer Raffat在给客户的一份报告中指出,此次披露的这项研究中,允许患者在症状首次出现后12天内启动瑞德西韦治疗。这是一个很长的窗口,对于治疗急性感染的抗病毒药物,“越早启动治疗,效果越好”,“对我来说,关于早期启动瑞德西韦治疗的患者疗效,真正的细节尚不清楚”。
吉利德方面也对试验失败的说法表示异议。吉利德首席医疗官Merdad Parsey医学博士在一份声明中称:“我们认为这份文稿包含了对这项研究的不恰当描述。由于患者入组率低,这项研究已提前终止,因此无法得出具有统计学意义的结论。虽然结果还没有定论,但我们确实看到,数据趋势表明瑞德西韦有潜在的益处,特别是在疾病早期治疗的患者中。”
华尔街知名投行Jefferies分析师Michael Yee也强调,这项研究提前结束是因为难以招募到患者。Michael Yee在周四的一份报告中写道:“我们重申,这项研究是在中国进行的,但由于患者入组率低而停止,而且从未完成;我们反复说过,瑞德西韦可能会有所帮助,但无论如何也不可能是灵丹妙药。”这与吉利德对这些数据的看法相呼应。
上周,美国芝加哥大学医学院泄露的早期数据显示,瑞德西韦治疗能迅速缓解重症COVID-19患者的发热和呼吸系统症状。该医学院正在参与2项由吉利德赞助的III期临床试验,试验中没有对照组。
Evercore ISI分析师Umer Raffat表示,“我认为,真相就在中间”。
瑞德西韦临床结果公布时间表:4月底重症开放标签试验、5月初中症开发标签试验、5月底不同严重程度双盲安慰剂对照试验
目前,有多项III期试验正在评估瑞德西韦在抗击新型冠状病毒(SARS-CoV-2)方面的有效性。除了开展2项III期试验外,吉利德还将瑞德西韦提供给了其他赞助者(包括中国的赞助者)进行研究,该公司还通过同情用药项目将瑞德西韦提供给了全球超过1700例患者。美国国家过敏症和传染病研究所(NIAID)正在进行一项将瑞德西韦与安慰剂对比的研究,而吉利德正在中度COVID-19患者中将2种瑞德西韦方案与标准护理治疗进行比较。
吉利德首席医疗官Merdad Parsey医学博士表示:“这些研究将有助于明确瑞德西韦的治疗对象、治疗的启动时间以及持续时间。这些研究有的已经完成初级分析所需的全部入组,有的按照计划即将完成入组。”
在今日发布的一份声明中,吉利德表示:我们预期在本月底发布我们针对瑞德西韦用于新型冠状病毒肺炎重症患者的开放标签研究的结果。这是一项随机的临床试验,已经完成全部的患者入组,研究将比较使用瑞德西韦5天或10天后的治疗结果和安全性。我们预期在五月底获得对中症患者的开放标签研究数据,该研究将对比患者使用瑞德西韦5天、10天以及接受标准治疗的结果。我们预计,五月底还可以获得美国国家过敏和传染病研究所(NIAID)对不同严重程度的患者进行的瑞德西韦双盲、安慰剂对照研究的数据。
目前,全世界都在等待吉利德公布相关临床试验结果。我们希望,“人民的希望”瑞德西韦不要辜负了大众的期望。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->