Nature:发现导致致命心脏病的基因突变!新药指日可待!
来源:本站原创 2019-07-22 07:58
2019年7月22日讯 /生物谷BIOON /——斯坦福大学医学院(Stanford University School of Medicine)的研究人员进行的一项研究表明,一种与扩张性心肌病(心脏主泵房的危险增大)有关的基因突变,激活了正常情况下在健康成年人心脏中关闭的生物通路。研究发现,通过化学药物抑制这一途径,可以纠正实验室培养皿中患者衍生心脏细胞的突变效应。更关键的是,研究人员使用的药物
2019年7月22日讯 /生物谷BIOON /——斯坦福大学医学院(Stanford University School of Medicine)的研究人员进行的一项研究表明,一种与扩张性心肌病(心脏主泵房的危险增大)有关的基因突变,激活了正常情况下在健康成年人心脏中关闭的生物通路。
研究发现,通过化学药物抑制这一途径,可以纠正实验室培养皿中患者衍生心脏细胞的突变效应。更关键的是,研究人员使用的药物已经获得了美国食品和药物管理局的批准。
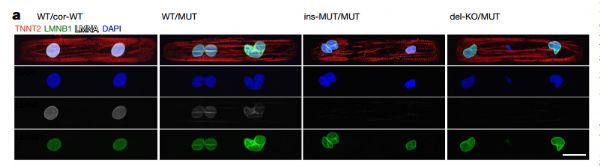
图片来源:Nature
这项研究结果于近日发表在《Nature》杂志上。研究结果表明,现有药物总有一天会被重新用于治疗扩张性心肌病。从更广泛的意义上说,这项研究表明,患者的心脏细胞可以帮助科学家更好地研究心脏,并筛选新的候选药物。
"有了10毫升的血液,我们就可以在一个盘子里制造出供临床使用的大量跳动的心脏细胞,"该研究的主要作者、医学博士、斯坦福心血管研究所所长、该技术的先驱Joseph Wu说道。"如果你告诉我你正在服用一种治疗心脏疾病的药物,比如受体阻滞剂或他汀类药物,我们可以添加这些药物来观察它对心脏的影响。这就是这种方法的美妙之处。"
研究人员研究了扩张性心肌病相关基因突变患者的心肌细胞。核纤层蛋白突变的心脏细胞(形成了核包膜的一部分)就像患有这种疾病的病人一样,无法正常跳动。科学家们发现,这种缺陷是血小板衍生生长因子通路激增的结果。这种途径对于血管的形成很重要,通常只有在心脏第一次形成或处于压力之下时才会被激活。用现有的药物抑制剂治疗心脏细胞可以恢复正常的节律跳动。
不要停止跳动
在扩张性心肌病中,心脏的主泵腔,左心室,扩张得如此之大,以至于心脏不再有规律地跳动。患者会出现呼吸急促、胸痛以及严重的心脏骤停。大约每250名美国人中就有1人患有某种形式的扩张性心肌病,其确切病因尚不清楚,但其中20%至35%的病例发生在家庭中。
先前的研究将核纤层蛋白突变与家族性扩张性心肌病联系起来,但这似乎是一种奇怪的联系。核纤层蛋白形成了核膜的一部分,这种结构将DNA从细胞的其他部分分离出来,并调节分子进出细胞核的运动--这看上去并不是调节心脏功能的主要因子。
Wu教授说:"我们很困惑。为什么不涉及心脏的挤压,如肉瘤蛋白,或心脏的电生理学,如离子通道核包膜蛋白的突变会导致扩张性心肌病?"
为了解开这个谜团,研究人员需要研究心肌细胞中的核包膜蛋白突变。研究人员要么从病人的心脏切除组织样本--一种侵入性的医疗程序,不是一个好的选择;要么使用老鼠组织,但老鼠的发现在人类中并不总是站得住脚。
相反,科学家们通过倒转病人皮肤细胞的生物钟来产生心脏细胞,从而产生诱导的多能干细胞,这种干细胞可以成为全身发现的任何一种特殊细胞。尽管研究人员在研究中使用了皮肤细胞,但Wu表示同样的技术也可以用10毫升的血液细胞。
心脏肌肉细胞在盘子里有节奏地跳动,就像它们在身体里一样。但是,来自一个有核包膜蛋白突变和扩张性心肌病史的家族成员的细胞的节律明显异常,并且有不规则的电活动。这种缺陷可以通过使用基因编辑技术进行修复。此外,将这种突变引入到健康患者的细胞中会导致这些细胞跳动过快。有核包膜蛋白突变的细胞的钙水平异常--一种调节肌肉收缩的关键离子。
恢复节奏
作为核膜的一部分,核包膜蛋白与一种被称为异染色质的紧密结合的DNA相互作用。有趣的是,研究人员通过各种DNA测序技术发现,具有核包膜蛋白突变的细胞含有较少的异染色质区域。由于DNA包装会影响哪些基因被激活或被关闭,研究人员研究了基因激活模式,以确定在突变的细胞中哪些通路出了问题--以及他们能做些什么。
"尽管我们做了所有这些测序和其他实验,但如果没有特定的目标,我们也无法提供正确的治疗,"该研究的主要作者、前博士后、现为韩国成均馆大学药学院助理教授的Jaecheol Lee博士说。
他们发现突变细胞中近250个基因比正常细胞中更活跃。许多基因是血小板衍生生长因子(PDGF)通路的一部分。当研究人员测试扩张性心肌病患者的心脏组织时,他们发现同样的通路被激活了。
但是PDGF通路的激活是否会引起异常的节律呢?为了测试这一点,研究人员用两种药物--克雷诺拉尼和舒尼替尼--来治疗心脏细胞,这两种药物可以抑制关键的PDGF受体。治疗后,核包膜蛋白突变的心脏细胞开始更有规律地跳动,它们的基因激活模式与来自健康捐献者的细胞更为接近。
这两种药物被FDA批准用于治疗各种癌症。但是Wu的团队之前的工作表明,这些药物在高剂量下可能会损害心脏,这将使找到正确的剂量或更安全的替代方案变得至关重要。
目前的研究的目的是利用这些患者细胞在培养皿中筛选和发现新药。这就是为什么Wu实验室从1000多名患者身上产生了心肌细胞,其中包括他自己、他的儿子和女儿。
"我们的博士后采集了我的血液,并将我的多能干细胞分化成脑细胞、心脏细胞和肝细胞,"Wu说。"他们帮我测试了一些我可能需要在未来服用的药物。"(生物谷Bioon.com)
参考资料:
Joseph C. Wu et al. Activation of PDGF pathway links LMNA mutation to dilated cardiomyopathy, Nature (2019). DOI: 10.1038/s41586-019-1406-x
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->